1 . 控制变量法是科学研究的重要方法。相同质量的锌与足量的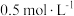 硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
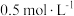 硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是| 选项 | 锌的状态 | 实验温度 |
| A | 粉末 | 20 |
| B | 粉末 | 30 |
| C | 块状 | 20 |
| D | 块状 | 30 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 醋酸亚铬 为砖红色晶体,难溶于冷水,易与酸反应,可用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌将三价铬反应为二价铬;二价铬再与醋酸钠
为砖红色晶体,难溶于冷水,易与酸反应,可用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌将三价铬反应为二价铬;二价铬再与醋酸钠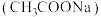 溶液作用即可制得醋酸亚铬。实验装置如图所示,试回答下列问题:
溶液作用即可制得醋酸亚铬。实验装置如图所示,试回答下列问题:___________ ,仪器a的名称是___________ 。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开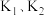 ,关闭
,关闭 ,c中溶液由绿色逐渐变为亮蓝色,同时c中有气体产生,写出生成该气体的化学方程式
,c中溶液由绿色逐渐变为亮蓝色,同时c中有气体产生,写出生成该气体的化学方程式___________ ,在这一步中该气体的作用是___________ 。
(3)打开___________ ,关闭___________ ,c中亮蓝色溶液流入d,d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是___________ 、___________ 、洗涤、干燥。
(4)指出装置d可能存在的缺点___________ 。
 为砖红色晶体,难溶于冷水,易与酸反应,可用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌将三价铬反应为二价铬;二价铬再与醋酸钠
为砖红色晶体,难溶于冷水,易与酸反应,可用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌将三价铬反应为二价铬;二价铬再与醋酸钠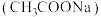 溶液作用即可制得醋酸亚铬。实验装置如图所示,试回答下列问题:
溶液作用即可制得醋酸亚铬。实验装置如图所示,试回答下列问题:
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开
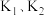 ,关闭
,关闭 ,c中溶液由绿色逐渐变为亮蓝色,同时c中有气体产生,写出生成该气体的化学方程式
,c中溶液由绿色逐渐变为亮蓝色,同时c中有气体产生,写出生成该气体的化学方程式(3)打开
(4)指出装置d可能存在的缺点
您最近一年使用:0次
3 . 我国科研人员提出了由 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意图如下所示。
的催化反应历程,该历程示意图如下所示。
 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意图如下所示。
的催化反应历程,该历程示意图如下所示。
| A.该反应为化合反应 |
| B.该反应历程中催化剂可改变反应速率 |
| C.该历程中三种含碳化合物碳元素化合价均相同 |
D.生成的 中C、H、O元素的质量比为 中C、H、O元素的质量比为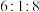 |
您最近一年使用:0次
名校
4 .  为阿伏加德罗常数的值下列说法正确的是
为阿伏加德罗常数的值下列说法正确的是
 为阿伏加德罗常数的值下列说法正确的是
为阿伏加德罗常数的值下列说法正确的是A.标准状况下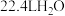 中含有的分子数为 中含有的分子数为 |
B.常温常压下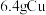 与足量 与足量 充分反应转移的电子数为 充分反应转移的电子数为 |
C.常温常压下 的 的 溶液中含有的 溶液中含有的 数目为 数目为 |
D.标准状况下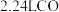 和 和 混合气体中含有的碳原子数为 混合气体中含有的碳原子数为 |
您最近一年使用:0次
5 . 水垢可以看作由多种物质组成的混合物,化学组成可表示为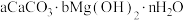 或
或 。为研究某锅炉水所形成水垢的化学组成,取水垢
。为研究某锅炉水所形成水垢的化学组成,取水垢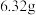 ,加热使其失去结晶水,得到
,加热使其失去结晶水,得到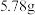 剩余固体A。高温灼烧A至恒重,放出的气体若用过量的
剩余固体A。高温灼烧A至恒重,放出的气体若用过量的 溶液吸收,得到
溶液吸收,得到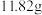 沉淀;若被碱石灰完全吸收,碱石灰增重2.82克。
沉淀;若被碱石灰完全吸收,碱石灰增重2.82克。
(1)写出高温灼烧固体A时所发生反应的化学方程式:_______ ;(写出任意正确的1个)
(2)通过计算判断该水垢中是否含有
_______ (填“有”或“无”)。
(3)计算固体A中 的质量是
的质量是_______ g。
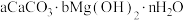 或
或 。为研究某锅炉水所形成水垢的化学组成,取水垢
。为研究某锅炉水所形成水垢的化学组成,取水垢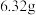 ,加热使其失去结晶水,得到
,加热使其失去结晶水,得到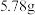 剩余固体A。高温灼烧A至恒重,放出的气体若用过量的
剩余固体A。高温灼烧A至恒重,放出的气体若用过量的 溶液吸收,得到
溶液吸收,得到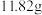 沉淀;若被碱石灰完全吸收,碱石灰增重2.82克。
沉淀;若被碱石灰完全吸收,碱石灰增重2.82克。(1)写出高温灼烧固体A时所发生反应的化学方程式:
(2)通过计算判断该水垢中是否含有

(3)计算固体A中
 的质量是
的质量是
您最近一年使用:0次
名校
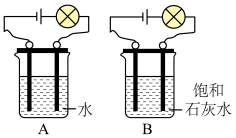
6 . 某化学兴趣小组用如图所示的装置,对氢氧化钙溶液进行探究。_______ ;通电相同时间,发现B装置中两个电极附近产生气泡比A装置多,此条件下产生气泡的化学方程式为_______ 。
(2)接通直流电,同时利用温度传感器测量溶液的温度。观察到B装置中插入溶液的两个碳棒(石墨)电极附近有气泡产生,一段时间后发现烧杯中的溶液的温度由 变为
变为 ,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是
,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是_______ ,还可能是_______ 。
(3)仔细观察,发现B装置中,白色浑浊出现在正极附近。联想电解水时,与电源正极相连的电极附近产生的_______ 气,它可能与石墨电极中的碳反应生成二氧化碳而使石灰水变浑浊,如果假设成立,则最后一步反应的化学方程式为_______ 。为了验证白色浑浊液体的成分,取上述实验得到的浑浊液体少量,滴加酚酞变红色,说明浑浊液体中还存在_______ 。
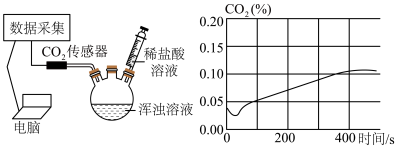
(4)将B装置中剩余浑浊液搅拌均匀后分成等体积的两份,第一组同学取一份加入一定量的稀盐酸,没有发现气泡产生。第二组同学取另一份倒入密封的三颈烧瓶中进行数字化实验。连接好传感器等装置,先开启测量二氧化碳含量的数据传感器,然后用注射器注入足量的稀盐酸数字化实验装置及所测量到的二氧化碳体积分数变化情况如图。_______ (除水外)。
实验反思:
①第一组同学的实验中,没有发现产生气泡,原因可能是_______ 。
②第二组同学在数字化实验中,发现曲线图开始时段的 百分比下降,可能的原因是
百分比下降,可能的原因是_______ 。
(2)接通直流电,同时利用温度传感器测量溶液的温度。观察到B装置中插入溶液的两个碳棒(石墨)电极附近有气泡产生,一段时间后发现烧杯中的溶液的温度由
 变为
变为 ,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是
,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是(3)仔细观察,发现B装置中,白色浑浊出现在正极附近。联想电解水时,与电源正极相连的电极附近产生的
(4)将B装置中剩余浑浊液搅拌均匀后分成等体积的两份,第一组同学取一份加入一定量的稀盐酸,没有发现气泡产生。第二组同学取另一份倒入密封的三颈烧瓶中进行数字化实验。连接好传感器等装置,先开启测量二氧化碳含量的数据传感器,然后用注射器注入足量的稀盐酸数字化实验装置及所测量到的二氧化碳体积分数变化情况如图。
实验反思:
①第一组同学的实验中,没有发现产生气泡,原因可能是
②第二组同学在数字化实验中,发现曲线图开始时段的
 百分比下降,可能的原因是
百分比下降,可能的原因是
您最近一年使用:0次
7 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
8 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
名校
9 . 请按要求完成下列方程式的书写。
(1) 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)金属钠投入氯化钠溶液_______ 。
(3)酸性条件下 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:_______ 。
(4)氢氧化铁受热分解:_______ 。
(1)
 与
与 反应的化学方程式:
反应的化学方程式:(2)金属钠投入氯化钠溶液
(3)酸性条件下
 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:(4)氢氧化铁受热分解:
您最近一年使用:0次
名校
10 . 物质的量是联系宏观和微观的桥梁:
(1) 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2) 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数_______ (填“相等”或“不相等”)
(3)含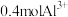 的
的 中所含的
中所含的 的个数是
的个数是_______ (用 表示),
表示), 的电离方程式是
的电离方程式是_______ 。
(4) 个
个 含
含_______ molO。
(1)
 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是(2)
 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数(3)含
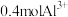 的
的 中所含的
中所含的 的个数是
的个数是 表示),
表示), 的电离方程式是
的电离方程式是(4)
 个
个 含
含
您最近一年使用:0次



