名校
解题方法
1 . 研发二氧化碳的碳捕集和碳利用技术是科学研究热点问题,其中催化转化法最具应用价值。回答下列问题:
(1)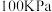 下,由最稳定单质生成
下,由最稳定单质生成 物质B的焓变,叫做物质B的标准摩尔生成焓
物质B的焓变,叫做物质B的标准摩尔生成焓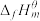 。298K,几种气态物质的标准摩尔生成焓如下表。
。298K,几种气态物质的标准摩尔生成焓如下表。
则

_______ 
(2)催化加氢制取甲醇,反应如下:
主反应:

副反应:

在一定条件下,向某 恒容密闭容器中充入
恒容密闭容器中充入
 和
和
 发生反应,起始总压强为
发生反应,起始总压强为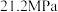 。实验测得
。实验测得 的平衡转化率和平衡时
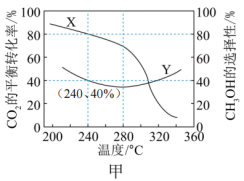
的平衡转化率和平衡时 的选择性随温度变化如图甲所示:
的选择性随温度变化如图甲所示:
已知: 的选择性
的选择性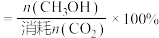 。
。
①图甲中表示平衡时 的选择性的曲线为
的选择性的曲线为_______ (填“X”或“Y”),温度高于280℃时,曲线Y随温度升高而升高的原因是_______ 。
②240℃时,反应 容器内达到平衡状态,副反应的
容器内达到平衡状态,副反应的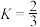 ,初始充入
,初始充入 的物质的量
的物质的量
_______ mol,主反应的平衡常数
_______ 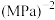 (用平衡分压代替平衡浓度,
(用平衡分压代替平衡浓度,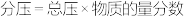 ;计算结果保留1位小数)。
;计算结果保留1位小数)。
(1)
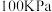 下,由最稳定单质生成
下,由最稳定单质生成 物质B的焓变,叫做物质B的标准摩尔生成焓
物质B的焓变,叫做物质B的标准摩尔生成焓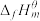 。298K,几种气态物质的标准摩尔生成焓如下表。
。298K,几种气态物质的标准摩尔生成焓如下表。则



| 物质 |  |  |  |  |
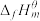 ( ( ) ) |  | 0 | 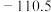 | 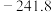 |
主反应:


副反应:


在一定条件下,向某
 恒容密闭容器中充入
恒容密闭容器中充入
 和
和
 发生反应,起始总压强为
发生反应,起始总压强为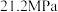 。实验测得
。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图甲所示:
的选择性随温度变化如图甲所示:
已知:
 的选择性
的选择性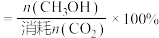 。
。①图甲中表示平衡时
 的选择性的曲线为
的选择性的曲线为②240℃时,反应
 容器内达到平衡状态,副反应的
容器内达到平衡状态,副反应的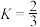 ,初始充入
,初始充入 的物质的量
的物质的量

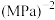 (用平衡分压代替平衡浓度,
(用平衡分压代替平衡浓度,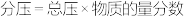 ;计算结果保留1位小数)。
;计算结果保留1位小数)。
您最近一年使用:0次
2 . 水煤合成气的生产和应用在化学工业中有极为重要的地位。回答下列问题:
(1)利用合成气(主要成分CO、CO2和H2)在催化剂作用下合成甲醇,可能发生的反应有:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-63 kJ•mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
③CH3OH(g)=CO(g)+2H2(g) ΔH3
已知部分化学键键能数据如下表:
则ΔH3=_______ kJ•mol-1。
(2)CO2和CH4在一定条件下反应也可制得合成水煤气。在1.0 L密闭容器中充入1.0 mol CH4和1.0 mol CO2,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
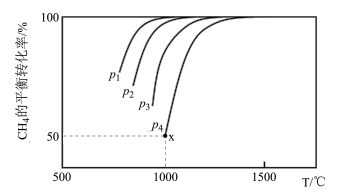
①比较压强大小:p1_______ p3(选填“>”、“<”或“=”)。
②若要提高CH4的平衡转化率,可采取的措施有_______ ,_______ 。(任写两条)
③若p4=2.0 MPa,则x点的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)化学家利用电化学原理回收CO2达到节能减排的目的,有一种实验设计的装置如下图所示。
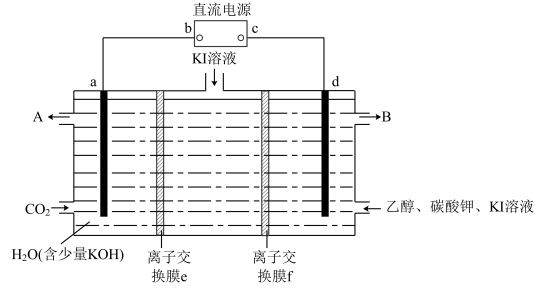
已知在碱性条件下,卤素单质可以将乙醇氧化为乙醛。实验一段时间后,测得a电极周围有甲酸根离子HCOO-生成。回答:
①电极b为_______ 极;
②电解时a电极附近溶液的pH_______ (选填“降低”、“升高”、“不变”);
③e为_______ 交换膜;
④d电极周围除了发生电极反应外,还有_______ (用离子方程式表示)。
(1)利用合成气(主要成分CO、CO2和H2)在催化剂作用下合成甲醇,可能发生的反应有:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-63 kJ•mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
③CH3OH(g)=CO(g)+2H2(g) ΔH3
已知部分化学键键能数据如下表:
| 化学键 | H-H | C=O | C≡O | O-H |
| 键能(kJ•mol-1) | 436 | 803 | 1076 | 465 |
(2)CO2和CH4在一定条件下反应也可制得合成水煤气。在1.0 L密闭容器中充入1.0 mol CH4和1.0 mol CO2,在一定条件下发生反应CH4(g)+CO2(g)
 2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
①比较压强大小:p1
②若要提高CH4的平衡转化率,可采取的措施有
③若p4=2.0 MPa,则x点的平衡常数Kp=
(3)化学家利用电化学原理回收CO2达到节能减排的目的,有一种实验设计的装置如下图所示。

已知在碱性条件下,卤素单质可以将乙醇氧化为乙醛。实验一段时间后,测得a电极周围有甲酸根离子HCOO-生成。回答:
①电极b为
②电解时a电极附近溶液的pH
③e为
④d电极周围除了发生电极反应外,还有
您最近一年使用:0次
2022-11-05更新
|
140次组卷
|
2卷引用:海南省海口中学2023-2024学年高二上学期12月月考化学试题



