名校
1 . 试从化学键的角度理解化学反应中的能量变化。(以2H2+O2=2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=_______ kJ;形成生成物中的化学键放出的总能量为=________ kJ。所以该反应要_____ (填“吸收”或“放出”)能量,能量变化值的大小△E=_______ kJ(填数值)
(2)由图可知,化学反应的本质是_____ 化学反应中能量变化的主要原因是_____ (从总能量说明)
(1)从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=
(2)由图可知,化学反应的本质是
您最近一年使用:0次
名校
解题方法
2 . 请参考题中图表,已知 E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
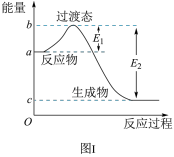
(1)图Ⅰ是 1mol NO2(g)和 1mol CO (g)反应生成 CO2(g)和 NO (g)过程中的能量变化示意图, 若在反应体系中加入催化剂,反应速率增大,E1的变化是______ (填“增大”、“减小”或“不变”, 下同),△H 的变化是 ______ 请写出 NO2和 CO 反应的热化学方程式: ______ 。
(2)将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H = +49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H = -192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) △H = -192.9 kJ·mol-1
又知③H2O(g) ═ H2O(l) △H = -44 kJ·mol-1,写出表示甲醇蒸 汽燃烧热的热化学方程式为:______ 。

(1)图Ⅰ是 1mol NO2(g)和 1mol CO (g)反应生成 CO2(g)和 NO (g)过程中的能量变化示意图, 若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H = +49.0 kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H = -192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) △H = -192.9 kJ·mol-1又知③H2O(g) ═ H2O(l) △H = -44 kJ·mol-1,写出表示甲醇蒸 汽燃烧热的热化学方程式为:
您最近一年使用:0次
2020-08-06更新
|
172次组卷
|
4卷引用:河南省郑州市第一中学2019-2020学年高二上学期入学测试化学试题



