名校
解题方法
1 . 氨是最重要的氮肥,是产量最大的化工产品之一、其合成原理为:N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ·mol−1。
I.在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应:
(1)测得反应放出的热量_______ 92.4kJ(填“小于”“大于”或“等于”)。
(2)当反应达到平衡时,N2和H2的浓度比是_______ ;N2和H2的转化率比是_______
(3)升高平衡体系的温度(保持体积不变),平衡将_______ (填“正向”“逆向”或“不”)移动,混合气体的平均相对分子质量_______ (填“变大”“变小”或“不变”)。
(4)当达到平衡时,充入氩气并保持压强不变,平衡将_______ (填“正向”“逆向”或“不”)移动。
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将_____ (填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度_____ (填“小于”“大于”或“等于”)原来的2倍。
II.该反应N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ·mol−1在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。
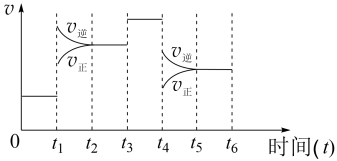
(6)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
t1_______ ,t3_______ ,t4_______
(7)下列时间段中,氨的百分含量最高的是_______。
I.在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应:
(1)测得反应放出的热量
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),平衡将
(4)当达到平衡时,充入氩气并保持压强不变,平衡将
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将
II.该反应N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ·mol−1在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。

(6)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
t1
(7)下列时间段中,氨的百分含量最高的是_______。
| A.0~t1 | B.t2~t3 | C.t3~t4 | D.t4~t5 |
您最近一年使用:0次



