解题方法
1 . TiO2和TiCl4均为重要的工业原料。已知:
Ⅰ.TiCl4(g)+O2(g) TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1
TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1
Ⅱ.2C(s)+O2(g) 2CO(g) ΔH2= -220.9kJ·mol-1
2CO(g) ΔH2= -220.9kJ·mol-1
请回答下列问题:
(1)TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为_____________________ 。升高温度,对该反应的影响为___________________________________ 。
(2)若反应Ⅱ的逆反应活化能表示为EkJ·mol-1,则E________ 220.9(填“>”“<”或“=”)。
(3)t℃时,向10 L恒容密闭容器中充入1molTiCl4和2 molO2,发生反应Ⅰ。5min达到平衡时测得TiO2的物质的量为0.2 mol。
①0~5 min 内,用Cl2表示的反应速率v(Cl2)=__________ 。
②TiCl4的平衡转化率a=__________________ 。
③下列措施,既能加快逆反应速率又能增大TiCl4的平衡转化率的是__________ (填选项字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分TiO2 D.增大O2浓度
④t℃时,向10 L恒容密闭容器中充入3 mol TiCl4和一定量O2的混合气体,发生反应Ⅰ,两种气体的平衡转化率(a)与起始的物质的量之比(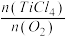 )的关系如图所示:
)的关系如图所示:
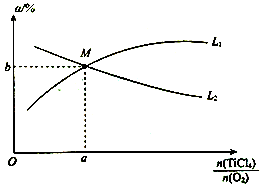
能表示TiCl4平衡转化率的曲线为__________ (填“L1”或“L2”);M点的坐标为___________ 。
Ⅰ.TiCl4(g)+O2(g)
 TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1
TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1Ⅱ.2C(s)+O2(g)
 2CO(g) ΔH2= -220.9kJ·mol-1
2CO(g) ΔH2= -220.9kJ·mol-1 请回答下列问题:
(1)TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为
(2)若反应Ⅱ的逆反应活化能表示为EkJ·mol-1,则E
(3)t℃时,向10 L恒容密闭容器中充入1molTiCl4和2 molO2,发生反应Ⅰ。5min达到平衡时测得TiO2的物质的量为0.2 mol。
①0~5 min 内,用Cl2表示的反应速率v(Cl2)=
②TiCl4的平衡转化率a=
③下列措施,既能加快逆反应速率又能增大TiCl4的平衡转化率的是
A.缩小容器容积 B.加入催化剂 C.分离出部分TiO2 D.增大O2浓度
④t℃时,向10 L恒容密闭容器中充入3 mol TiCl4和一定量O2的混合气体,发生反应Ⅰ,两种气体的平衡转化率(a)与起始的物质的量之比(
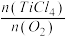 )的关系如图所示:
)的关系如图所示:
能表示TiCl4平衡转化率的曲线为
您最近一年使用:0次
2018-01-27更新
|
687次组卷
|
6卷引用:2020年北京高二下学期 复习模拟试题二(选修4人教版)
2020年北京高二下学期 复习模拟试题二(选修4人教版)河北省张家口市2018届高三上学期期末考试化学试题(已下线)【优等生百日捷进提升系列】专题01 化学反应速率与化学平衡原理综合应用安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题(已下线)2021年1月浙江高考化学试题变式题26-31



