名校
解题方法
1 . 向四个体积相同的密闭容器(甲、乙、丙、丁)中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列顺序正确的是
甲:在500℃时,10mol SO2和6mol O2反应
乙:在500℃时,用V2O5作催化剂,10mol SO2和5mol O2反应
丙:在450℃时,8mol SO2和5mol O2反应
丁:在500℃时,8mol SO2和5mol O2反应。
甲:在500℃时,10mol SO2和6mol O2反应
乙:在500℃时,用V2O5作催化剂,10mol SO2和5mol O2反应
丙:在450℃时,8mol SO2和5mol O2反应
丁:在500℃时,8mol SO2和5mol O2反应。
| A.甲、乙、丙、丁 | B.乙、甲、丙、丁 |
| C.乙、甲、丁、丙 | D.丁、丙、乙、甲 |
您最近一年使用:0次
2021-03-04更新
|
188次组卷
|
2卷引用:湖北省襄阳市襄州区第二高级中学2021-2022学年高一下学期期中考试化学试题
解题方法
2 . 研究发现,大多数化学反应并不是经过简单碰撞就能完成的,而往往经过多个反应步骤才能实现。碘钟反应是一种化学振荡反应,其体现了化学动力学的原理。某小组同学在室温下对某“碘钟实验”的原理进行探究。
资料:该“碘钟实验”反应分A、B两步进行:
反应A: (慢)
(慢)
反应B: (快)
(快)
(1)该“碘钟实验”的总反应是___ 。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向K2S2O8溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入试剂Y溶液,溶液的蓝色褪去。
试剂X是___ 、试剂Y是___ 。
(3)已知A反应的速率方程为: (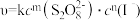 ),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
①表中V1=__ mL,理由是___ ;
②通过数据计算得知:m=___ ,n=___ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验III。(溶液浓度均为0.01mol/L)
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验III未产生颜色变化的原因:___ 。
资料:该“碘钟实验”反应分A、B两步进行:
反应A:
 (慢)
(慢)反应B:
 (快)
(快)(1)该“碘钟实验”的总反应是
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向K2S2O8溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入试剂Y溶液,溶液的蓝色褪去。
试剂X是
(3)已知A反应的速率方程为: (
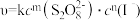 ),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)
),式中k为常数。为确定m、n值进行实验II。(溶液浓度均为0.01mol/L)| 实验 序号 | 试剂体积V/mL | 显色时间 t/s | ||||
| K2S2O8溶液 | KI溶液 | 水 | Na2S2O3溶液 | 淀粉溶液 | ||
| ① | 10 | 10 | 0 | 4 | 1 | 27.0 |
| ② | 5 | 10 | 5 | 4 | 1 | 54.0 |
| ③ | 2.5 | 10 | V1 | 4 | 1 | 108.0 |
| ④ | 10 | 5 | 5 | 4 | 1 | 54.0 |
②通过数据计算得知:m=
(4)为探究其他因素对该“碘钟实验”的影响,进行实验III。(溶液浓度均为0.01mol/L)
| 试剂体积V/mL | ||||
| K2S2O8溶液 | KI溶液 | 水 | Na2S2O3溶液 | 淀粉溶液 |
| 10 | 5 | 3 | 6 | 1 |
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验III未产生颜色变化的原因:
您最近一年使用:0次
名校
解题方法
3 . 下列过程中,需要增大化学反应速率的是
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氮 |
您最近一年使用:0次
2020-04-22更新
|
334次组卷
|
19卷引用:湖北省天门市三校2016-2017学年高一下学期期中考试化学试题
湖北省天门市三校2016-2017学年高一下学期期中考试化学试题(已下线)2010-2011学年江西省鄱阳县油墩街中学高一下学期期中考试化学试卷2015-2016学年四川省广安二中高一下学期期中化学试卷2016-2017学年天津市河东区高二上学期期中质检化学试卷福建省三明市第一中学2017-2018学年高二上学期期中考试(理)化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题江西省上饶市鄱阳县第二中学2019-2020学年高二上学期期中考试化学试题北京景山学校2021-2022学年高一下学期期中考试化学试题(已下线)2013-2014浙江省宁波市高一下学期期末考试化学试卷2014-2015学年广东省惠州市高一下学期期末考试化学文科试卷2015-2016学年青海省西宁四中高二上学期期末化学试卷2016-2017学年河北省武邑中学高二上入学考试化学试卷2016-2017学年河北省武邑中学高二上8.28周考化学卷2016-2017学年河北省武邑中学高二上9.21周考化学卷山西省怀仁县第八中学2016-2017学年高一(普通班)下学期期末考试化学试题河南省周口市陈州高级中学2019-2020学年高一下学期摸底考试化学试题山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题江苏省盐城市伍佑中学2020-2021学年高一下学期第一次阶段考试化学试题江苏省镇江实验高级中学2020-2021学年高一下学期第一次月考化学试题
4 . 一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是
| A.加少量稀NaOH溶液 | B.加入少量NaNO3固体 |
| C.加入少量NaHSO4固体 | D.加入少量CuSO4溶液 |
您最近一年使用:0次



