名校
1 . Ⅰ.将CO2转化为CO、CH3OH等燃料,可以有效的缓解能源危机,同时可以减少温室气体,实现“双碳目标”。
800℃时,H2还原CO2反应的热化学方程式及其平衡常数如下:
ⅰ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
(1)反应CO(g)+2H2(g) CH3OH(g) ΔH3=
CH3OH(g) ΔH3=___________ kJ·mol-1,K3=___________ 。
Ⅱ.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
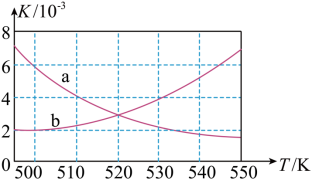
(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为___________ (填曲线标记字母),其判断理由是___________ 。
(3)在一定温度下,向2.0L固定容积的密闭容器中充入2mol H2和1mol CO,经过一段时间后,反应4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
①0~20min的平均反应速率v(CO)=___________ mol·L−1·min−1。
②达到平衡时,H2的转化率为___________ 。
③能表明该反应达到平衡状态的是___________ (填字母)。
A.容器中二甲醚的浓度不变 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
800℃时,H2还原CO2反应的热化学方程式及其平衡常数如下:
ⅰ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104
CO(g)+H2O(g) ΔH1=+41kJ·mol-1 K1=104ⅱ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3
CH3OH(g)+H2O(g) ΔH2=-49.5kJ·mol-1 K2=10-3(1)反应CO(g)+2H2(g)
 CH3OH(g) ΔH3=
CH3OH(g) ΔH3=Ⅱ.为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为

(3)在一定温度下,向2.0L固定容积的密闭容器中充入2mol H2和1mol CO,经过一段时间后,反应4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表:| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | — |
| n(CO)/mol | 1.0 | — | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | — | — | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
②达到平衡时,H2的转化率为
③能表明该反应达到平衡状态的是
A.容器中二甲醚的浓度不变 B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变 D.混合气体的密度不变
您最近一年使用:0次



