1 . As(0)、As(Ⅲ)和As(V)分别表示砷单质、三价砷和五价砷的化合物。硫酸厂产生的酸性废水中含有超标的H3AsO3,需处理达标后才能排放。目前含砷废水的处理常用石灰中和-PFS、氧化吸附、纳米级零价铁等方法。
(1)石灰中和-PFS法,处理过程如下:
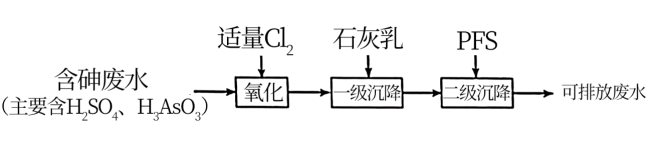
含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。
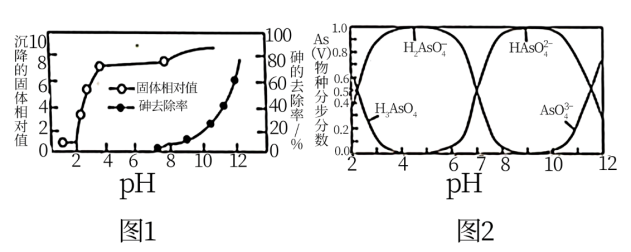
①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为___________ 。pH调节到8时,开始产生Ca3(AsO4)2沉淀,原因是___________ 。
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为___________ 。
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。
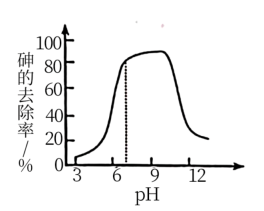
①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为___________ 。
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是___________ 。
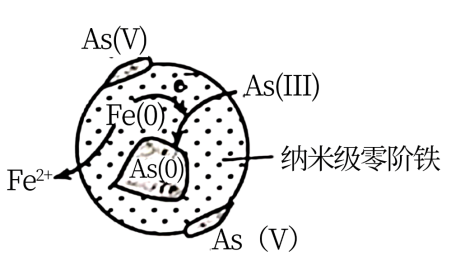
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:___________ 。
(1)石灰中和-PFS法,处理过程如下:

含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。

①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。

①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:

您最近一年使用:0次
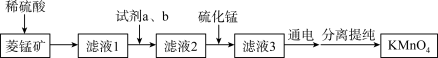
2 . 用菱锰矿(MnCO3)(含铁、铝、铜、硅的氧化物等杂质)为原料制取KMnO4,其工业生产流程示意图如下:
已知:①Ksp(MnS)>>Ksp(CuS);②KMnO4受热易分解。
回答下列问题:
(1)为提高矿石浸出率,可采取的措施有_______ (写2种)。
(2)向滤液1中依次加入试剂a、b后,过滤,除去溶液中的铁、铝杂质,试剂a、b分别是_______ 、_______ (各举一例,写名称),检验溶液中含铁元素的离子被除净的操作是_______ 。
(3)向滤液2中加入硫化锰(MnS)固体除去溶液中的Cu2+,写出发生反应的离子方程式_______ 。
(4)向滤液3中加入K2SO4后通电,写出电解时阳极的电极反应式_______ 。
(5)从电解后的溶液得到KMnO4晶体的方法是_______ (按实验先后顺序选填字母)。
A.过滤 B.蒸发至干 C.冷却 D.减压蒸发、浓缩
(6)经测定,制得产品含锰为37%,通过计算分析产品所含杂质可能是_______ (填化学式)。

已知:①Ksp(MnS)>>Ksp(CuS);②KMnO4受热易分解。
回答下列问题:
(1)为提高矿石浸出率,可采取的措施有
(2)向滤液1中依次加入试剂a、b后,过滤,除去溶液中的铁、铝杂质,试剂a、b分别是
(3)向滤液2中加入硫化锰(MnS)固体除去溶液中的Cu2+,写出发生反应的离子方程式
(4)向滤液3中加入K2SO4后通电,写出电解时阳极的电极反应式
(5)从电解后的溶液得到KMnO4晶体的方法是
A.过滤 B.蒸发至干 C.冷却 D.减压蒸发、浓缩
(6)经测定,制得产品含锰为37%,通过计算分析产品所含杂质可能是
您最近一年使用:0次



