解题方法
1 . 下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向盛有2mL0.l mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1 mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
B | 向淀粉溶液中加入适量的20%H2SO4溶液,加热,冷却后加入NaOH溶液至碱性,加入少量碘水 | 溶液未变蓝 | 淀粉已完全水解 |
C | 加热2NO2(g) N2O4(g)平衡体系 N2O4(g)平衡体系 | 颜色加深 | 证明正反应是放热反应 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-05更新
|
403次组卷
|
2卷引用:辽宁省新高考2021届高三上学期第三次调研化学试题
解题方法
2 . 废旧铅蓄电池拆解获得铅膏(主要由PbSO4、PbO2、PbO形成的悬浊液),对其回收利用可减少环境污染。流程如下:

(1)“还原”步骤为了加快速率可采取的一项措施是_________________ 。该步骤PbO2发生反应的化学方程式为_________________ 。
(2)已知25℃ ,
, ,
,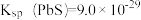 ,“脱硫”步骤选择最合适的试剂为
,“脱硫”步骤选择最合适的试剂为_________________ 。
a.(NH4)2CO3b.(NH4)2S c.NH4NO3
利用选出的脱硫试剂写出“脱硫”步骤的离子方程式________________ ;指出该步骤获得滤液的一种农业生产上的用途________________ 。
(3)“酸浸”步骤HBF4是一种强酸,试解释其酸性强于HF的原因________________ ,该步骤PbO发生反应的离子方程式为________________ 。
(4)电解时,酸度不宜过大的原因是________________ ;若电解时阳极有微量PbO2生成,写出生成PbO2的电极反应式________________ 。

(1)“还原”步骤为了加快速率可采取的一项措施是
(2)已知25℃
 ,
, ,
,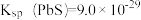 ,“脱硫”步骤选择最合适的试剂为
,“脱硫”步骤选择最合适的试剂为a.(NH4)2CO3b.(NH4)2S c.NH4NO3
利用选出的脱硫试剂写出“脱硫”步骤的离子方程式
(3)“酸浸”步骤HBF4是一种强酸,试解释其酸性强于HF的原因
(4)电解时,酸度不宜过大的原因是
您最近一年使用:0次



