1 . 海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
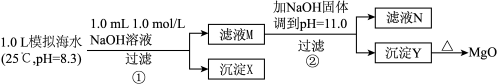
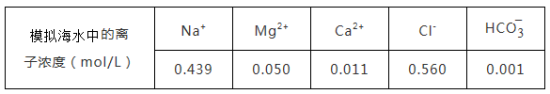
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
Ksp(CaCO3)=4.96×10-9Ksp(MgCO3)=6.82×10-6
Ksp[Ca(OH)2]=4.68×10-6Ksp[Mg(OH)2]=5.61×10-12
下列说法正确的是


注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
Ksp(CaCO3)=4.96×10-9Ksp(MgCO3)=6.82×10-6
Ksp[Ca(OH)2]=4.68×10-6Ksp[Mg(OH)2]=5.61×10-12
下列说法正确的是
| A.沉淀物X为CaCO3 |
| B.溶液M中存在Mg2+、不存在Ca2+ |
| C.溶液N中存在Mg2+、Ca2+ |
| D.步骤②中若改为加入4.2g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物 |
您最近半年使用:0次



