20-21高二上·浙江绍兴·阶段练习
1 . I.用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题
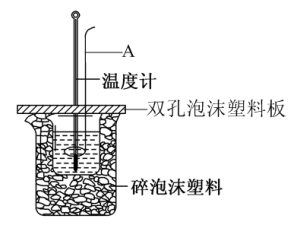
(1)图中仪器A的名称___________
(2)碎泡沫塑料的作用是___________ ,用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会___________ 57.3kJ/mol(填“大于”、“小于”或“等于”)。
(3)取50mL 0.50mol·L-1NaOH溶液和50mL 0.50mol/L硫酸溶液进行中和测定实验,实验数据如下表:
①近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则中和热ΔH=___________ 。(取小数点后一位)
②上述实验数值结果与57.3kJ·mol-1有偏差,产生偏差的原因可能是___________ (填字母)。
a. 实验装置保温、隔热效果差
b. 量取NaOH溶液的体积时仰视读数
c. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d. 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
II.(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a. C(s)+O2(g)=CO2(g) ΔH=E1①
b. C(s)+H2O(g)=CO(g)+H2(g) ΔH=E2②
请表达E1、E2、E3、E4之间的关系为E2=___________ 。
(2)如图所示,在常温常压下,1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________ 。

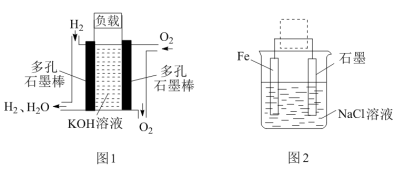
(3)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点,图1为氢氧燃料电池的结构示意图,试回答下列问题:
①写出该氢氧燃料电池工作时负极的反应式___________ 。
②用图1作为电源连接图2装置,铁电极与图1通氧气的电极相连进行电解,写出电解池的化学方程式:___________ 。
③钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图2(Fe与石墨用导线相连)所示:写出该电池反应的总反应方程式:___________ 。

(1)图中仪器A的名称
(2)碎泡沫塑料的作用是
(3)取50mL 0.50mol·L-1NaOH溶液和50mL 0.50mol/L硫酸溶液进行中和测定实验,实验数据如下表:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.6 |
| 2 | 27.0 | 27.4 | 27.2 | 30.8 |
| 3 | 25.9 | 25.9 | 25.9 | 29.3 |
| 4 | 26.4 | 26.2 | 26.3 | 31.4 |
①近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则中和热ΔH=
②上述实验数值结果与57.3kJ·mol-1有偏差,产生偏差的原因可能是
a. 实验装置保温、隔热效果差
b. 量取NaOH溶液的体积时仰视读数
c. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d. 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
II.(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a. C(s)+O2(g)=CO2(g) ΔH=E1①
b. C(s)+H2O(g)=CO(g)+H2(g) ΔH=E2②
H2(g)+ O2(g)=H2O(g) ΔH=E3③
O2(g)=H2O(g) ΔH=E3③
CO(g)+ O2(g)=CO2(g) ΔH=E4④
O2(g)=CO2(g) ΔH=E4④
请表达E1、E2、E3、E4之间的关系为E2=
(2)如图所示,在常温常压下,1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(3)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点,图1为氢氧燃料电池的结构示意图,试回答下列问题:
①写出该氢氧燃料电池工作时负极的反应式
②用图1作为电源连接图2装置,铁电极与图1通氧气的电极相连进行电解,写出电解池的化学方程式:
③钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图2(Fe与石墨用导线相连)所示:写出该电池反应的总反应方程式:

您最近一年使用:0次
名校
2 . 为研究金属腐蚀的条件呢和速率,某课外小组学生用铜丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一周后,下列对实验结束时现象描述不正确的是
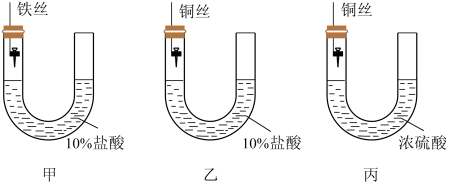

| A.装置Ⅰ左侧的液面一定会下降 |
| B.左侧液面装置Ⅰ比装置Ⅱ的低 |
| C.装置Ⅱ中的铁钉腐蚀最严重 |
| D.装置Ⅲ中的铁钉几乎没被腐蚀 |
您最近一年使用:0次
2019-11-09更新
|
229次组卷
|
18卷引用:浙江省诸暨中学2019-2020学年高二上学期10月阶段性考试化学试题
浙江省诸暨中学2019-2020学年高二上学期10月阶段性考试化学试题(已下线)2011-2012学年浙江省东阳市南马高中高三下学期期中考试化学试卷(已下线)2012届湖北省武穴中学高三上学期11月份月考化学试卷(已下线)2011-2012学年陕西省西安一中高一下学期期末考试化学试卷(已下线)2012年苏教版高中化学选修6 5.1原电池练习卷(已下线)2013-2014学年贵州省重点高中高二上学期期中考试文科化学试卷(已下线)2014年高二化学人教版选修一 3.2 金属的腐蚀和防护练习卷(已下线)同步君 选修4 第4章 第4节 金属的电化学腐蚀与防护山东省枣庄市第三中学2017-2018学年高二10月质量检测化学试题山东省济南市第一中学2017-2018学年高二10月阶段测试化学试题高中化学人教版 选修四 第四章 电化学基础 第四节 金属的电化学腐蚀与防护 金属的电化学腐蚀与防护(已下线)【新东方】高中化学164(已下线)2019年12月11日《每日一题》化学人教版(选修4)—— 影响钢铁腐蚀的因素鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第4节 金属的腐蚀与防护(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第三节 金属的腐蚀与防护 方法帮江西省景德镇市浮梁一中2020-2021学年高二下学期4月月考化学试题四川省成都市第七中学2022-2023学年高二下学期3月月考化学试题



