解题方法
1 . 锌铜原电池(如图所示)工作时,下列叙述正确的是
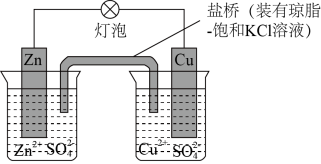

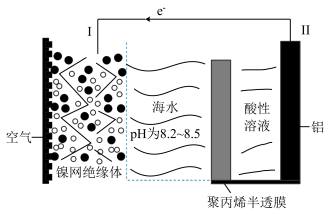
A.电池总反应为 | B.该电池中电子由正极流向负极 |
C.正极反应为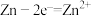 | D.盐桥中的 移向 移向 溶液 溶液 |
您最近一年使用:0次
解题方法
2 . 图为锌铜原电池装置,下列有关描述正确的是

| A.铜片和锌片不能互换位置 | B.缺少电流表,则不能产生电流 |
C.盐桥可用吸有 溶液的滤纸条代替 溶液的滤纸条代替 | D.Zn发生氧化反应,Cu发生还原反应 |
您最近一年使用:0次
解题方法
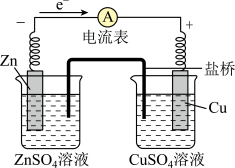
3 . 中国科学家研究出对环境污染小、便于铝回收的海水电池,其工作原理示意图如图:
下列说法正确的是( )

下列说法正确的是( )
A.电极I为负极,电极反应为 |
| B.聚丙烯半透膜允许阳离子从右往左通过 |
| C.如果电极Ⅱ为活性镁铝合金,则负极区会逸出大量气体 |
| D.当负极质量减少5.4g时,正极消耗336L气体 |
您最近一年使用:0次
解题方法
4 . 锂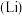 -空气电池的工作原理如图所示。下列说法不正确的是( )
-空气电池的工作原理如图所示。下列说法不正确的是( )
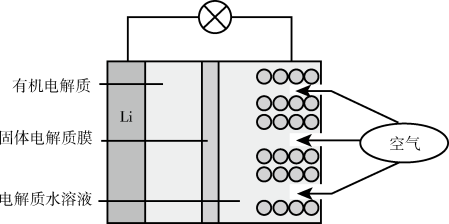
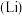 -空气电池的工作原理如图所示。下列说法不正确的是( )
-空气电池的工作原理如图所示。下列说法不正确的是( )
| A.金属锂做负极,发生氧化反应 |
B. 通过有机电解质向水溶液处移动 通过有机电解质向水溶液处移动 |
C.正极的电极反应: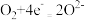 |
D.电池总反应: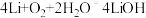 |
您最近一年使用:0次
名校
解题方法
5 . 一种新型微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示。下列说法正确的是( )
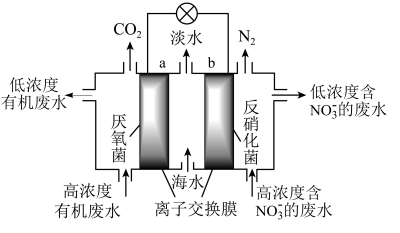

| A.a极为电池的正极 |
B.海水淡化的原理是电池工作时, 移向右室 移向右室 |
C.处理 的电极反应为 的电极反应为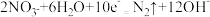 |
D.若用 表示有机废水中的有机物,则每消耗 表示有机废水中的有机物,则每消耗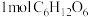 转移 转移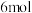 电子 电子 |
您最近一年使用:0次
2020-09-19更新
|
209次组卷
|
2卷引用:鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池
9-10高一下·山东聊城·期末
解题方法
6 . 已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液: 溶液、
溶液、 溶液、稀硫酸。按要求回答下列问题:
溶液、稀硫酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因:________________ 。
(2)若电极材料选铜和石墨,电解质溶液选 溶液,外加导线,能否构成原电池?
溶液,外加导线,能否构成原电池?______ 。若能,请写出电极反应式,负极:__________________ ,正极:_________________ (若不能,后两空不填)。
(3)设计一种以铁和稀硫酸反应为原理的原电池,在下面的方框中画出装置图__________ (需标明电极材料及电池的正负极)。

 溶液、
溶液、 溶液、稀硫酸。按要求回答下列问题:
溶液、稀硫酸。按要求回答下列问题:(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因:
(2)若电极材料选铜和石墨,电解质溶液选
 溶液,外加导线,能否构成原电池?
溶液,外加导线,能否构成原电池?(3)设计一种以铁和稀硫酸反应为原理的原电池,在下面的方框中画出装置图

您最近一年使用:0次
2020-09-19更新
|
308次组卷
|
4卷引用:鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池
鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 方法帮(已下线)2010年山东省聊城二中高一第二学期期末考试化学试题(已下线)2012-2013学年甘肃省武威市第六中学高一下学期期中测试化学试卷
解题方法
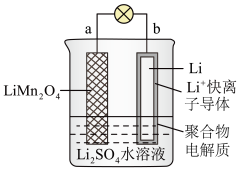
7 . 如图所示为水溶液锂离子电池体系。放电时,电池的负极是_____ (填“a”或“b”),溶液中的 从
从____ (填“a向b”或“b向a”)迁移。
 从
从
您最近一年使用:0次
名校
解题方法
8 . 由锌片、铜片和 稀硫酸组成的原电池如图所示。
稀硫酸组成的原电池如图所示。
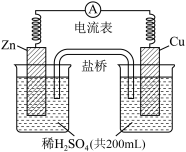
(1)原电池的负极反应式为_______ ,正极反应式为_________ 。
(2)电流的方向是_____ 。
(3)一段时间后,当在铜片上放出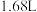 (标准状况)气体时,
(标准状况)气体时, 恰好消耗一半。则产生这些气体的同时,共消耗
恰好消耗一半。则产生这些气体的同时,共消耗____ g锌,有_____ 个电子通过了导线,原稀硫酸的物质的量浓度是______ (设 为阿伏加 德罗常数的值,溶液体积不变)。
为阿伏加 德罗常数的值,溶液体积不变)。
 稀硫酸组成的原电池如图所示。
稀硫酸组成的原电池如图所示。
(1)原电池的负极反应式为
(2)电流的方向是
(3)一段时间后,当在铜片上放出
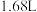 (标准状况)气体时,
(标准状况)气体时, 恰好消耗一半。则产生这些气体的同时,共消耗
恰好消耗一半。则产生这些气体的同时,共消耗 为阿伏加 德罗常数的值,溶液体积不变)。
为阿伏加 德罗常数的值,溶液体积不变)。
您最近一年使用:0次
2020-09-12更新
|
252次组卷
|
5卷引用:鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 综合训练
鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 综合训练高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 第一节综合训练(已下线)4.1.1 原电池的工作原理(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北阜城中学2020-2021学年高二上学期期中考试化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题
名校
解题方法
9 . 某原电池的总反应的离子方程式为:2Fe3++Fe=3Fe2+,能实现该反应的原电池组成是( )
| A.正极为铜,负极为铁,电解质溶液为NaCl溶液 |
| B.正极为碳,负极为铁,电解质溶液为Fe(NO3)3溶液 |
| C.正极为铁,负极为锌,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为银,负极为铁,电解质溶液为CuSO4溶液 |
您最近一年使用:0次
2020-08-30更新
|
192次组卷
|
3卷引用:第1课时 原电池的工作原理
19-20高二·全国·课时练习
解题方法
10 . 控制适合的条件,将反应2Fe3++2I-⇌2Fe2++I2设计成如图所示的原电池。

请回答下列问题:
(1)①反应开始时,乙中石墨电极上发生__ (填“氧化”或“还原”)反应,电极反应式为___ 。甲中石墨电极上发生___ (填“氧化”或“还原”)反应,电极反应式为__ 。
②电流表读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作__ (填“正”或“负”)极,该电极的电极反应式为___ 。
(2)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为___ 。

请回答下列问题:
(1)①反应开始时,乙中石墨电极上发生
②电流表读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(2)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
您最近一年使用:0次



