2023高三·全国·专题练习
名校
解题方法
1 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
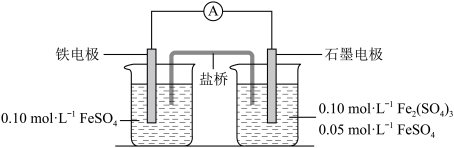
回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为___________________ ,铁电极的电极反应式为_______________________________ 。因此,验证了Fe2+氧化性小于________ 、还原性小于________ 。

回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
22-23高一下·河南·阶段练习
名校
解题方法
2 . 在海洋岛礁上安装“空气―Mg”金属燃料电池可为水上照明信标供电,其原理如图所示。下列说法中不正确的是
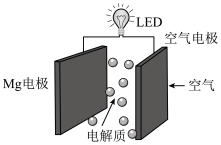
A.电池工作时,海水中的 向空气电极移动 向空气电极移动 |
B.0.5mol 参与反应,2mol电子流入Mg电极 参与反应,2mol电子流入Mg电极 |
| C.Mg电极上发生氧化反应,该电极需定期更换 |
D.理论上参与反应的Mg与 的物质的量之比为2∶1 的物质的量之比为2∶1 |
您最近一年使用:0次
2023-06-24更新
|
277次组卷
|
3卷引用:单项选择题
22-23高一下·山东泰安·期中
3 . 物质都是由微观粒子构成的,这些粒子的结合重组,是构成物质及其物质变化和能量变化的根本原因。
(1)6Li、14C、14N、7Li、23Na、16O这些微粒中,共有_______ 种核素,互为同位素的是_______ 。
(2)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是_______ (填序号),仅离子键被破坏的是_______ (填序号)。
(3)若将反应2Fe3++Cu=2Fe2++Cu2+设计成原电池装置,则负极材料为_______ ,离子导体为_______ ,正极电极反应式是_______ ;若反应过程中有0.2mol电子通过,则电解质溶液的质量变化为_______ 。
(4)从能量的变化角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
则生成1molH2O(g)可以放出热量_______ kJ。
(1)6Li、14C、14N、7Li、23Na、16O这些微粒中,共有
(2)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是
(3)若将反应2Fe3++Cu=2Fe2++Cu2+设计成原电池装置,则负极材料为
(4)从能量的变化角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
| 化学键 | H—H | O=O | H—O |
| 能量(kJ) | 436 | 496 | 463 |
您最近一年使用:0次
22-23高一下·四川成都·期中
解题方法
4 . 化学电源在生产生活中有着广泛的应用,请回答下列问颕:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_____ (填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如图两个对比实验(除图Ⅱ中增加导线和铜片外,其余条件完全相同)。经过相同时间后,温度计示数:图I_____ 图Ⅱ(填“高于”、“等于”或“低于”),产生气体的速率:图I_____ 图Ⅱ(填“大于”、“等于”或“小于”)。
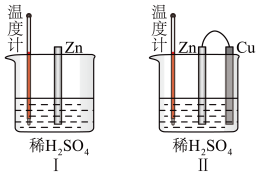
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是_____ (填化学式),电解质溶液是_____ (填化学式)溶液。
②正极上发生的电极反应为_____ 。
③若导线上转移的电子为1mol,则消耗的金属铜的质量为_____ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是
| A.Ba(OH)2+2NH4Cl=BaCl2+2NH3↑+2H2O | B.Cu+Ag+=Ag+Cu2+ |
| C.Zn+H2SO4=ZnSO4+H2↑ | D.CaO+H2O=Ca(OH)2 |

(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是
②正极上发生的电极反应为
③若导线上转移的电子为1mol,则消耗的金属铜的质量为
您最近一年使用:0次
22-23高二下·安徽·开学考试
解题方法
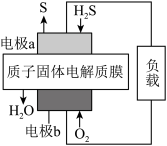
5 . 如图,利用反应 处理工业废气
处理工业废气 并回收单质硫。下列说法错误的是
并回收单质硫。下列说法错误的是
 处理工业废气
处理工业废气 并回收单质硫。下列说法错误的是
并回收单质硫。下列说法错误的是
| A.电极b为电池的正极 |
B. 由a电极经质子膜移向b极区 由a电极经质子膜移向b极区 |
C.电极a上的电极反应式为 |
D. 反应,则电池内部释放 反应,则电池内部释放 热能 热能 |
您最近一年使用:0次
22-23高一下·江苏扬州·开学考试
名校
解题方法
6 . 某Al- 电池原理如图所示,电池总反应为
电池原理如图所示,电池总反应为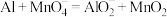 ,下列说法正确的是
,下列说法正确的是
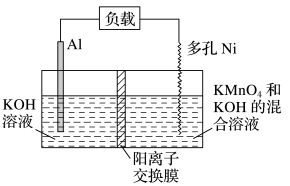
 电池原理如图所示,电池总反应为
电池原理如图所示,电池总反应为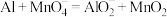 ,下列说法正确的是
,下列说法正确的是
| A.多孔Ni电极作负极 |
| B.Al电极发生还原反应 |
C.正极的电极反应式为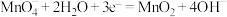 |
| D.电池工作时,K+向正极区移动 |
您最近一年使用:0次
2023-02-03更新
|
603次组卷
|
4卷引用:2019年高考海南卷化学试题变式题(不定项选择题)
(已下线)2019年高考海南卷化学试题变式题(不定项选择题)江苏省扬州中学2022-2023学年高一下学期开学摸底考试化学试题江西省大余中学2022-2023学年高一下学期4月期中化学试题(已下线)第六章 化学反应与能量 单元测试
22-23高二上·甘肃武威·开学考试
名校
7 . N2H4−空气燃料电池是一种环保型碱性燃料电池,电解质溶液为30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O。该电池工作时,下列说法正确的是
A.正极反应式为 |
| B.溶液中的阴离子向正极移动 |
C.负极反应式为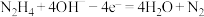 |
| D.溶液的pH保持不变 |
您最近一年使用:0次
21-22高一下·福建福州·期末
解题方法
8 . 潜艇中使用的液氨一液氧燃料电池工作原理如图所示,电池工作时,下列说法正确的是


| A.电子由电极a流向电极b,经过溶液回到电极a |
B.溶液中的 向电极a移动 向电极a移动 |
| C.转移电子0.4mol,参加反应的氧气体积是2.24L |
D.电极a的电极反应式为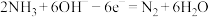 |
您最近一年使用:0次
21-22高一下·吉林长春·期中
名校
9 .  电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的总反应为
电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的总反应为 。下列说法正确的是
。下列说法正确的是

 电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的总反应为
电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的总反应为 。下列说法正确的是
。下列说法正确的是
A. 为电池的正极 为电池的正极 |
B.正极的电极反应式为 |
C.电池工作时, 向正极移动 向正极移动 |
D.将熔融的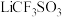 改为 改为 的水溶液,电池性能更好 的水溶液,电池性能更好 |
您最近一年使用:0次
21-22高一下·山东德州·期中
名校
解题方法
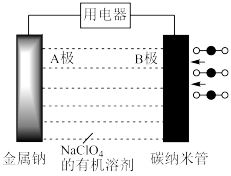
10 . 火星大气中 占96%,钠—
占96%,钠— 电池在火星探测中具有广泛的应用前景。电池总反应为
电池在火星探测中具有广泛的应用前景。电池总反应为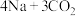
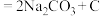 ,装置如图所示,下列说法正确的是
,装置如图所示,下列说法正确的是
 占96%,钠—
占96%,钠— 电池在火星探测中具有广泛的应用前景。电池总反应为
电池在火星探测中具有广泛的应用前景。电池总反应为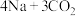
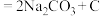 ,装置如图所示,下列说法正确的是
,装置如图所示,下列说法正确的是
| A.该电池中的金属钠可用金属锂或钾代替 |
| B.图中有机溶剂可以用水代替 |
C.电子移动方向:A极→用电器→B极→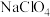 的有机溶剂→A极 的有机溶剂→A极 |
D.若有标准状况下67.2L 参与反应,电路中转移的电子数为4 参与反应,电路中转移的电子数为4 |
您最近一年使用:0次
2022-05-10更新
|
271次组卷
|
3卷引用:2019年高考海南卷化学试题变式题(不定项选择题)



