名校
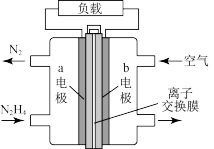
1 . 一种以液态肼( )为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
 )为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
| A.b极发生氧化反应 |
B.a极的电极反应为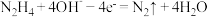 |
| C.放电时,电流从a极经过负载流向b极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
您最近一年使用:0次
2 . 一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其负极反应式为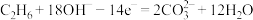 ,正极反应式为
,正极反应式为 ,有关此电池的推断正确的是
,有关此电池的推断正确的是
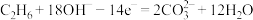 ,正极反应式为
,正极反应式为 ,有关此电池的推断正确的是
,有关此电池的推断正确的是A.当转移0.4mol电子时,消耗 的体积为2.24L 的体积为2.24L |
B.参加反应的氧气与 的物质的量之比为7∶2 的物质的量之比为7∶2 |
| C.放电一段时间后,KOH的物质的量浓度不变 |
| D.电解质溶液中OH-向负极移动 |
您最近一年使用:0次
2022-07-15更新
|
290次组卷
|
3卷引用:河北省邯郸市2021-2022学年高一下学期期末考试化学试题
名校
3 . 一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电池放电时的说法错误的是
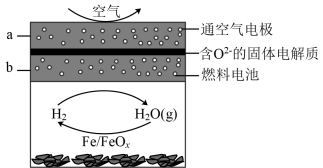

| A.a电极上发生氧化反应 |
B.负极的电极反应式为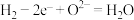 |
C.铁表面发生的反应为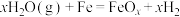 |
| D.若标准状况下33.6L空气参与反应,电路中理论上有6mol电子转移 |
您最近一年使用:0次
2022-07-14更新
|
441次组卷
|
3卷引用:山东省菏泽市2021-2022学年高一下学期期末教学质量检测化学试题
解题方法
4 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是
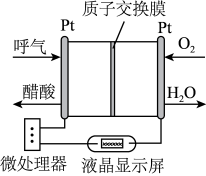

| A.电流由O2所在的铂电极经外电路流向另一电极 |
| B.O2所在的铂电极处发生氧化反应 |
C.该电池的负极反应式为 |
| D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
您最近一年使用:0次
名校
解题方法
5 . 利用氢气燃料电池电解CuSO4溶液、MgCl2溶液,装置如图所示:
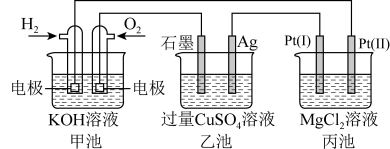
下列说法错误的是

下列说法错误的是
| A.甲池是将化学能转化为电能的装置,乙、丙池是将电能转化为化学能的装置 |
| B.反应一段时间后,向乙池中加入一定量CuO能使CuSO4溶液恢复到原浓度 |
| C.丙池的Pt(II)电极发生的电极反应为2Cl--2e-=Cl2↑ |
| D.甲池中消耗280mLO2,此时丙池中理论上最多产生1.45g固体 |
您最近一年使用:0次
2022-07-11更新
|
277次组卷
|
2卷引用:河北省承德市2021-2022学年高一下学期期末考试化学试题
6 . 新一代电池体系是化学、物理等学科的基础理论研究与应用技术的前沿。锂硒电池具有优异的循环稳定性。下列有关说法不正确的是
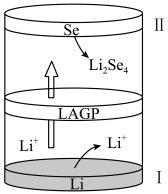

| A.电极I为该电池的负极,被还原 |
B.电极材料 可由 可由 通入亚硒酸( 通入亚硒酸( )溶液中反应制得,则该反应中氧化剂与还原剂的物质的量之比为1∶2 )溶液中反应制得,则该反应中氧化剂与还原剂的物质的量之比为1∶2 |
C.锂硒电池放电时正极的电极反应式为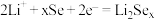 |
| D.该电池放电时,电子由电极I经电解质溶液通过LAGP隔膜流向电极II |
您最近一年使用:0次
解题方法
7 . 某CH4燃料电池以固体氧化物作为电解质,总反应为CH4+2O2=CO2+2H2O,工作原理示意图如图所示。下列说法错误的是
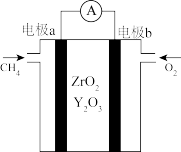

| A.电池工作过程中化学能转化为电能 |
| B.电极b为负极,发生还原反应 |
| C.电流从电极a经导线流向电极b |
| D.燃料电池具有安全、高效等特点 |
您最近一年使用:0次
8 . 下列实验操作能达到目的的是
| 选项 | 操作 | 目的 |
| A | 向混合物中加入足量NaOH溶液,充分反应后过滤、洗涤、干燥 | 除去Fe2O3中的Al2O3杂质 |
| B | 测定相同浓度的HCl溶液、HBr溶液的pH | 比较Cl和Br的非金属性强弱 |
| C | 将相同大小的镁片和铝片用导线连接,插入NaOH溶液中 | 证明原电池中活泼性较强的金属作负极 |
| D | 向蔗糖溶液中加入新制的银氨溶液,水浴加热 | 证明蔗糖是非还原性糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 2018年5月,美国研究人员成功实现在常温常压下用氮气和水生产氨,其原理如图所示。下列说法不正确的是
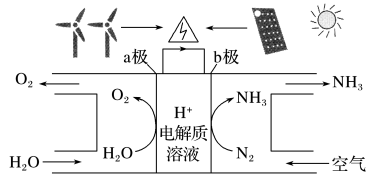

| A.图中能量转化的方式有2种 |
| B.b极的发生的电极反应方程式为:N2+6e-+6H+=2NH3 |
| C.H+向b极区移动 |
| D.a极上每产生22.4LO2,流过电极的电子数为4NA |
您最近一年使用:0次
名校
解题方法
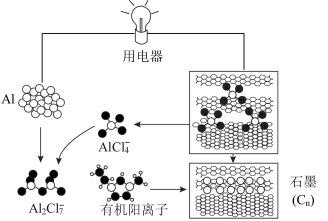
10 . 研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池。该电池分别以铝和石墨为电极,用AlCl 和有机阳离子构成的电解质溶液作为离子导体,其放电工作原理如图所示。下列说法中,不正确的是
和有机阳离子构成的电解质溶液作为离子导体,其放电工作原理如图所示。下列说法中,不正确的是
 和有机阳离子构成的电解质溶液作为离子导体,其放电工作原理如图所示。下列说法中,不正确的是
和有机阳离子构成的电解质溶液作为离子导体,其放电工作原理如图所示。下列说法中,不正确的是
| A.放电时,铝为负极,石墨为正极 |
| B.放电时,有机阳离子向铝电极方向移动 |
C.放电时的负极反应为:Al+7AlCl -3e-=4Al2Cl -3e-=4Al2Cl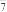 |
D.充电时的阳极反应为:Cn+AlCl +e-=CnAlCl4 +e-=CnAlCl4 |
您最近一年使用:0次
2022-06-10更新
|
349次组卷
|
2卷引用:山东省泰安市泰安一中2021-2022学年高一下学期6月学情诊断化学试题



