名校
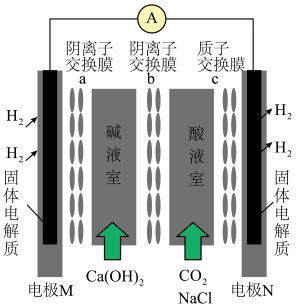
1 . 某种浓差电池的装置如图所示,碱液室中加入电石渣浆液[主要成分为 ],酸液室通入
],酸液室通入 (以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述正确的是 ( )
(以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述正确的是 ( )
 ],酸液室通入
],酸液室通入 (以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述正确的是 ( )
(以NaCl为支持电解质),产生电能的同时可生产纯碱等物质。下列叙述正确的是 ( )
| A.电子由N极经外电路流向M极 |
B.N电极区的电极反应式为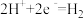 ↑ ↑ |
C.在碱液室可以生成 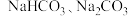 |
| D.放电一段时间后,酸液室溶液pH减小 |
您最近一年使用:0次
2019-06-03更新
|
709次组卷
|
4卷引用:甘肃省定西市陇西县第一中学2019届高三下学期适应性训练化学试题
名校
2 . 以氨作为燃料的燃料电池,具有能量效率高的特点,另外氨气含氢量高,易液化,方便运输和贮存,是很好的氢源载体。NH3-O2燃料电池的结构如图所示,下列说法正确的是
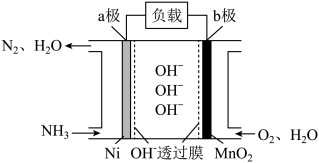

| A.a极为电池的正极 |
| B.负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O |
| C.当生成1 mol N2时,电路中通过的电子的物质的量为3 mol |
| D.外电路的电流方向为从a极流向b极 |
您最近一年使用:0次
2019-05-20更新
|
940次组卷
|
7卷引用:辽宁省营口市部分重点高中2017-2018学年高一下学期期末考试化学试题
3 . 一种新型的“电池的正极采用含有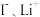 的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用
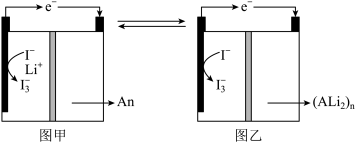
的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用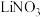 溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含
溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含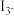 的溶液呈棕黄色,下列有关判断正确的是
的溶液呈棕黄色,下列有关判断正确的是
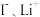 的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用
的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用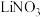 溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含
溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含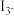 的溶液呈棕黄色,下列有关判断正确的是
的溶液呈棕黄色,下列有关判断正确的是
| A.图甲是原电池工作原理图,图乙是电池充电原理图 |
| B.放电时,正极液态电解质溶液的颜色变浅 |
C.放电时, 从右向左通过聚合物离子交换膜 从右向左通过聚合物离子交换膜 |
D.放电时,负极的电极反应式为: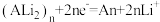 |
您最近一年使用:0次
名校
4 . a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b 相连时,电流由a经导线流向b,c、d相连时,电子由d到c;a、c相连时,a极上产生大量气泡,b、d相连时,H+移向d极,则四种金属的活动性顺序由强到弱的顺序为
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>d>c>a |
您最近一年使用:0次
2019-04-15更新
|
1669次组卷
|
20卷引用:辽宁省锦州市义县高级中学2020-2021学年高二12月月考化学试题
辽宁省锦州市义县高级中学2020-2021学年高二12月月考化学试题【全国百强校】江苏省海安高级中学2018-2019学年高一下学期3月月考化学试题2【市级联考】贵州省遵义市2018-2019学年高一下学期期中考试化学试题课时2 原电池的原理及应用——A学习区 夯实基础(鲁科版(2019)第二册)课时1 利用化学反应制备物质——A学习区 夯实基础(鲁科版必修2)山东省潍坊市五县市2019-2020学年高一下学期期中考试化学试题河南省平顶山市鲁山县第一高级中学2019-2020学年高一6月月考化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第二节 化学反应与能量转化 方法帮山西省朔州市怀仁县大地学校2019-2020学年高一下学期期末考试化学试题湖南省长沙县第九中学2019-2020学年高一上学期第一次月考化学试题安徽省蚌埠田家炳中学2020-2021学年高二12月月考化学试题山东省临朐县实验中学2020-2021学年高一下学期4月月考化学试题重庆市第七中学校2020-2021学年高一下学期半期考试化学试题重庆市四川外语学院重庆第二外国语学校2021-2022学年高一下学期期中考试化学试题广西钦州市第一中学2021-2022学年高二下学期期中考试理科综合化学试题北京市第五中学2021-2022学年高一下学期期中考试化学试题第一节 原电池 第1课时 原电池的工作原理四川省凉山州西昌市2021-2022学年高一下学期期中考试化学试题山东省文登第一中学2022-2023学年高二上学期1月期末考试化学试题四川省宜宾市叙州区第一中学校2022-2023学年高一下学期4月月考化学试题
名校
5 . 下图为利用电化学方法处理有机废水的原理示意图。下列说法正确的是


| A.a、b极不能使用同种电极材料 |
| B.工作时,a极的电势低于b极的电势 |
| C.工作一段时间之后,a极区溶液的pH减小 |
D.b极的电极反应式为:CH3 COO-+4H2O-8e-=2HCO +9H+ +9H+ |
您最近一年使用:0次
2019-04-03更新
|
2513次组卷
|
6卷引用:【全国百强校】辽宁省沈阳市东北育才学校2018-2019学年高一下学期期中考试化学试题
6 . 据报导,我国已研制出“可充室温钠—二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠四甘醇二甲醚,电池总反应为:4Na+3CO2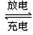 2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
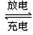 2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是| A.放电时钠金属片发生氧化反应 |
| B.放电时吸收CO2,充电时释放CO2 |
| C.放电时Na+向碳纳米管移动 |
| D.放电时的负极反应为2Na-2e-+CO32-=Na2CO3 |
您最近一年使用:0次
2019-03-28更新
|
883次组卷
|
4卷引用:【市级联考】辽宁省葫芦岛市普通高中2019届高三下学期第一次模拟考试理综合化学试题
7 . 一种检测空气中甲醛(HCHO)含量的电化学传感器的工作原理如图所示。下列说法正确的是

| A.传感器工作时,工作电极电势高 |
| B.工作时,H+通过交换膜向工作电极附近移动 |
| C.当导线中通过2×l0﹣6 mol电子,进入传感器的甲醛为3×10﹣3 mg |
| D.工作时,对电极区电解质溶液的pH增大 |
您最近一年使用:0次
2019-03-18更新
|
717次组卷
|
3卷引用:【全国百强校】辽宁省沈阳市东北育才学校2018-2019学年高一下学期期中考试化学试题
名校
8 . 我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置进行脱硫,将硫化氢气体转化成硫沉淀。已知甲、乙池中发生的反应为(右图):下列说法正确的是
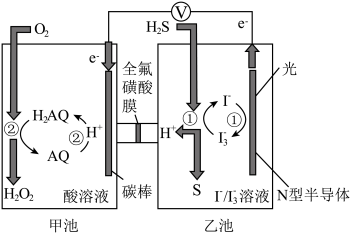

| A.甲池中得到H2O2的反应,H2O2既是氧化产物也是还原产物 |
| B.电路中每转移0.2mol电子,甲池溶液质量变化3.4g,乙池溶液质量保持不变 |
| C.光照时乙池电极上发生的反应为:H2S+I3-=3I-+S+2H+ |
| D.甲池中炭棒上发生的电极反应为:AQ+2H+-2e-=H2AQ |
您最近一年使用:0次
2019-02-21更新
|
849次组卷
|
9卷引用:【校级联考】江西省临川一中,南昌二中,九江一中,新余一中等九校重点中学协作体2019届高三上学期第一次联考理科综合化学试题
【校级联考】江西省临川一中,南昌二中,九江一中,新余一中等九校重点中学协作体2019届高三上学期第一次联考理科综合化学试题陕西省西安中学2020届高三上学期第三次月考化学试题2020届高三化学化学二轮复习——高考常考题型:电极反应式的书写专练【精编29题】江西省丰城中学2019-2020学年高二下学期期末考试化学试题(创新班)(已下线)第04章 电化学基础(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)江西省赣州市部分重点中学2021届高三上学期期中考试化学试题四川省成都实验中学2021届高三上学期11月月考理综化学试题辽宁省沈阳市第二中学2021-2022学年高一下学期期中考试化学试题2020高考化学二轮总复习高分必备 题型专题1 选择题专练
名校
9 . 锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质 LiClO4溶于混合有机溶剂中,Li+通过电解质的有机溶液迁移入 MnO2晶格中,生成 LiMnO2。下列说法正确的是


| A.外电路的电流方向是由 a 极流向 b 极。 |
| B.电池b 极反应式为 MnO2+e-+Li+=LiMnO2 |
| C.可用水代替电池中的混合有机溶剂 |
| D.a 极发生还原反应 |
您最近一年使用:0次
2019-02-14更新
|
223次组卷
|
3卷引用:辽宁省辽阳县集美学校2018-2019学年高二下学期开学考试化学试题
解题方法
10 . 铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是__________ (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计的原电池,请在图甲中的横线上完成标注________ 。
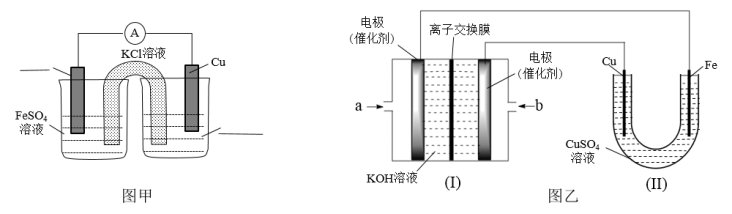
②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入____ (填“CH4”或“O2”),b处电极上发生的电极反应式为_________ ;
若把II中电极均换为惰性电极,电解液换为含有0.1 mol NaCl溶液400 mL,当阳极产生的气体为448 mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,______________ 直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计的原电池,请在图甲中的横线上完成标注

②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入
若把II中电极均换为惰性电极,电解液换为含有0.1 mol NaCl溶液400 mL,当阳极产生的气体为448 mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,
您最近一年使用:0次
2019-01-30更新
|
205次组卷
|
2卷引用:2015届辽宁省沈阳铁路实验中学高三下学期初考理综化学试卷



