名校
解题方法
1 . 关于如图所示的原电池,下列说法正确的是


| A.石墨电极上发生氧化反应 |
| B.电子由锌片通过导线流向石墨棒 |
| C.该装置将电能转化为化学能 |
| D.将稀硫酸换成乙醇,灯泡亮度不变 |
您最近一年使用:0次
2021-02-17更新
|
2141次组卷
|
7卷引用:(人教版2019)必修第二册 模块学业水平合格性测评
名校
解题方法
2 . 电能是现代社会应用最广泛的能源之一、
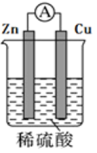
(1)某原电池装置如图所示。其中,Zn电极为原电池的___________ 极(填“正”或“负”)。
(2)Zn电极的电极反应式是___________ 。
(3)Cu电极上发生的反应属于___________ (填“氧化”或“还原”)反应。
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了___________ mol电子。
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2

(1)某原电池装置如图所示。其中,Zn电极为原电池的
(2)Zn电极的电极反应式是
(3)Cu电极上发生的反应属于
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2
您最近一年使用:0次
2021-05-07更新
|
1581次组卷
|
11卷引用:吉林省通化县综合高级中学2020-2021学年高一下学期期中考试化学试题
吉林省通化县综合高级中学2020-2021学年高一下学期期中考试化学试题吉林省松原市乾安七中2020-2021学年高一下学期第七次质量检测化学试题北京市西城区2018-2019学年高一第二学期期末考试化学试题北京市西城区高一化学下学期前三章综合阶段性试卷辽宁省葫芦岛市2019-2020学年高一下学期期末考试化学试题安徽省亳州市第二中学2021-2022学年高二上学期开学摸底考试化学试题甘肃省兰州市教育局第四片区2021-2022学年高一下学期期中考试化学试题江西省南昌县莲塘第一中学2021-2022学年高一下学期4月期中线上质量检测化学试题云南省昆明光华学校2021-2022学年高一3月月考化学试题广西钦州市第四中学2021-2022学年高一下学期4月份考试化学试题(已下线)考点09 电化学原理-2020年【衔接教材·暑假作业】新高三一轮复习化学
名校
3 . 硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是
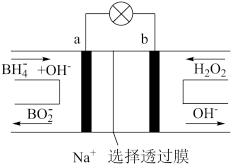

| A.电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+ |
| B.放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4 |
| C.电池放电时Na+从b极区移向a极区 |
| D.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
您最近一年使用:0次
2019-07-16更新
|
3272次组卷
|
11卷引用:人教版2019必修第二册 第六章 专题强化练2 电极反应式的书写及新型电源
人教版2019必修第二册 第六章 专题强化练2 电极反应式的书写及新型电源四川省内江市第六中学2020-2021学年高一下期期中考试化学试题江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题河南省信阳高级中学2021-2022学年高二上学期9月月考化学试题福建省福建师范大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第二册第六单元01讲核心广东省揭阳市2018-2019学年高二下学期期末考试理综化学试题广东省潮州市2019-2020学年高二下学期期末统考化学试题河南省驻马店市第二高级中学2019-2020学年高二下学期期末考试化学试题黑龙江省大庆铁人中学2020-2021学年高二上学期第一次月考化学试题海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(段考)化学科试题
名校
解题方法
4 . 一种 电池工作原理如装置图所示。下列说法正确的是
电池工作原理如装置图所示。下列说法正确的是

 电池工作原理如装置图所示。下列说法正确的是
电池工作原理如装置图所示。下列说法正确的是
| A.电池工作时电能转化为化学能 |
B.放电过程中电极 区溶液的 区溶液的 增大 增大 |
C.电池工作一段时间后 浓度增大 浓度增大 |
D. 极区的反应为 极区的反应为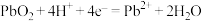 |
您最近一年使用:0次
2021-11-12更新
|
1387次组卷
|
8卷引用:江苏省南京师范大学苏州实验学校2021-2022学年高一上学期12月月考(日新班)化学试题
江苏省南京师范大学苏州实验学校2021-2022学年高一上学期12月月考(日新班)化学试题江苏省苏州市2021-2022学年高三上学期期中考试调研化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期期中调研考试化学试题辽宁省大连市金普新区省示范性高中联合体2021-2022学年高三上学期第二阶段考试化学试题湖北省黄冈市蕲春县第四高级中学2021-2022学年上学期高三11月月考化学试题(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练河北省衡水中学2023届高三上学期三调考试化学试题(已下线)专题一 原电池的工作原理及其应用
名校
解题方法
5 . 原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献。关于如图所示原电池的说法正确的是
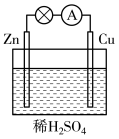

| A.将电能转化为化学能的装置 |
| B.电子由铜片经导线流向锌片 |
| C.锌片为负极,发生氧化反应 |
| D.铜片上发生的反应为Cu2++2e-=Cu |
您最近一年使用:0次
2022-03-03更新
|
674次组卷
|
5卷引用:云南省红河州开远市、弥勒市2020-2021学年高一下学期期末联考化学试题
名校
解题方法
6 . 锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应式是Li+MnO2=LiMnO2。下列说法正确的是
| A.Li是负极,电极反应为Li-e-=Li+ |
| B.Li是正极,电极反应为Li+e-=Li- |
C.MnO2是负极,电极反应为MnO2+e-=MnO |
| D.Li是负极,电极反应为Li-2e-=Li2+ |
您最近一年使用:0次
2023-03-17更新
|
716次组卷
|
11卷引用:河北省唐山市英才国际学校2020-2021学年高一下学期期中考试化学试题
河北省唐山市英才国际学校2020-2021学年高一下学期期中考试化学试题2020年人教版高中化学必修2第二章《化学反应与能量》测试卷2(已下线)专题05 化学能与电能(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)吉林省长春市实验中学2019-2020学年高一下学期期末考试化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二上学期期中联考化学试题河北省邢台市第二中学2019-2020学年高二上学期期中考试化学试题黑龙江省绥化市青冈县第一中学2020-2021学年高二上学期开学考试化学试题(已下线)专题五 锂电池和锂离子电池(练习)宁夏银川市唐徕中学2022-2023学年高二下学期3月月考化学试题(已下线)题型16 锂电池和锂离子电池的应用
名校
解题方法
7 . 某化学兴趣小组为了探究铝电极在原电池中的作用,在常温下,设计并进行了以下一系列实验,实验结果记录如下。
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)是否相同?__ (填“是”或“否”)。
(2)由实验3完成下列填空:
①铝为__ 极,电极反应式:__ 。
②石墨为__ 极,电极反应式:__ 。
③电池总反应式:__ 。
(3)实验4中铝作负极还是正极?__ ,理由是__ 。写出铝电极的电极反应式:__ 。
(4)解释实验5中电流表指针偏向铝的原因:__ 。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:__ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Al、Mg | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Al、Mg | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极(正极或负极)是否相同?
(2)由实验3完成下列填空:
①铝为
②石墨为
③电池总反应式:
(3)实验4中铝作负极还是正极?
(4)解释实验5中电流表指针偏向铝的原因:
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:
您最近一年使用:0次
2021-02-19更新
|
1287次组卷
|
8卷引用:(鲁科版2019)必修第二册 第2章 化学键 化学反应规律 第2节 化学反应与能量转化 第2课时 化学反应能量转化的重要应用——化学电池
名校
解题方法
8 . 十九大报告中提出要“打赢蓝天保卫战”,意味着对污染防治比过去要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下,当该装置工作时,下列说法正确的是


| A.盐桥中Cl-向Y极移动 |
| B.电路中流过7.5 mol电子时,共产生标准状况下N2的体积为16.8L |
| C.电流由X极沿导线流向Y极 |
| D.Y极发生的反应为2NO3-+10e-+6H2O=N2↑+12OH-,周围pH增大 |
您最近一年使用:0次
2021-08-05更新
|
1217次组卷
|
25卷引用:江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题
江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题(已下线)模块八 电化学基础(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆铁人中学2021-2022学年高二上学期开学考试化学试题(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)1.2.1 原电池的工作原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)江苏省华东师范大学盐城实验中学2021-2022学年高二上学期第一次月考化学试题 山东省烟台市福山区第一中学2021-2022学年高三上学期9月月考化学试题.湖北省荆门市2019—2020学年高三上学期元月调研考试理综化学试题2020届高三《新题速递·化学》1月第02期(考点07-10)【百强校】江西省南昌市第十中学2020届高三下学期综合模拟考试化学试题湖北省武汉市华中师大一附中高三理科四调综合训化学试题天津市七校联考2020届高三二模化学试卷福建省安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高二上学期期中联考化学试题(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-测试甘肃省天水市第一中学2021-2022学年高二下学期开学检测化学试题福建省漳州第一中学2021-2022学年高三下学期第五次阶段考化学试题(已下线)必刷卷03-2022年高考化学考前信息必刷卷(山东专用)湖南省株洲市醴陵市第一中学2021-2022学年高三下学期期中考试化学试题福建省福州市三校2022-2023学年高二上学期期中联考化学试题河南省信阳市普通高中2022-2023学年高三上学期第二次教学质量检测化学试题福建省福州第二中学2022-2023学年高二上学期期末考试化学试题河南省信阳高级中学2022-2023学年高二下学期开学考试化学试题江苏省苏州第一中学校2023-2024学年高二上学期10月月考化学试题
名校
解题方法
9 . 某原电池的结构如图所示,下列说法错误的是
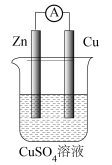

| A.Zn为该原电池的负极,发生氧化反应 |
| B.Cu电极上的反应为Cu2++2e-=Cu |
| C.电子由Zn电极流出,经过溶液流入Cu电极 |
| D.反应一段时间后,溶液的蓝色变浅 |
您最近一年使用:0次
2021-11-02更新
|
1122次组卷
|
6卷引用:河北省沧州市第一中学2020-2021学年高一下学期第一次检测化学试题
河北省沧州市第一中学2020-2021学年高一下学期第一次检测化学试题云南省弥勒市第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)专题4.1.1 原电池的工作原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)4.1 原电池-2021-2022学年高二化学课后培优练(人教版选修4)重庆第二十三中学校2021-2022学年高一下学期第一次月考化学试题湖南省祁东县育贤中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
10 . 如图为一原电池示意图,在原电池两极之间设有隔膜,Zn2+、SO 可以自由通过。则下列说法不正确的是
可以自由通过。则下列说法不正确的是

 可以自由通过。则下列说法不正确的是
可以自由通过。则下列说法不正确的是
| A.Zn2+通过隔膜从负极区向正极区移动 |
| B.电子由Cu极通过导线流向Zn极 |
| C.一段时间后,ZnSO4溶液浓度增大,CuSO4溶液浓度减小 |
| D.隔膜可以避免Zn极直接接触CuSO4溶液,提高了能量转换效率 |
您最近一年使用:0次
2022-01-11更新
|
637次组卷
|
4卷引用:湖北省部分省级示范高中2020-2021学年高一下学期期末测试化学试题



