1 . 在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
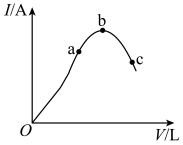
(1)a、b、c三点对应的溶液中, 由小到大的顺序为
由小到大的顺序为__________ 。
(2)a、b、c三点对应的溶液中, 的电离程度最大的是
的电离程度最大的是__________ 。
(3)若使c点对应的溶液中的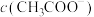 增大,则下列措施中,可行的是
增大,则下列措施中,可行的是__________ (填字母,下同)。
A.加热 B.加入NaOH固体 C.加入浓盐酸溶液
D.加水 E.加入 固体 F.加入锌粒
固体 F.加入锌粒
(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是__________。
(5)依反应 设计的原电池如图1所示。
设计的原电池如图1所示。
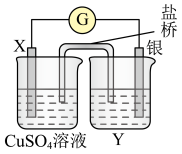
图1
请回答下列问题:
①电极X的材料是__________ ;电解质溶液Y是__________ 溶液。
②银电极为电池的__________ 极,发生的电极反应式为__________ 。

(1)a、b、c三点对应的溶液中,
 由小到大的顺序为
由小到大的顺序为(2)a、b、c三点对应的溶液中,
 的电离程度最大的是
的电离程度最大的是(3)若使c点对应的溶液中的
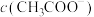 增大,则下列措施中,可行的是
增大,则下列措施中,可行的是A.加热 B.加入NaOH固体 C.加入浓盐酸溶液
D.加水 E.加入
 固体 F.加入锌粒
固体 F.加入锌粒(4)在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是__________。
A. | B. |
C. 分子数 分子数 | D.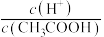 |
(5)依反应
 设计的原电池如图1所示。
设计的原电池如图1所示。
图1
请回答下列问题:
①电极X的材料是
②银电极为电池的
您最近一年使用:0次
2 . 二次电池液体锌电池具有成本低、安全性强、可循环使用等特点,其示意图如图。下列说法不正确的是
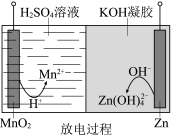

A.放电过程中, 由正极向负极迁移 由正极向负极迁移 |
B.放电过程中,正极的电极反应: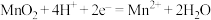 |
| C.充电时,左侧电极连接外电路直流电源的正极 |
D.充电时,阴极的电极反应: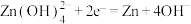 |
您最近一年使用:0次
名校
解题方法
3 . 能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。
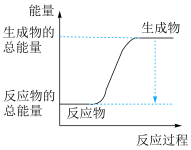
(1)下列过程的能量变化与图相符的是_______。
(2)工业上冶炼铝时,电解熔融A2O3而不电解熔融AlCl3的原因是_______ 。
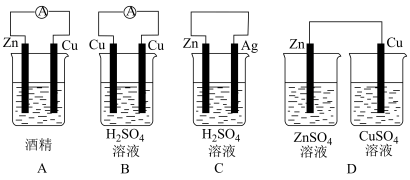
(3)下列装置中能够实现化学能转化为电能的是_______ 。
(4)某化学兴趣小组利用反应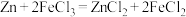 ,设计了下图所示的原电池装置。
,设计了下图所示的原电池装置。
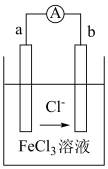
①b电极为_______ 极,a电极的电极反应式为_______ 。
②若电路中有0.4mol电子通过时,溶液质量增加_______ g。
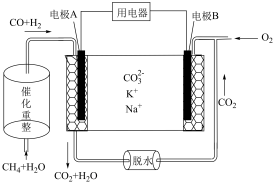
(5)科学家发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。电池工作时,外电路上电子移动的方向应从电极_______ (填A或B)流向用电器。内电路中正离子向电极_______ (填A或B)移动。
(1)下列过程的能量变化与图相符的是_______。

| A.铝热反应 | B.Ba(OH)2·8H2O晶体与NH4Cl晶体反应 |
| C.铁在氯气中燃烧 | D.碳酸氢钠溶液与柠檬酸反应 |
(2)工业上冶炼铝时,电解熔融A2O3而不电解熔融AlCl3的原因是
(3)下列装置中能够实现化学能转化为电能的是

(4)某化学兴趣小组利用反应
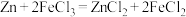 ,设计了下图所示的原电池装置。
,设计了下图所示的原电池装置。
①b电极为
②若电路中有0.4mol电子通过时,溶液质量增加
(5)科学家发明了一种以熔融碳酸盐为离子导体的新型燃料电池,工作原理如下图所示。电池工作时,外电路上电子移动的方向应从电极

您最近一年使用:0次
名校
解题方法
4 . 甲醇(化学式: )是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
)是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知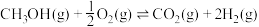 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是___________ (填字母)。 转变成
转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程
b.化学变化不仅有新物质生成,同时也一定有能量变化
c. 的生成速率与
的生成速率与 的消耗速率之比为
的消耗速率之比为
d.1mol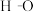 键断裂的同时2mol
键断裂的同时2mol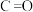 键断裂,则反应达最大限度
键断裂,则反应达最大限度
(2)某温度下,将5mol 和2mol
和2mol 充入2L的密闭容器中,经过4min反应达到平衡,测得
充入2L的密闭容器中,经过4min反应达到平衡,测得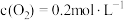 ,4min内平均反应速率
,4min内平均反应速率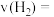
___________ ,则 的转化率为
的转化率为___________ 。
(3) 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为___________ ,下列说法正确的是___________ (填序号)。
b.电池放电时,电解质溶液的碱性逐渐减弱
c.电池放电时每消耗6.4g 转移1.2mol电子
转移1.2mol电子
d.电池放电时 向a电极移动
向a电极移动
(4)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别加入甲醇和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则c电极的名称为
。则c电极的名称为___________ (填“正极”或“负极”),d电极上的电极反应式为___________ 。
 )是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
)是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。(1)已知
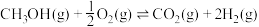 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是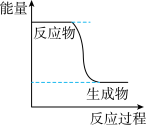
 转变成
转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程b.化学变化不仅有新物质生成,同时也一定有能量变化
c.
 的生成速率与
的生成速率与 的消耗速率之比为
的消耗速率之比为
d.1mol
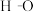 键断裂的同时2mol
键断裂的同时2mol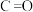 键断裂,则反应达最大限度
键断裂,则反应达最大限度(2)某温度下,将5mol
 和2mol
和2mol 充入2L的密闭容器中,经过4min反应达到平衡,测得
充入2L的密闭容器中,经过4min反应达到平衡,测得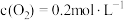 ,4min内平均反应速率
,4min内平均反应速率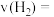
 的转化率为
的转化率为(3)
 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
燃料电池是目前开发最成功的燃料电池之一,这种燃料电池如图所示,由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为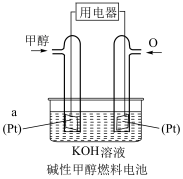
b.电池放电时,电解质溶液的碱性逐渐减弱
c.电池放电时每消耗6.4g
 转移1.2mol电子
转移1.2mol电子d.电池放电时
 向a电极移动
向a电极移动(4)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别加入甲醇和空气,其中固体电解质是掺杂了
 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则c电极的名称为
。则c电极的名称为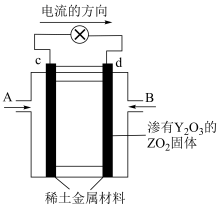
您最近一年使用:0次
5 . 电化学技术在处理污染气体领域的应用广泛。
(1)用 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的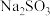 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
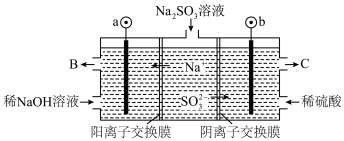
①图中a极要连接电源的_____ (填“正”或“负”)极,C口流出的物质是_____ 。
② 放电时的电极反应式为
放电时的电极反应式为_____ 。
(2)工业上也可直接以含 废气为原料,用电化学方法制取硫酸,装置如图。
废气为原料,用电化学方法制取硫酸,装置如图。
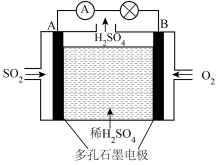
①写出负极反应式_____ 。
②写出正极反应式_____ 。
(1)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
①图中a极要连接电源的
②
 放电时的电极反应式为
放电时的电极反应式为(2)工业上也可直接以含
 废气为原料,用电化学方法制取硫酸,装置如图。
废气为原料,用电化学方法制取硫酸,装置如图。
①写出负极反应式
②写出正极反应式
您最近一年使用:0次
6 . 如图所示的锌 铜及稀硫酸组成的原电池中,下列有关说法正确的是
铜及稀硫酸组成的原电池中,下列有关说法正确的是
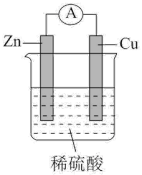
 铜及稀硫酸组成的原电池中,下列有关说法正确的是
铜及稀硫酸组成的原电池中,下列有关说法正确的是

A.锌片上有气泡产生,溶液中的 变小 变小 |
| B.电子从铜片沿导线流向锌片 |
C.稀硫酸中, 移向铜片 移向铜片 |
D.铜片上的电极反应为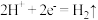 |
您最近一年使用:0次
名校
解题方法
7 . 我国科学家利用废弃塑料设计了微生物燃料电池(A、B电极材料均为石墨烯),其工作原理如图所示。下列说法错误的是
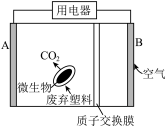

| A.A电极作负极 |
B. 经过质子交换膜从A电极向B电极移动 经过质子交换膜从A电极向B电极移动 |
| C.B电极采用疏松多孔的石墨烯,主要是为了增强溶液的导电性 |
D.若废弃塑料为聚乙烯,A电极的电极反应式为 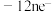 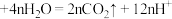 |
您最近一年使用:0次



