名校
解题方法
1 . 回答下列问题:
(1)下列反应是氧化还原反应且是吸热反应的是____ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____ ,当线路中转移0.2mol电子时,则被腐蚀铜的质量为____ g。
(3)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为____ ,正极附近溶液的碱性____ (填“增强”“减弱”“不变”)。
(4)实验小组对可逆反应aX(g)+bY(g) pZ(g)进行探究。回答下列问题:
pZ(g)进行探究。回答下列问题:
T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
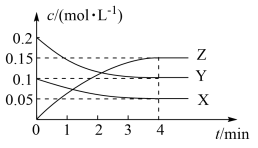
①0~4min内的反应速率v(Y)=____ 。
②为提高此反应的速率,下列措施可行的是____ (填字母代号)。
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达最大限度时Y的体积分数为____ 。
④下列描述能表示该反应达平衡状态的是____ 。
A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.2v(X)=v(Y)
D.X的体积分数不再改变
(1)下列反应是氧化还原反应且是吸热反应的是
| A.稀醋酸与烧碱溶液反应 | B.灼热的炭与CO2的反应 |
| C.铁片与稀盐酸的反应 | D.Ba(OH)2•8H2O与NH4Cl的反应 |
(3)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为(4)实验小组对可逆反应aX(g)+bY(g)
 pZ(g)进行探究。回答下列问题:
pZ(g)进行探究。回答下列问题:T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。

①0~4min内的反应速率v(Y)=
②为提高此反应的速率,下列措施可行的是
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达最大限度时Y的体积分数为
④下列描述能表示该反应达平衡状态的是
A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.2v(X)=v(Y)
D.X的体积分数不再改变
您最近一年使用:0次



