1 . 电池在我们的生活中有着重要的应用,请回答下列问题:
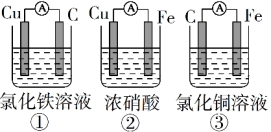
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______ (填序号),写出正极的电极反应式______________ 。若构建原电池时两个电极的质量相等,当导线中通过0.05 mol电子时,两个电极的质量差为_____________ 。
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH−向B 电极定向移动,则_____ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_________________ 当消耗甲烷的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为________ 。
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH−向B 电极定向移动,则
您最近一年使用:0次
2018-06-29更新
|
699次组卷
|
8卷引用:甘肃省临泽县第一中学2017-2018学年高一下学期6月月考化学试题
名校
解题方法
2 . (1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:Cd+2NiO(OH)+2H2O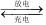 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是___________ ,负极的反应式是___________ 。放电时负极附近的溶液的碱性________ (填“不变”、“变大”或“变小”)。
(2)一种熔融碳酸盐燃料电池原理示意如图所示:

电池工作时,外电路上电流的方向应从电极________ (填A或B)流向用电器。内电路中,CO32-向电极___________ (填A或B)移动,电极A上CO参与的电极反应为___________ 。
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲醇(CH3OH)和氧气构成燃料电池,则通入甲醇的电极是原电池的____ 极,该极的电极反应式是____________ ,通入氧气的电极是原电池的____ 极,电极反应式是___________________ 。如果消耗甲醇160 g,假设化学能完全转化为电能,则转移电子的数目为_______________ (用NA表示)。
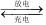 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是(2)一种熔融碳酸盐燃料电池原理示意如图所示:

电池工作时,外电路上电流的方向应从电极
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲醇(CH3OH)和氧气构成燃料电池,则通入甲醇的电极是原电池的
您最近一年使用:0次



