名校
解题方法
1 . 下列四个常用电化学装置的叙述正确的是
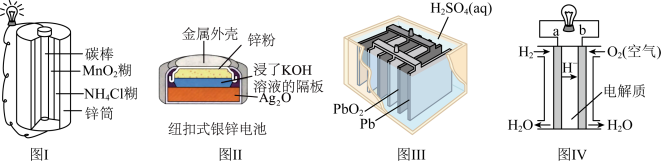

| A.图Ⅰ所示电池中,电子由碳棒通过导线流向锌筒 |
| B.图Ⅱ所示电池中,锌为负极,发生氧化反应 |
| C.图Ⅲ所示电池为二次电池,可无限次重复使用 |
D.图Ⅳ所示电池,b电极为正极,电极反应式为: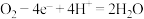 |
您最近一年使用:0次
2023-05-02更新
|
383次组卷
|
3卷引用:山东菏泽市曹县一中2022-2023学年高一下学期5月月考化学试题
解题方法
2 . 氢氧燃料电池可以使用在航天飞机上,其反应原理如图。下列有关氢氧燃料电池的说法错误的是


| A.该电池工作时化学能转化为电能 | B.该电池工作时OH-向b极移动 |
| C.外电路中电子由电极a通过导线流向电极b | D.a极的电极反应是H2-2e-=2H+ |
您最近一年使用:0次
3 . Ⅰ.在1×105Pa、298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能(已知氨分子中有三个等价的氮氢共价键):
(1)根据上表中的数据判断工业合成氨的反应是___________ (填“吸热”或“放热”)反应。
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为___________ kJ。
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小关系为___________ 。
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
Ⅱ.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是CH4-8e-+10OH-=CO +7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
+7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
(1)通入CH4的电极为___________ 极,发生___________ 反应。
(2)若将该电池中的燃料改为氢气,其正极反应式为O2+4e-+2H2O=4OH-,则其负极反应式为___________ 。
| 共价键 | H—H | N≡N | N—H |
| 键能(kJ·mol-1) | 436 | 945 | 391 |
(1)根据上表中的数据判断工业合成氨的反应是
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小关系为
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
Ⅱ.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入CH4的一极,其电极反应式是CH4-8e-+10OH-=CO
 +7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:
+7H2O;通入O2的另一极,其电极反应式是2O2+8e-+4H2O=8OH-。请完成下列各题:(1)通入CH4的电极为
(2)若将该电池中的燃料改为氢气,其正极反应式为O2+4e-+2H2O=4OH-,则其负极反应式为
您最近一年使用:0次
解题方法
4 . 人们应用原电池原理制作了多种电池,以满足不同的需求。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时发生的电池反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则正极的电极反应式为__________________________________________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用的电极材料为__________ ;电解质溶液为__________ ,当电路中转移0.2 mol 电子时,被腐蚀的铜的质量为________ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为________ (填标号)。
A.铝片.铜片 B.铜片.铝片 C.铝片.铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图,试回答下列问题:

①氢氧燃料电池的总反应方程式为_____________ ;
②电池工作一段时间后硫酸溶液的浓度会________ (填“增大”“减小”或“不变”)。
(1)铅蓄电池在放电时发生的电池反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,则正极的电极反应式为
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用的电极材料为
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片.铜片 B.铜片.铝片 C.铝片.铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图,试回答下列问题:

①氢氧燃料电池的总反应方程式为
②电池工作一段时间后硫酸溶液的浓度会
您最近一年使用:0次
2020-10-09更新
|
358次组卷
|
2卷引用:山东省菏泽市单县第五中学2020-2021学年高二上学期第一次月考(10月)化学试题
2016高一·全国·课时练习
解题方法
5 . 人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
正极电极反应式为______________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_____________ ,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为_____________ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为______________ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
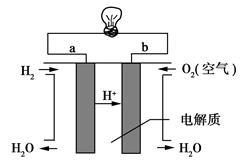
①氢氧燃料电池的总反应化学方程式是:________________ 。
②电池工作一段时间后硫酸溶液的浓度_____________ (填“增大”、“减小”或“不变”)。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
正极电极反应式为
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:
②电池工作一段时间后硫酸溶液的浓度
您最近一年使用:0次
2020-09-13更新
|
971次组卷
|
3卷引用:山东省菏泽市单县第五中学2020-2021学年高二上学期开学考试化学试题
11-12高二上·山东菏泽·阶段练习
解题方法
6 . 据报道,我国拥有完全自主产权的氢氧燃料电池车将在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是
| A.正极反应式为:O2+2H2O+4e-=4OH- |
| B.工作一段时间后,电解液中的KOH的物质的量不变 |
| C.负极反应式为:H2-2e-=2H+ |
| D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移 |
您最近一年使用:0次
名校
7 . 下列叙述中,正确的是( )
| A.钢铁腐蚀的负极反应为:Fe-3e-=Fe3+ |
| B.Mg-Al及NaOH溶液构成的原电池中负极材料为Mg |
| C.无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液中的有效成分NaClO |
| D.H2-O2燃料电池中电解液为H2SO4,则正极反应式为:O2+4e-=2O2- |
您最近一年使用:0次
2017-11-08更新
|
537次组卷
|
3卷引用:山东省鄄城县第一中学2022-2023学年高一下学期5月月考化学试题
8 . (1)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-
则A极是电池的________ 极;电子从该极________ (填“流入”或“流出”)。
(2)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________ ,发生的电极反应为__________________ 。
A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-
则A极是电池的
(2)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
您最近一年使用:0次
9 . 根据如图回答,下列说法不正确的是


| A.此装置用于铁表面镀铜时,a为铁 |
| B.此装置用于电镀铜时,硫酸铜溶液的浓度不变 |
| C.燃料电池中正极反应为1/2O2+2e-+2H+===H2O |
| D.若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜 |
您最近一年使用:0次
2016-12-09更新
|
332次组卷
|
7卷引用:山东省菏泽市第一中学老校区2018-2019学年高二上学期期末模拟化学试题
2013·山东菏泽·二模
解题方法
10 . A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是___________ (填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于_____________________ 。
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为:______________________________________________________ 。
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为_______________________ ,
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的pH=_____ (假设电解过程中溶液的体积不变) 。
(4)可逆反应2EC2(气)+C2(气) 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )______ t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A )_______ a( B )。

(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有_____________ (填“序号”)。
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为:
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的pH=
(4)可逆反应2EC2(气)+C2(气)
 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )
(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易
您最近一年使用:0次



