1 . 其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
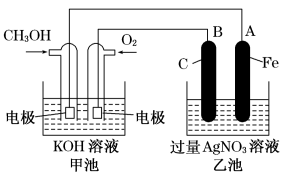
(1)甲池中,通入甲醇电极反应式为___________ 。
(2)乙池中,总反应式为___________ 。
(3)在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2___________ L(标准状况下)。
(4)若甲池中乙醇与氧气互换,则乙池中A端反应式为___________ B端现象为___________ 。

(1)甲池中,通入甲醇电极反应式为
(2)乙池中,总反应式为
(3)在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2
(4)若甲池中乙醇与氧气互换,则乙池中A端反应式为
您最近一年使用:0次
2021-11-02更新
|
327次组卷
|
2卷引用:宁夏银川市第六中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
2 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
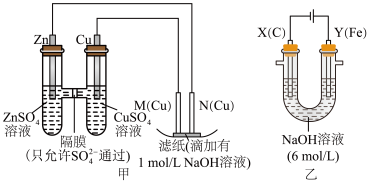
Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,
________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________________ 。
(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和_________________ 。
II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:
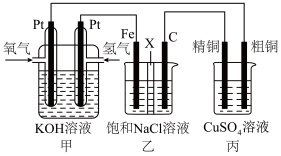
(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为____
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用________ 交换膜(填“阳离子”或“阴离子”)
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减 小”或“不变”)
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.
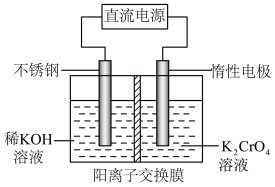
(1)不锈钢作_________ 极
(2)分析阳极区能得到重铬酸钾溶液的原因________________________________________________ 。

Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,

(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:

(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.

(1)不锈钢作
(2)分析阳极区能得到重铬酸钾溶液的原因
您最近一年使用:0次
名校
解题方法
3 . 由于存在同种电解质溶液的浓度差而产生电动势的电池称为浓差电池。利用浓差电池电解硫酸钠溶液可以制得氧气、氢气、硫酸和氢氧化钠,其装置如图所示(a、b电极均为石墨电极)。下列说法正确的是(已知:溶液A为 1L 1mol/L AgNO3溶液; 溶液B为 1L 4mol/L AgNO3溶液)
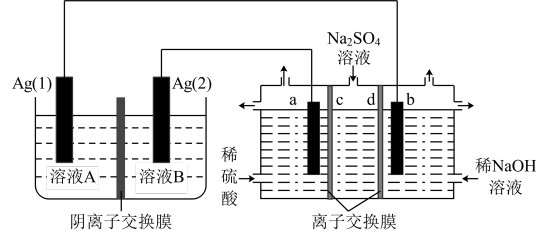

| A.电池放电过程中Ag(1)为正极,电极反应为Ag+ + e-= Ag |
| B.a电极的电极反应为2H2O-4e-=O2↑+4H+,b电极上发生的是还原反应 |
| C.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 |
| D.电池从开始工作到停止放电,电解池理论上可制得80g氢氧化钠 |
您最近一年使用:0次
2021-04-30更新
|
1111次组卷
|
6卷引用:宁夏银川一中2020-2021学年高二下学期期中考试化学试题
宁夏银川一中2020-2021学年高二下学期期中考试化学试题福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题河南省南阳市2022-2023学年高二上学期10月期中考试化学试题河南省南阳市方城县第一高级中学2022-2023学年高二上学期11月期中考试化学试题(已下线)2022年浙江1月高考真题变式题(21-25)(已下线)化学-2023年高考押题预测卷01(全国乙卷)(含考试版、全解全析、参考答案、答题卡)
名校
解题方法
4 . 下列四种装置中,溶液的体积均为250mL,开始时电解质溶液的浓度均为0.10mol/L,工作一段时间后,测得导线上均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述正确的是
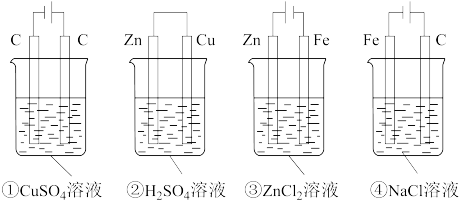

| A.工作一段时间后产生气体的总体积:②>④>①>③ |
| B.工作一段时间后溶液的pH:④>③>①>② |
| C.工作一段时间后原溶液的浓度:①=②=③=④ |
| D.工作一段时间后电极上析出固体的质量:②>①>③>④ |
您最近一年使用:0次
名校
解题方法
5 . 丙烷(C3H8)熔融盐燃料电池和锌蓄电池均为用途广泛的直流电源,放电时锌蓄电池的总反应为2Zn+O2=2ZnO。用丙烷(C3H8)燃料电池为锌蓄电池充电的装置如图所示,下列说法不正确的是
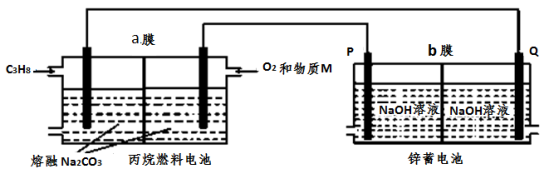

| A.物质M为CO2,该电池使用过程中不需要补充Na2CO3 |
| B.燃料电池消耗1molO2时,理论上有4molOH-透过b膜向P电极移动 |
| C.该装置工作时,电子通过由Q经电解质溶液穿过阴离子交换膜回到P电极 |
| D.该装置工作时,锌蓄电池的负极上发生的反应式为: ZnO+H2O+2e-= Zn+2OH- |
您最近一年使用:0次
名校
解题方法
6 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。请按要求回答相关问题:
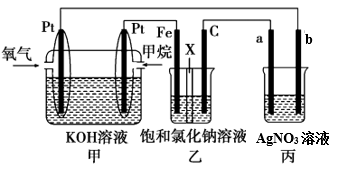
(1)甲装置电池负极发生的电极反应式是:_______
(2)乙中X是_______ (阴、阳)离子交换膜,向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因_______
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为_______
(4)若丙装置中a、b电极均为Cu,则丙中发生的离子反应是_______
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解 的原理如图所示
的原理如图所示
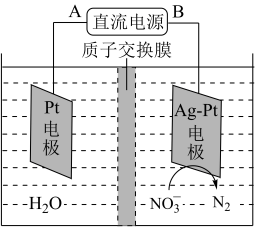
Ag-Pt电极上的电极反应式为_______

(1)甲装置电池负极发生的电极反应式是:
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
(4)若丙装置中a、b电极均为Cu,则丙中发生的离子反应是
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解
 的原理如图所示
的原理如图所示
Ag-Pt电极上的电极反应式为
您最近一年使用:0次
2021-02-15更新
|
120次组卷
|
2卷引用:宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题
7 . 烧杯A中盛放0.1 mol/L的H2SO4溶液,烧杯B中盛放0.1 mol/L的CuCl2溶液(两种溶液均足量),组成的装置如图所示。下列说法不正确的是
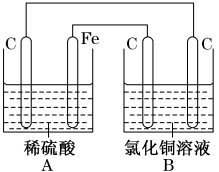

| A.经过一段时间,B烧杯中溶液的质量减小 |
| B.B为原电池 |
| C.当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol |
| D.A装置中C有气泡产生但C不参与反应 |
您最近一年使用:0次
2021-05-13更新
|
154次组卷
|
2卷引用:宁夏银川市第六中学2021-2022学年高二上学期第一次月考化学试题
9-10高二下·河北·阶段练习
名校
解题方法
8 . 下面有关电化学的图示,完全正确的是
A.Cu-Zn原电池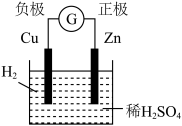 | B.粗铜的精炼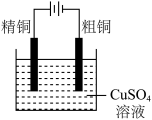 |
C.铁片镀锌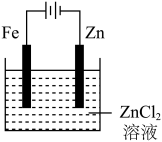 | D.验证NaCl溶液(含酚酞)电解产物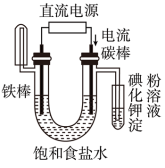 |
您最近一年使用:0次
2022-12-21更新
|
689次组卷
|
59卷引用:宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】
宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】(已下线)2009—2010学年存瑞中学第二学期第二阶段考试高二化学试题2014-2015湖南省娄底市湘中名校高二上学期期末化学(理)试卷2014-2015学年福建省晋江市季延中学高二下学期期中考试化学试卷2015-2016学年河北省成安一中高二上学期1月月考化学试卷2015-2016学年黑龙江东部地区高二上学期期末联考化学试卷2016-2017学年山东省寿光中学高二上10月月考化学卷2017届宁夏石嘴山三中高三上期中化学试卷2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷内蒙古包头市铁路一中2016-2017学年高二下学期期末考试化学试题山东省寿光现代中学2017-2018学年高二上学期开学考试化学试题河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题河南省安阳市2016-2017学年高二上学期期末考试化学试题青海省西宁市第四高级中学2017-2018学年高二上学期期末考试化学试题山东省德州市2017-2018学年高二上学期期末考试化学试题四川省什邡中学2017-2018学年高二春秋招班第三次月考化学试题云南省腾冲市第八中学2017-2018学年高二下学期期末考试化学试题河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题高二人教版选修4 第四章 第三节 电解池【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安第四中学2018-2019学年高二上学期12月月考化学试题【校级联考】江西省吉安市几所重点中学2018-2019学年高二上学期联考化学试题【全国百强校】江西省临川第一中学2018-2019学年高二上学期12月月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题【全国百强校】黑龙江省大庆市第一中学2018-2019学年高二下学期第三次阶段考试化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题广东省深圳科学高中2019-2020学年高二上学期开学考试化学试题浙江省宁波市余姚中学2019-2020学年高二上学期期中考试化学试题黑龙江省大庆市第十中学2019-2020学年高二上学期期末考试化学试题陕西省咸阳市2019—2020学年高二上学期期末考试化学试题湖南广益实验中学2019-2020学年高二上学期期末考试化学试题四川省新津中学2019-2020学年高二下学期4月月考(入学)化学试题江西省上饶市2018-2019学年高二下学期期末教学质量测试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高二上学期开学考试(8月)化学试题宁夏银川市宁夏大学附属中学2021届高三上学期第一次月考化学试题(已下线)【浙江新东方】43山东省泰安市宁阳一中2020-2021学年高二上学期10月学习质量检测化学试题 山东省泰安市宁阳县宁阳一中2020-2021学年高二上学期第一阶段考试化学试题(已下线)【浙江新东方】绍兴qw124内蒙古北京八中乌兰察布分校2020-2021学年高二上学期期末考试化学试题安徽省六安市舒城县舒州中学2020-2021学年高二上学期12月月考化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期质量检测月考化学试题安徽省泗县第一中学2021-2022学年高二上学期第二次月考化学试题河北省邢台市第一中学2021-2022学年高二上学期第三次月考化学试题陕西省安康市六校联考2021-2022学年高二上学期期末考试化学试题四川省凉山州2021-2022学年高二上学期期末考试化学试题陕西省西安市西航一中2021-2022学年高二上学期期末考试化学试题(已下线)第29讲 第四章《化学反应与电能》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)辽宁省锦州市黑山县黑山中学2021-2022学年高二上学期12月月考化学试题广东省兴宁市下堡中学2021-2022学年高二上学期期末质量检测化学试题福建省宁德第一中学2020-2021学年高二上学期第一次月考化学试题2015届江西省吉安市白鹭洲中学高三上学期期中化学试卷2015届上海市虹口区高三上学期期末考试化学试卷2015-2016学年广西钦州港经济开发区中学高一上学期期末化学试卷【全国百强校】上海市复旦大学附属中学2019—2020学年高三上学期期中考试化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
9 . 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池,其工作原理如下图,有关说法正确的是
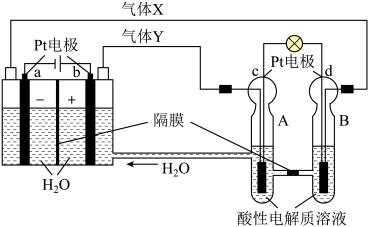

| A.c极上发生的电极反应式:O2+2H2O+4e-=4OH- |
| B.左端装置中化学能转化为电能,右端装置中电能转化为化学能 |
| C.d极上进行还原反应,右端装置B中的H+ 可以通过隔膜进入A |
| D.当有0.1 mol电子转移时,a极产生标准状况下1.12 LH2 |
您最近一年使用:0次
2020-11-27更新
|
247次组卷
|
5卷引用:宁夏银川市贺兰一中2023-2024学年高二上学期第三阶段考试化学试题
名校
解题方法
10 . (1)如图所示装置:若烧杯中溶液为稀硫酸,则正极反应为_____________ 。若烧杯中溶液为氢氧化钠溶液,则负极反应为___________ 。将铝片和铜片用导线相连,插入浓硝酸中,电池总反应为___________ 。
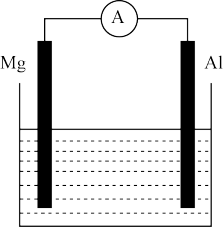
(2)钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义。
①下列各种情况,在其中Fe片腐蚀由快到慢的顺序为_____________
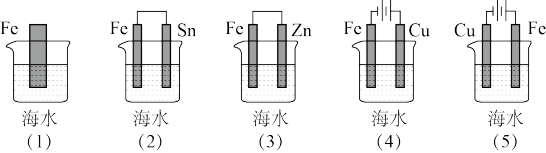
②利用下图装置,可以模拟铁的电化学防护。
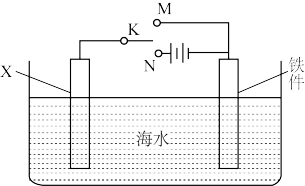
若X为碳棒,为减缓铁件的腐蚀,开关K应置于____________ 处
若X为碳棒,开关K置于M处,则碳棒发生的电极反应为_________ ,产生氢氧化铁的化学方程式为__________ 。若X为锌,开关K置于M处,该电化学防护法称为________________ 。
(3)利用氧化还原反应 可设计出原电池。在方框内画出所设计的双液原电池的示意图,并标出正负极材料和电解质溶液
可设计出原电池。在方框内画出所设计的双液原电池的示意图,并标出正负极材料和电解质溶液__________ 。

(2)钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义。
①下列各种情况,在其中Fe片腐蚀由快到慢的顺序为

②利用下图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁件的腐蚀,开关K应置于
若X为碳棒,开关K置于M处,则碳棒发生的电极反应为
(3)利用氧化还原反应
 可设计出原电池。在方框内画出所设计的双液原电池的示意图,并标出正负极材料和电解质溶液
可设计出原电池。在方框内画出所设计的双液原电池的示意图,并标出正负极材料和电解质溶液
您最近一年使用:0次



