解题方法
1 . 如下图所示的装置中,若通入直流电5min时,铜电极质量增加2.16g,试回答:
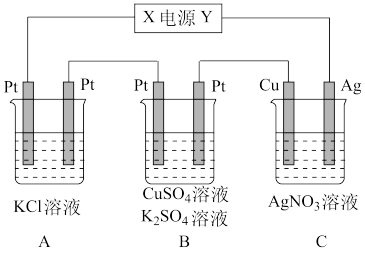
(1)电源电极X的名称为___________ 。
(2)pH变化:A___________ (填“增大”、“减小”或“不变),B___________ ,C___________ 。
(3)通电5min后,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为___________ (设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200mL,电解后,溶液中OH-的物质的量浓度为___________ (设电解前后溶液体积无变化)。

(1)电源电极X的名称为
(2)pH变化:A
(3)通电5min后,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为
(4)若A中KCl溶液的体积也是200mL,电解后,溶液中OH-的物质的量浓度为
您最近半年使用:0次
名校
解题方法
2 . 已知高能锂离子电池的总反应式为:2Li+FeS=Fe+Li2S[LiPF6·SO(CH3)2为电解质]。用该电池为电源,石墨为电极进行如图的电解实验
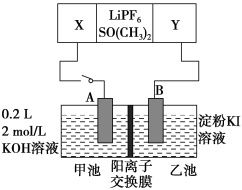
①当电极X减少2.8g时,电子转移___________ mol。(电解质均足量)。
②当电流为I A(1安培=1库仑/秒),通过时间t s时,甲池增重mg(每个电子的电量为q库伦),请写出阿伏加德罗常数的表达式___________ 。

①当电极X减少2.8g时,电子转移
②当电流为I A(1安培=1库仑/秒),通过时间t s时,甲池增重mg(每个电子的电量为q库伦),请写出阿伏加德罗常数的表达式
您最近半年使用:0次
解题方法
3 . 某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。
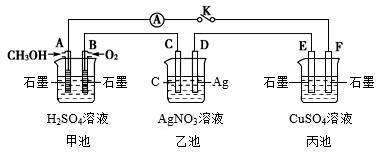
请回答下列问题:
(1)甲池为__ (填“原电池”“电解池”或“电镀池”),通入O2电极的电极反应式为__ 。
(2)乙池中C(石墨)电极的名称为___ (填“正极”“负极”或“阴极”“阳极”),总反应的化学方程式为____ 。
(3)当乙池中D极质量增加5.4g时,甲池中理论上消耗O2的体积为___ mL(标准状况),转移的电子数为__ 。
(4)丙池中__ (填“E”或“F”)极析出铜。
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将__ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池中C(石墨)电极的名称为
(3)当乙池中D极质量增加5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将
您最近半年使用:0次
解题方法
4 . 研究电化学过程的实验装置如图所示。
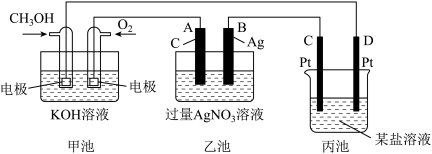
(1)甲池中通入O2的一极作__________ 极,通入CH3OH的电极的电极反应式为:____________ 。
(2)乙池中总反应的化学方程式为___________
(3)当乙池中B(Ag)电极的质量增加5.40g时,甲池中理论上消耗O2_________ mL(标准状况下)。

(1)甲池中通入O2的一极作
(2)乙池中总反应的化学方程式为
(3)当乙池中B(Ag)电极的质量增加5.40g时,甲池中理论上消耗O2
您最近半年使用:0次
解题方法
5 . 蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2 + Fe + 2H2O Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。
(1)此电池放电时_____ (填正极或负极)发生还原反应,该物质是_____ (填序号)。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)用此蓄电池分别电解以下两种溶液,假如电路中转移了0.02 mol电子,且电解池的电极均为惰性电极,试回答下列问题。
①电解M(NO3)x溶液时某一电极增加了ag M,则金属M的相对原子质量为__________ (用含“a、x”的表达式表示)。
②电解含有0.01 mol CuSO4和0.01 mol NaCl的混合溶液100mL,阳极产生的气体在标准状况下的体积是______ ;将电解后的溶液加水稀释至1L,此时溶液的c(H+)=________ 。
 Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。(1)此电池放电时
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)用此蓄电池分别电解以下两种溶液,假如电路中转移了0.02 mol电子,且电解池的电极均为惰性电极,试回答下列问题。
①电解M(NO3)x溶液时某一电极增加了ag M,则金属M的相对原子质量为
②电解含有0.01 mol CuSO4和0.01 mol NaCl的混合溶液100mL,阳极产生的气体在标准状况下的体积是
您最近半年使用:0次
2020-10-11更新
|
266次组卷
|
2卷引用:山东省菏泽市单县第五中学2020-2021学年高二上学期第一次月考(10月)化学试题
6 . 如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
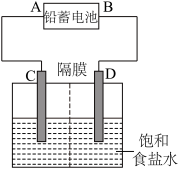
已知:铅蓄电池在放电时发生下列电极反应:
负极:Pb+SO42--2e-=PbSO4正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式__ 。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为__ 极。
(3)用铅蓄电池电解200ml浓度为0.5mol/LCuSO4 溶液一段时间后
①若两极收集到的气体体积相等,则转移电子_____ mol。
②阳极收集到的气体体积(标准状况下)为_____ L。

已知:铅蓄电池在放电时发生下列电极反应:
负极:Pb+SO42--2e-=PbSO4正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为
(3)用铅蓄电池电解200ml浓度为0.5mol/LCuSO4 溶液一段时间后
①若两极收集到的气体体积相等,则转移电子
②阳极收集到的气体体积(标准状况下)为
您最近半年使用:0次
名校
解题方法
7 . 某兴趣小组的同学用图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)通入 CH3OH 电极的电极反应:___________________ 。
(2)乙池中 A(石墨)电极的名称为_________________ (填“正极”、“负极”或“阴极”、“阳极”),总化学反应式为___________________ 。
(3)当乙池中 B 极质量增加 5.40g 时,甲池中理论上消耗 O2的体积为_______ mL(标准状况)。若丙池中KCl溶液的体积是500mL,电解后,溶液的pH为_________ (设电解前后溶液体积无变化)。

请回答下列问题:
(1)通入 CH3OH 电极的电极反应:
(2)乙池中 A(石墨)电极的名称为
(3)当乙池中 B 极质量增加 5.40g 时,甲池中理论上消耗 O2的体积为
您最近半年使用:0次
名校
8 . 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,弃去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计的装置示意图如图所示。
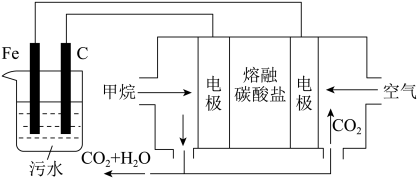
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________ 。
a.H2SO4
b.CH3CH2OH
c.Na2SO4
d.NaOH
(2)电解过程中,电解池阳极发生了两个电极反应,其中一个为2H2O-4e- = O2↑+4H+,则另一个电极反应式为_____________________________ 。
(3)电解池溶液中得到Fe(OH)3沉淀的离子方程式为_______________________________ 。
(4)熔融盐燃料电池以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料为电极。
①负极的电极反应式为__________________________________________ ;
②正极的电极反应式为__________________________________________ 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)_____ L。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的
a.H2SO4
b.CH3CH2OH
c.Na2SO4
d.NaOH
(2)电解过程中,电解池阳极发生了两个电极反应,其中一个为2H2O-4e- = O2↑+4H+,则另一个电极反应式为
(3)电解池溶液中得到Fe(OH)3沉淀的离子方程式为
(4)熔融盐燃料电池以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料为电极。
①负极的电极反应式为
②正极的电极反应式为
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)
您最近半年使用:0次
2019-02-26更新
|
589次组卷
|
3卷引用:广州省广州市石化中学2018-2019学年高二上学期期末考试化学试题
10-11高二下·浙江绍兴·期末
9 . 有下图所示的装置:

该装置中离子交换膜只允许______ 离子通过。反应一段时间后,向烧杯中加入0.1molCu(OH)2后恰好恢复到反应前的CuSO4溶液的浓度和pH。则反应过程中消耗锌的质量为_________________ g ,烧杯左侧碳棒上析出物质的量为__________ mol。在此过程中烧杯中右侧电极上发生的电极反应方程式为:__________________________________

该装置中离子交换膜只允许
您最近半年使用:0次
10-11高一下·江苏盐城·期末
10 . 铅蓄电池属于二次电池,其电极材料分别是Pb和PbO2,电解质溶液为一定浓度的硫酸,工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O;PbSO4不溶。
(1)该蓄电池工作时负极的电极反应式为_______________________________________
(2)将质量相等的铁棒和石墨棒分别插入CuSO4溶液中,铁棒接该蓄电池Pb极,石墨棒接该蓄电池PbO2极,一段时间后测得铁棒比石墨棒增加了3.2克,则CuSO4溶液质量_________ (增加、减少)_________ 克;如果要求将CuSO4溶液恢复成与开始时完全相同,则可以加入下列物质中的___________
E.Cu固体 F. Cu2(OH) 2CO3固体
(3)若用该蓄电池作电源(都用惰性材料做电极)电解400克饱和食盐水,如果电池内硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数_________ (该温度下氯化钠的溶解度为32克)。
(1)该蓄电池工作时负极的电极反应式为
(2)将质量相等的铁棒和石墨棒分别插入CuSO4溶液中,铁棒接该蓄电池Pb极,石墨棒接该蓄电池PbO2极,一段时间后测得铁棒比石墨棒增加了3.2克,则CuSO4溶液质量
| A.CuSO4溶液 | B.CuCO3固体 | C.CuO固体 | D.Cu(OH)2固体 |
E.Cu固体 F. Cu2(OH) 2CO3固体
(3)若用该蓄电池作电源(都用惰性材料做电极)电解400克饱和食盐水,如果电池内硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数
您最近半年使用:0次



