解题方法
1 . 某化学兴趣小组同学对电化学原理进行了一系列探究活动。
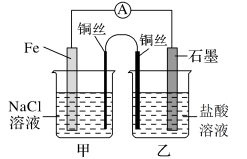
(1)如图,为某化学兴趣小组依据氧化还原反应:___________ (用离子方程式表示)设计的原电池装置,当导线中通过0.5mol电子的电量时,理论上石墨电极上产生气体体积为___________ L(标准状况下)。

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了___________ 腐蚀(填“吸氧”或“析氢”),试写出使酚酞溶液变红的电极反应式为___________ 。
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为___________ 极(填“正”、“负”、“阴”或“阳”),乙装置中总反应的离子方程式为___________ ,该反应为___________ (填“自发”或“非自发”)的氧化还原反应。___________ ,产物常用___________ 检验,一段时间后,乙装置中溶液pH___________ (填“变大”、“变小”或“不变”)。
(1)如图,为某化学兴趣小组依据氧化还原反应:

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为
您最近半年使用:0次
解题方法
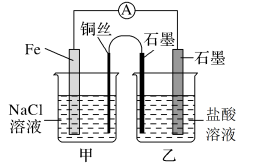
2 . 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: 溶液,则反应一段时间后:
溶液,则反应一段时间后:
①乙池中阳极的电极反应式是_______ 。
②若要保护金属铁,可将甲池中的C棒换成 棒,则该防护方法称为
棒,则该防护方法称为_______ 。
(2)若两池中电解质溶液均为饱和 溶液:
溶液:
①写出乙池中总反应的离子方程式_______ 。
②甲池中碳极上电极反应式是_______ 。
③若乙池转移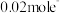 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
_______ 。

 溶液,则反应一段时间后:
溶液,则反应一段时间后:①乙池中阳极的电极反应式是
②若要保护金属铁,可将甲池中的C棒换成
 棒,则该防护方法称为
棒,则该防护方法称为(2)若两池中电解质溶液均为饱和
 溶液:
溶液:①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③若乙池转移
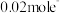 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
您最近半年使用:0次
名校
解题方法
3 . 回答下列问题
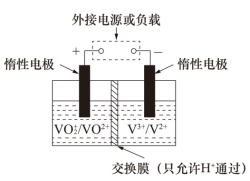
(1)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。______________ 。
②放电过程中,右槽溶液颜色逐渐由___________ 色变为___________ 色。
③放电过程中氢离子的作用是:参与正极反应和______________ 。
④放电时若转移的电子数为 个,左槽溶液中
个,左槽溶液中 的变化量为
的变化量为___________ 。
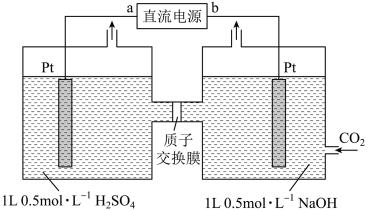
(2)某研究小组采用甲烷燃料电池作为电源,电解饱和氯化钠溶液的原理如图所示。_______________ 。
②闭合K后,a、b电极上均有气体产生,其中b电极的产物是___________ ,a电极的电极反应式为________________ 。
(1)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。

②放电过程中,右槽溶液颜色逐渐由
③放电过程中氢离子的作用是:参与正极反应和
④放电时若转移的电子数为
 个,左槽溶液中
个,左槽溶液中 的变化量为
的变化量为(2)某研究小组采用甲烷燃料电池作为电源,电解饱和氯化钠溶液的原理如图所示。

②闭合K后,a、b电极上均有气体产生,其中b电极的产物是
您最近半年使用:0次
名校
解题方法
4 . 某同学利用如图所示装置制作简单的燃料电池。
①电极a的电极反应式是_______________ 。
② 的迁移方向为
的迁移方向为_______________ (填“ ”或“
”或“ ”)。
”)。
③一段时间后,电极b附近的现象是_______________ 。
(2)一段时间后断开K1,闭合K2,电流表的指针偏转。
①电极b的电极反应式是______________ 。
②电极a附近的
___________ (选填“增大”、“减小”或“不变”)。
(3)下列说法中,不正确的是________ (填字母)。
a.通过调节K1、K2可以实现化学能和电能的相互转化
b.若将Na2SO4溶液替换为稀硫酸,闭合K2后,电极反应不变
c.闭合K1,电路中每转移4mol电子,电极a理论上产生的气体在标准状况下的体积为

①电极a的电极反应式是
②
 的迁移方向为
的迁移方向为 ”或“
”或“ ”)。
”)。③一段时间后,电极b附近的现象是
(2)一段时间后断开K1,闭合K2,电流表的指针偏转。
①电极b的电极反应式是
②电极a附近的

(3)下列说法中,不正确的是
a.通过调节K1、K2可以实现化学能和电能的相互转化
b.若将Na2SO4溶液替换为稀硫酸,闭合K2后,电极反应不变
c.闭合K1,电路中每转移4mol电子,电极a理论上产生的气体在标准状况下的体积为

您最近半年使用:0次
名校
5 . Ⅰ.下图装置的盐桥中盛有饱和 琼脂溶液,能够连接两份电解质溶液,形成闭合回路:
琼脂溶液,能够连接两份电解质溶液,形成闭合回路:___________ ,装置工作时,盐桥中的 移向
移向___________ 。(“ 溶液”或“
溶液”或“ 溶液”)
溶液”)
(2)若将盐桥换成n型铜丝,电路中也有电流通过,则左边装置是___________ ,(填“原电池”或“电解池”),则n型铜丝左端为___________ 极,该极电极反应式为:___________ 。
Ⅱ.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(3) 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。 中
中 键角比
键角比 分子中
分子中 键角
键角___________ (填“大”或“小”)。
②丁二酮肟镍分子内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键 e.共价键
(4)关于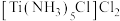 的说法中错误的是
的说法中错误的是___________ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol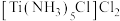 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀
 琼脂溶液,能够连接两份电解质溶液,形成闭合回路:
琼脂溶液,能够连接两份电解质溶液,形成闭合回路: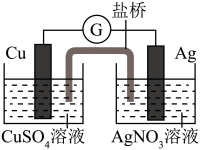
 移向
移向 溶液”或“
溶液”或“ 溶液”)
溶液”)(2)若将盐桥换成n型铜丝,电路中也有电流通过,则左边装置是
Ⅱ.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(3)
 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。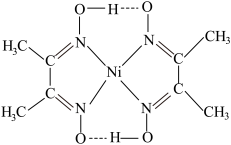
 中
中 键角比
键角比 分子中
分子中 键角
键角②丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键 e.共价键
(4)关于
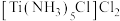 的说法中错误的是
的说法中错误的是A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol
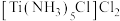 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀
您最近半年使用:0次
名校
解题方法
6 . 完成下列问题
(1)如图所示,甲池的总反应式为 ,
,___________ (填“原电池”或“电解池”),写出通入 一极发生电极反应式
一极发生电极反应式___________ 。
②乙池中电解反应的化学方程式为___________ 。
③当甲池中消耗 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是___________ 。
(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取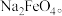 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在___________ (填“阴极室”或“阳极室”);阳极电极反应式为:___________ 。 电极上的电极反应式为
电极上的电极反应式为___________ ;
②该装置中使用的是___________ (填“阴”或“阳”)离子交换膜。
(1)如图所示,甲池的总反应式为
 ,
,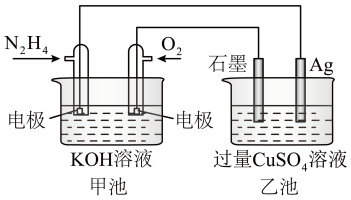
 一极发生电极反应式
一极发生电极反应式②乙池中电解反应的化学方程式为
③当甲池中消耗
 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取
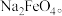 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在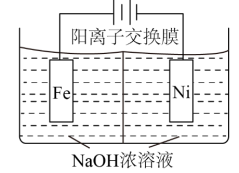
 电极上的电极反应式为
电极上的电极反应式为②该装置中使用的是
您最近半年使用:0次
7 . 认真观察下列装置,回答下列问题:
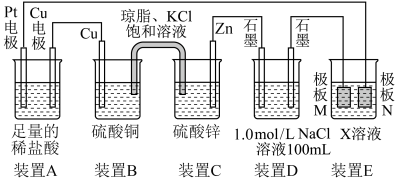
(1)C装置中,Zn电极叫___________ (填“正极”或“负极”);电极方程式为___________ ;盐桥中K+的移动方向___________ (填“向左”、“向右”或“不移动”)。
(2)电池工作初期,A装置中总反应的离子方程式为___________ 。
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为___________ ,极板M的材料为___________ 。
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为___________ L(标准状况下)。

(1)C装置中,Zn电极叫
(2)电池工作初期,A装置中总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀Ag,则X溶液中的溶质为
(4)当装置A中Cu电极质量改变12.8g时,则装置D中产生的气体体积为
您最近半年使用:0次
名校
解题方法
8 . 某化学兴趣小组用下图所示装置进行电化学原理的实验探究,试回答下列问题:

(1)通 的
的 电极为电池
电极为电池___________ 极(填电极名称):其电极方程式为___________ 。
(2)若B池为电镀池,目的是在铁上镀一层银,则X电极材料为___________ 。
(3)B池为精炼铜,且粗铜中含有 、
、 、
、 、
、 等杂质,则该电池阳极泥的主要成分是
等杂质,则该电池阳极泥的主要成分是___________ 。
(4)若B池的电解质溶液为500mL1.0mol/L的 溶液,X、Y皆为惰性电极,常温下,当电池工作一段时间,断开电源
溶液,X、Y皆为惰性电极,常温下,当电池工作一段时间,断开电源 ,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变),此时
,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变),此时 电池溶液的
电池溶液的 =
=___________ ;要使该溶液恢复到原来的状态,需加入(填物质并注明物质的量)___________ 。
(5)若X、Y均是铜,电解质溶液为 溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是
溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是 ,试写出该电极发生的电极反应式为
,试写出该电极发生的电极反应式为___________ 。

(1)通
 的
的 电极为电池
电极为电池(2)若B池为电镀池,目的是在铁上镀一层银,则X电极材料为
(3)B池为精炼铜,且粗铜中含有
 、
、 、
、 、
、 等杂质,则该电池阳极泥的主要成分是
等杂质,则该电池阳极泥的主要成分是(4)若B池的电解质溶液为500mL1.0mol/L的
 溶液,X、Y皆为惰性电极,常温下,当电池工作一段时间,断开电源
溶液,X、Y皆为惰性电极,常温下,当电池工作一段时间,断开电源 ,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变),此时
,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变),此时 电池溶液的
电池溶液的 =
=(5)若X、Y均是铜,电解质溶液为
 溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是
溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是 ,试写出该电极发生的电极反应式为
,试写出该电极发生的电极反应式为
您最近半年使用:0次
9 . I.探究原电池和电解池原理,对生产生活具有重要的意义。
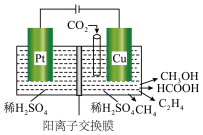
(1)近年来,有研究人员用 通过电催化生成多种燃料,其工作原理如图所示。请写出
通过电催化生成多种燃料,其工作原理如图所示。请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:___________ 。
(2)以惰性电极电解 溶液,通电一段时间后,加入0.1mol
溶液,通电一段时间后,加入0.1mol 可使溶液复原,则电路中转移电子为
可使溶液复原,则电路中转移电子为___________ mol。
(3)在直流电源作用下,双极膜中间层中的 解离为
解离为 和
和 。某技术人员利用双极膜(膜
。某技术人员利用双极膜(膜 、膜
、膜 )和离子交换膜高效制备
)和离子交换膜高效制备 和
和 ,工作原理如图所示:
,工作原理如图所示:
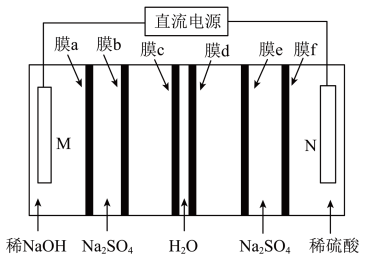
①膜 、
、 、
、 、
、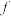 需选用阳离子交换膜的是
需选用阳离子交换膜的是___________
②当电路中转移2mol 时,整套装置将制得
时,整套装置将制得___________ mol
Ⅱ.利用电化学方法可以将CO₂有效地转化为 ,装置如图所示。
,装置如图所示。
(4)若以铅蓄电池为直流电源,则铅蓄电池中 极的电极反应式为
极的电极反应式为___________ 。
(5)装置工作时,阴极除有 生成外,还可能生成副产物,降低电解效率。
生成外,还可能生成副产物,降低电解效率。
已知:
①副产物可能是___________ (写出一种即可)。
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的 ,电解效率为
,电解效率为___________ (忽略电解前后溶液的体积变化)。
Ⅲ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。
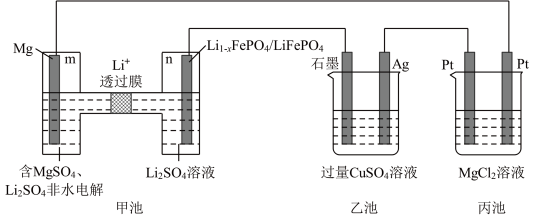
(6)放电时, 向
向___________ (填“ 极”或“
极”或“ 极”)移动;甲池中正极的电极反应式为
极”)移动;甲池中正极的电极反应式为___________ 。
(7)电解一段时间后,乙池中溶液的 将
将___________ (填“增大”、“减小”或“不变”)。
(8)丙池发生电解反应的总离子方程式为___________ 。
(1)近年来,有研究人员用
 通过电催化生成多种燃料,其工作原理如图所示。请写出
通过电催化生成多种燃料,其工作原理如图所示。请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:
(2)以惰性电极电解
 溶液,通电一段时间后,加入0.1mol
溶液,通电一段时间后,加入0.1mol 可使溶液复原,则电路中转移电子为
可使溶液复原,则电路中转移电子为(3)在直流电源作用下,双极膜中间层中的
 解离为
解离为 和
和 。某技术人员利用双极膜(膜
。某技术人员利用双极膜(膜 、膜
、膜 )和离子交换膜高效制备
)和离子交换膜高效制备 和
和 ,工作原理如图所示:
,工作原理如图所示:
①膜
 、
、 、
、 、
、 需选用阳离子交换膜的是
需选用阳离子交换膜的是②当电路中转移2mol
 时,整套装置将制得
时,整套装置将制得
Ⅱ.利用电化学方法可以将CO₂有效地转化为
 ,装置如图所示。
,装置如图所示。
(4)若以铅蓄电池为直流电源,则铅蓄电池中
 极的电极反应式为
极的电极反应式为(5)装置工作时,阴极除有
 生成外,还可能生成副产物,降低电解效率。
生成外,还可能生成副产物,降低电解效率。已知:

①副产物可能是
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的
 ,电解效率为
,电解效率为Ⅲ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。

(6)放电时,
 向
向 极”或“
极”或“ 极”)移动;甲池中正极的电极反应式为
极”)移动;甲池中正极的电极反应式为(7)电解一段时间后,乙池中溶液的
 将
将(8)丙池发生电解反应的总离子方程式为
您最近半年使用:0次
2024-04-04更新
|
167次组卷
|
2卷引用:山东省青岛超银高级中学2023-2024学年高二下学期期初考试化学试卷
10 . 研究金属腐蚀和防腐的原理很有现实意义。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。
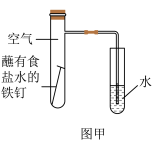
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为__________ 。

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
根据以上实验探究,试判断③______ (填“a”或“b”)为负极,该点腐蚀更严重。
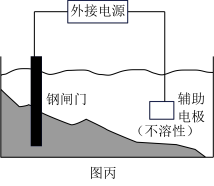
(4)图丙中钢闸门应与外接电源的__________ 相连(填“正极”或“负极”)钢闸门不会被腐蚀,属于__________ 保护法。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。

| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
实验操作 | 实验现象 | 实验结论 |
向 溶液中滴加2~3滴酚酞指示剂 溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
然后再滴加2~3滴铁氰化钾溶液 | b点周围出现监色沉淀 | b点电极反应为② |
(4)图丙中钢闸门应与外接电源的

您最近半年使用:0次



