名校
解题方法
1 . 液体锌电池是一种电压较高的二次电池,具有成本低、安全性强、可循环使用等特点,其放电过程示意图如图。下列说法不正确 的是
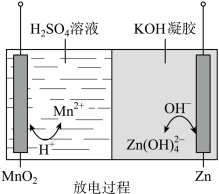
已知:① ;②KOH凝胶中允许离子存在、生成或迁移。
;②KOH凝胶中允许离子存在、生成或迁移。

已知:①
 ;②KOH凝胶中允许离子存在、生成或迁移。
;②KOH凝胶中允许离子存在、生成或迁移。A.充电过程中,阴极的电极反应: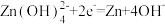 |
B.放电过程中,正极的电极反应: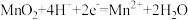 |
C.放电过程中, 由正极向负极迁移 由正极向负极迁移 |
D.在充、放电过程中,凝胶中的 可再生 可再生 |
您最近一年使用:0次
2024-01-04更新
|
511次组卷
|
7卷引用:北京市西城区2020届高三上学期期末考试化学试题
名校
解题方法
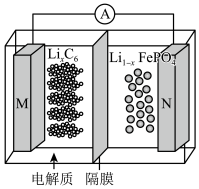
2 . 太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1- xFePO4 LiFePO4+C6,下列说法正确的是
LiFePO4+C6,下列说法正确的是
 LiFePO4+C6,下列说法正确的是
LiFePO4+C6,下列说法正确的是
A.放电时Li+从左边移向右边, 从右边移向左边 从右边移向左边 |
| B.放电时,正极反应式为 Li1-xFePO4+xLi++xe- =LiFePO4 |
C.充电时M极连接电源的负板,电极反应式为C6+xe-=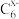 |
| D.充电时电路中通过2.0 mol电子,产生28 gLi |
您最近一年使用:0次
2023-01-26更新
|
490次组卷
|
11卷引用:湖南省长沙市周南中学2021-2022学年高二上学期(12月)第三次阶段检测卷化学试题
湖南省长沙市周南中学2021-2022学年高二上学期(12月)第三次阶段检测卷化学试题(已下线)2020年山东卷化学高考真题变式题11-15江苏省扬州中学2021-2022学年高二上学期10月阶段检测化学试题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)新疆维吾尔自治区疏附县第一中学2021-2022学年高三上学期期中考试化学试题江西省九江市第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)高中化学-高二上-10浙江省杭州高级中学2022-2023学年高三上学期模拟考试化学试题浙江省杭州外国语学校2022-2023学年高二上学期期中考试 化学试题山东省郓城第一中学2023-2024学年高二上学期开学考试化学试题江苏省南通市如东县2023-2024学年高二上学期期中学情检测化学试题
名校
3 . 相同金属在其不同浓度盐溶液中可形成浓差电池。它是通过一种物质从高浓度状态向低浓度状态的转移而获得电动势。如图所示装置是利用浓差电池电解 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和
和 。下列说法不正确的是
。下列说法不正确的是
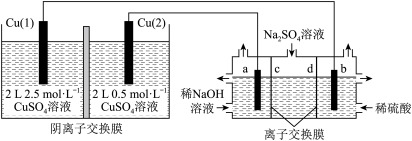
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和
和 。下列说法不正确的是
。下列说法不正确的是
A.a电极的电极反应为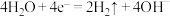 |
| B.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 |
C.电池放电过程中,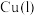 电极上的电极反应为 电极上的电极反应为 |
D.电池从开始工作到停止放电,电解池理论上可制得320g |
您最近一年使用:0次
2022-11-23更新
|
421次组卷
|
24卷引用:湖南省常德市第一中学2021届高三第四次月水平检测试化学试题
湖南省常德市第一中学2021届高三第四次月水平检测试化学试题山东省烟台市2020年高考诊断性测试(高三一模)化学试题湖南省蓝山县第二中学2021-2022学年高三下学期4月月考化学试题山东省青岛第二中学2020-2021学年高二上学期期中考试化学试题(已下线)江苏省常州市前黄高级中学、溧阳中学2021届高三上学期期末联合考试化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)【浙江新东方】高中化学20210323-001【高三下】(已下线)小题19 多池多室带膜电化学装置 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第11题 电化学基础-备战2021年高考化学临考题号押题(课标全国卷)(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)山东省济南市历城第二中学2021-2022学年(2022届)高三上学期开学考试(B)化学试题山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)2022年新高考化学时事热点情境化考题---电化学专题(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)山东省实验中学2021-2022学年高三上学期第三次诊断考试化学试题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)浙江省北仑中学2022-2023学年高二上学期期中检测化学试题武汉市第六中学2022-2023学年高二上学期第二次月考化学试题(已下线)热点题型训练 电化学串联装置的两大模型山东省青岛第二中学2021-2022学年高二上学期10月月考化学试题河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
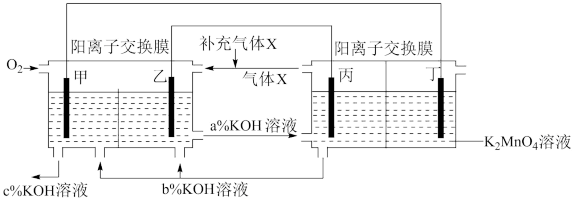
4 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为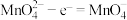 |
C.KOH溶液的质量分数: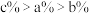 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
665次组卷
|
7卷引用:重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题
重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题
5 . 第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.其电路工作原理如图所示,下列说法正确的是


| A.放电时乙为正极,充电时乙为阴极 |
| B.汽车上坡时发生图中虚线所示的过程 |
| C.放电时负极的电极反应式为:MHn-ne-+nOH-=M+nH2O |
| D.电池充电时,OH-由甲侧向乙侧移动 |
您最近一年使用:0次
名校
解题方法
6 . 下面有关电化学的图示,完全正确的是
A.Cu-Zn原电池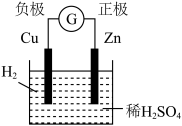 | B.粗铜的精炼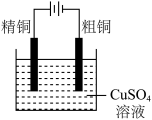 |
C.铁片镀锌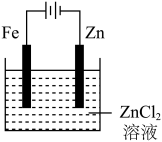 | D.验证NaCl溶液(含酚酞)电解产物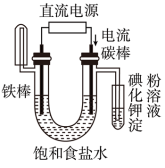 |
您最近一年使用:0次
2022-12-21更新
|
649次组卷
|
59卷引用:2014-2015湖南省娄底市湘中名校高二上学期期末化学(理)试卷
2014-2015湖南省娄底市湘中名校高二上学期期末化学(理)试卷湖南广益实验中学2019-2020学年高二上学期期末考试化学试题(已下线)2009—2010学年存瑞中学第二学期第二阶段考试高二化学试题2015届江西省吉安市白鹭洲中学高三上学期期中化学试卷2015届上海市虹口区高三上学期期末考试化学试卷2014-2015学年福建省晋江市季延中学高二下学期期中考试化学试卷2015-2016学年河北省成安一中高二上学期1月月考化学试卷2015-2016学年黑龙江东部地区高二上学期期末联考化学试卷2015-2016学年广西钦州港经济开发区中学高一上学期期末化学试卷2016-2017学年山东省寿光中学高二上10月月考化学卷2017届宁夏石嘴山三中高三上期中化学试卷2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷内蒙古包头市铁路一中2016-2017学年高二下学期期末考试化学试题山东省寿光现代中学2017-2018学年高二上学期开学考试化学试题河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题河南省安阳市2016-2017学年高二上学期期末考试化学试题青海省西宁市第四高级中学2017-2018学年高二上学期期末考试化学试题山东省德州市2017-2018学年高二上学期期末考试化学试题四川省什邡中学2017-2018学年高二春秋招班第三次月考化学试题云南省腾冲市第八中学2017-2018学年高二下学期期末考试化学试题河南省郑州市第一中学2018-2019学年高二上学期入学测试化学试题高二人教版选修4 第四章 第三节 电解池【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安第四中学2018-2019学年高二上学期12月月考化学试题【校级联考】江西省吉安市几所重点中学2018-2019学年高二上学期联考化学试题【全国百强校】江西省临川第一中学2018-2019学年高二上学期12月月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题【全国百强校】黑龙江省大庆市第一中学2018-2019学年高二下学期第三次阶段考试化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题广东省深圳科学高中2019-2020学年高二上学期开学考试化学试题浙江省宁波市余姚中学2019-2020学年高二上学期期中考试化学试题【全国百强校】上海市复旦大学附属中学2019—2020学年高三上学期期中考试化学试题黑龙江省大庆市第十中学2019-2020学年高二上学期期末考试化学试题陕西省咸阳市2019—2020学年高二上学期期末考试化学试题四川省新津中学2019-2020学年高二下学期4月月考(入学)化学试题江西省上饶市2018-2019学年高二下学期期末教学质量测试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高二上学期开学考试(8月)化学试题宁夏银川市宁夏大学附属中学2021届高三上学期第一次月考化学试题(已下线)【浙江新东方】43山东省泰安市宁阳一中2020-2021学年高二上学期10月学习质量检测化学试题 山东省泰安市宁阳县宁阳一中2020-2021学年高二上学期第一阶段考试化学试题(已下线)【浙江新东方】绍兴qw124安徽省六安市舒城县舒州中学2020-2021学年高二上学期12月月考化学试题福建省宁德第一中学2020-2021学年高二上学期第一次月考化学试题宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】内蒙古北京八中乌兰察布分校2020-2021学年高二上学期期末考试化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期第一次阶段考试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期质量检测月考化学试题安徽省泗县第一中学2021-2022学年高二上学期第二次月考化学试题河北省邢台市第一中学2021-2022学年高二上学期第三次月考化学试题陕西省安康市六校联考2021-2022学年高二上学期期末考试化学试题四川省凉山州2021-2022学年高二上学期期末考试化学试题陕西省西安市西航一中2021-2022学年高二上学期期末考试化学试题(已下线)第29讲 第四章《化学反应与电能》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)辽宁省锦州市黑山县黑山中学2021-2022学年高二上学期12月月考化学试题广东省兴宁市下堡中学2021-2022学年高二上学期期末质量检测化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
7 . 一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
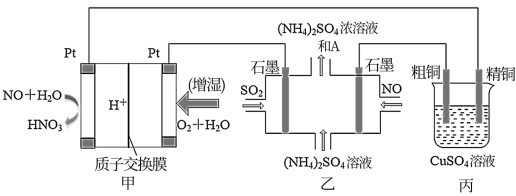
(1)燃料电池放电过程中正极的电极反应式________ 。
(2)乙装置中物质A是________ (填化学式),该装置电解过程阴极的电极反应式________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将________ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有________ mol;丙装置中阴极析出的质量为________ g。
 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
(1)燃料电池放电过程中正极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有
您最近一年使用:0次
2021-01-21更新
|
139次组卷
|
2卷引用:湖南省雅礼中学2020-2021学年高二上学期期中考试化学试题
名校
8 . 某同学用图中装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
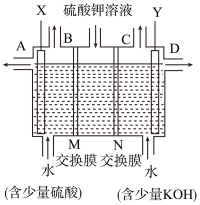
(1)X极与电源的___________ (填“正”或“负”)极相连,氢气从___________ (填“A”“B”“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为___________ (填“阴离子”或“阳离子”,下同)交换膜,N为___________ 交换膜,图中少量硫酸和少量氢氧化钾的作用是___________ 。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为___________ 。
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸___________ mol,负极板质量增加___________ g。

(1)X极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸
您最近一年使用:0次
2021-01-09更新
|
118次组卷
|
4卷引用:湖南省长沙市明德中学2020-2021学年高二上学期第三次月考化学试题
9 . 工业上通过惰性电极电解氯化铵和盐酸的方法来制备二氧化氯,其原理如图所示:

下列说法不正确的是

下列说法不正确的是
| A.工作时a接电源的正极,b接电源的负极 |
| B.工作时Cl-从电解池的左边移到电解池的右边 |
C.a电极反应式为:NH +6e-+3Cl-=NCl3+4H+ +6e-+3Cl-=NCl3+4H+ |
| D.ClO2发生器中发生的反应为:6NaClO2+NCl3+3H2O=NH3↑+6ClO2↑+3NaCl+3NaOH |
您最近一年使用:0次
名校
10 . 磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法治金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有 Al 箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
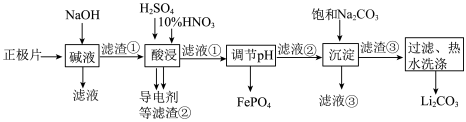
(1)从“正极”可以回收的金属有_______ 。
(2)“碱溶”时 Al 箔溶解的离子方程式为_______ 。
(3)“酸浸”时产生标况下2.24 L NO时,被氧化的LiFePO4为_______ mol(其他杂质不与HNO3反应)。
(4)磷酸亚铁锂电池总反应为:LiFePO4+6C Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向_______ (填“阳极”或“阴极”);放电时,正极反应式为_______ 。
(5)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取 1.40 g 试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入 HgCl2 饱和溶液,用二苯胺磺酸钠作指示剂,用 0.030 mol·L-1 重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00 mL。
已知:2Fe3++Sn2++6Cl-=SnCl +2Fe2+
+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl +Hg2Cl2
+Hg2Cl2
6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O
①实验中加入HgCl2饱和溶液的目的是_______ 。
②磷酸亚铁锂电池中铁的含量为_______ 。

(1)从“正极”可以回收的金属有
(2)“碱溶”时 Al 箔溶解的离子方程式为
(3)“酸浸”时产生标况下2.24 L NO时,被氧化的LiFePO4为
(4)磷酸亚铁锂电池总反应为:LiFePO4+6C
 Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向(5)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取 1.40 g 试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入 HgCl2 饱和溶液,用二苯胺磺酸钠作指示剂,用 0.030 mol·L-1 重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00 mL。
已知:2Fe3++Sn2++6Cl-=SnCl
 +2Fe2+
+2Fe2+4Cl-+Sn2++2HgCl2=SnCl
 +Hg2Cl2
+Hg2Cl26Fe2++Cr2O
 +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O①实验中加入HgCl2饱和溶液的目的是
②磷酸亚铁锂电池中铁的含量为
您最近一年使用:0次



