名校
解题方法
1 . 回答下列问题:
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知N2H4在氧气中完全燃烧生成氮气。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式是_______ ;负极的电极反应式是_______ 。
(2)如图是一个电化学过程示意图。
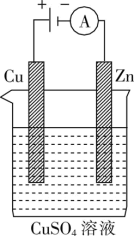
①锌片上发生的电极反应式是_______ 。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量减少128 g,则肼-空气燃料电池理论上消耗标准状况下的空气_______ L(假设空气中的氧气体积含量为20%)。
(3)传统制备肼的方法,以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是_______ 。
(4)工业上为了处理含有Cr2O 的酸性工业废水,采用了下面的处理方法:往工业废水中加入适量的NaCl,以Fe为电极进行电解,经过一段时间后,随着溶液酸性减弱,铁元素和铬元素转化为Cr(OH)3和Fe(OH)3沉淀,工业废水中铬的含量已低于排放标准。请回答下列问题:
的酸性工业废水,采用了下面的处理方法:往工业废水中加入适量的NaCl,以Fe为电极进行电解,经过一段时间后,随着溶液酸性减弱,铁元素和铬元素转化为Cr(OH)3和Fe(OH)3沉淀,工业废水中铬的含量已低于排放标准。请回答下列问题:
①写出两极发生反应的电极反应式:阳极:_______ ;阴极:_______ 。
②写出酸性条件下Cr2O 与Fe2+反应变为Cr3+的离子方程式:
与Fe2+反应变为Cr3+的离子方程式:_______ 。
③该装置_______ (填“能”或“不能”)改用石墨作电极。
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知N2H4在氧气中完全燃烧生成氮气。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式是
(2)如图是一个电化学过程示意图。

①锌片上发生的电极反应式是
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量减少128 g,则肼-空气燃料电池理论上消耗标准状况下的空气
(3)传统制备肼的方法,以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是
(4)工业上为了处理含有Cr2O
 的酸性工业废水,采用了下面的处理方法:往工业废水中加入适量的NaCl,以Fe为电极进行电解,经过一段时间后,随着溶液酸性减弱,铁元素和铬元素转化为Cr(OH)3和Fe(OH)3沉淀,工业废水中铬的含量已低于排放标准。请回答下列问题:
的酸性工业废水,采用了下面的处理方法:往工业废水中加入适量的NaCl,以Fe为电极进行电解,经过一段时间后,随着溶液酸性减弱,铁元素和铬元素转化为Cr(OH)3和Fe(OH)3沉淀,工业废水中铬的含量已低于排放标准。请回答下列问题:①写出两极发生反应的电极反应式:阳极:
②写出酸性条件下Cr2O
 与Fe2+反应变为Cr3+的离子方程式:
与Fe2+反应变为Cr3+的离子方程式:③该装置
您最近一年使用:0次
2 . 烟气的主要污染物为 和
和 ,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
(1)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收 ,反应器II吸收
,反应器II吸收 ,隔绝空气反应一段时间。
,隔绝空气反应一段时间。

①当观察到反应器I中悬浊液变澄清时,反应的离子方程式_______ 。
②反应器II中所发生的反应为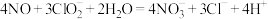 ,盛有
,盛有
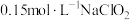 溶液最多能吸收
溶液最多能吸收 (标准状况下)的体积为
(标准状况下)的体积为_______
③已知: 溶液中含氯组分的百分含量(δ)随
溶液中含氯组分的百分含量(δ)随 变化如图1所示,其他条件相同,
变化如图1所示,其他条件相同, 溶液中脱硝效率随溶液初始
溶液中脱硝效率随溶液初始 的变化如图2所示。
的变化如图2所示。
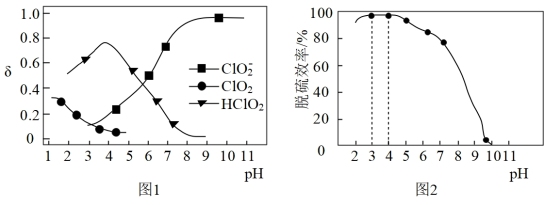
脱硝过程中,起脱硝作用的有效成分为_______ (填化学式)。将NaClO2溶液的pH从4调节至3的过程中,脱硝效率几乎不变的原因是_______ 。
(2)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为_______ 。

 和
和 ,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。(1)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收
 ,反应器II吸收
,反应器II吸收 ,隔绝空气反应一段时间。
,隔绝空气反应一段时间。
①当观察到反应器I中悬浊液变澄清时,反应的离子方程式
②反应器II中所发生的反应为
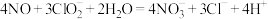 ,盛有
,盛有
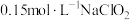 溶液最多能吸收
溶液最多能吸收 (标准状况下)的体积为
(标准状况下)的体积为③已知:
 溶液中含氯组分的百分含量(δ)随
溶液中含氯组分的百分含量(δ)随 变化如图1所示,其他条件相同,
变化如图1所示,其他条件相同, 溶液中脱硝效率随溶液初始
溶液中脱硝效率随溶液初始 的变化如图2所示。
的变化如图2所示。
脱硝过程中,起脱硝作用的有效成分为
(2)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为

您最近一年使用:0次



