解题方法
1 . Ⅰ. 全钒液流电池 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为 放电工作原理。
放电工作原理。
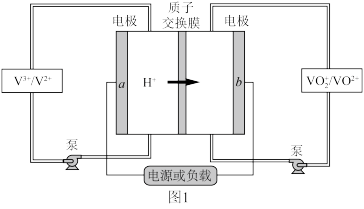
(1)电极 为
为___________ 极(填“正”或“负”),充电时, 电极的反应为
电极的反应为___________ 。
(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。
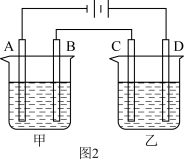
①甲槽是电极电解饱和食盐水的装置,产生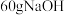 时,
时,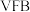 电池中消耗
电池中消耗___________ 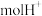 。
。
②乙槽为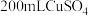 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为___________  。
。
③若通电一段时间后,向所得的乙槽溶液中加入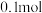 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为___________ (用 表示)。
表示)。
Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有 ,其中
,其中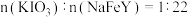 (其中
(其中 显
显 价);
价);
② 。
。
实验步骤:称取 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用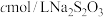 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。
(3)滴定终点的现象为___________ 。
(4)样品中铁元素的质量分数为___________ 。
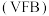 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为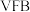 放电工作原理。
放电工作原理。
(1)电极
 为
为 电极的反应为
电极的反应为(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。

①甲槽是电极电解饱和食盐水的装置,产生
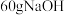 时,
时,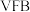 电池中消耗
电池中消耗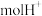 。
。②乙槽为
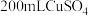 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为 。
。③若通电一段时间后,向所得的乙槽溶液中加入
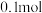 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为 表示)。
表示)。Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有
 ,其中
,其中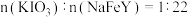 (其中
(其中 显
显 价);
价);②
 。
。实验步骤:称取
 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用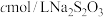 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。(3)滴定终点的现象为
(4)样品中铁元素的质量分数为
您最近半年使用:0次
解题方法
2 . 磷酸亚铁锂( )是制备新型锂离子电池的电极材料。工业以锂辉矿(主要成分为
)是制备新型锂离子电池的电极材料。工业以锂辉矿(主要成分为 ,含少量铁、钙、镁)为原料制备
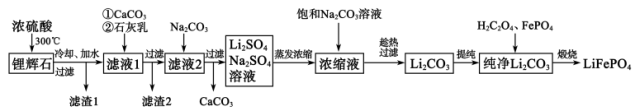
,含少量铁、钙、镁)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①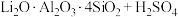 (浓)
(浓)
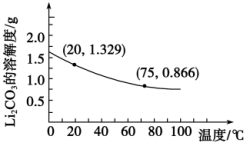
② 的溶解度随温度变化如图所示:
的溶解度随温度变化如图所示:
回答下列问题:
(1)滤渣1的主要成分是____________ ;
(2)向滤液1中加入适量的 细粉用于消耗硫酸并将
细粉用于消耗硫酸并将 转化为红褐色沉淀,若
转化为红褐色沉淀,若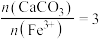 ,反应的离子方程式为
,反应的离子方程式为____________ ;
(3)向浓缩液加入 的目的是沉锂,洗涤所得
的目的是沉锂,洗涤所得 沉淀要使用
沉淀要使用____________ (选填“热水”或“冷水”),你选择的理由是________________________ ;
(4)煅烧制备 时,反应的化学方程式为
时,反应的化学方程式为________________________ ;
(5)用磷酸亚铁锂电池电解精炼银。当负极质量减轻0.7g时,电解精炼得到8.64g银,则电流利用效率为_________ (已知: )
)
(6)用重铬酸钾溶液测定产品 中
中 的含量。原理为:
的含量。原理为: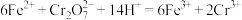
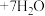 。分别取7.0g试样,用硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.3000
。分别取7.0g试样,用硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.3000 重铬酸钾溶液滴定,溶液由浅绿变为蓝紫,平均消耗重铬酸钾溶液20.00mL。
重铬酸钾溶液滴定,溶液由浅绿变为蓝紫,平均消耗重铬酸钾溶液20.00mL。
①产品中 的质量分数为
的质量分数为____________ 。
②测定结果偏低的原因可能是____________ 。
A.产品在空气中放置时间过长
B.滴定前仰视读数
C.滴定达终点时发现滴定管尖嘴内有气泡生成
D.滴定管没有用标准液润洗
 )是制备新型锂离子电池的电极材料。工业以锂辉矿(主要成分为
)是制备新型锂离子电池的电极材料。工业以锂辉矿(主要成分为 ,含少量铁、钙、镁)为原料制备
,含少量铁、钙、镁)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①
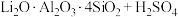 (浓)
(浓)
②
 的溶解度随温度变化如图所示:
的溶解度随温度变化如图所示:
回答下列问题:
(1)滤渣1的主要成分是
(2)向滤液1中加入适量的
 细粉用于消耗硫酸并将
细粉用于消耗硫酸并将 转化为红褐色沉淀,若
转化为红褐色沉淀,若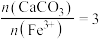 ,反应的离子方程式为
,反应的离子方程式为(3)向浓缩液加入
 的目的是沉锂,洗涤所得
的目的是沉锂,洗涤所得 沉淀要使用
沉淀要使用(4)煅烧制备
 时,反应的化学方程式为
时,反应的化学方程式为(5)用磷酸亚铁锂电池电解精炼银。当负极质量减轻0.7g时,电解精炼得到8.64g银,则电流利用效率为
 )
)(6)用重铬酸钾溶液测定产品
 中
中 的含量。原理为:
的含量。原理为: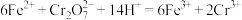
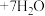 。分别取7.0g试样,用硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.3000
。分别取7.0g试样,用硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.3000 重铬酸钾溶液滴定,溶液由浅绿变为蓝紫,平均消耗重铬酸钾溶液20.00mL。
重铬酸钾溶液滴定,溶液由浅绿变为蓝紫,平均消耗重铬酸钾溶液20.00mL。①产品中
 的质量分数为
的质量分数为②测定结果偏低的原因可能是
A.产品在空气中放置时间过长
B.滴定前仰视读数
C.滴定达终点时发现滴定管尖嘴内有气泡生成
D.滴定管没有用标准液润洗
您最近半年使用:0次
解题方法
3 . 电化学的发展是化学对人类的一项重大贡献。探究原电池和电解池原理,对生产生活具有重要的意义。
(1)利用甲醇燃料电池(甲池)作电源同时电解乙池和丙池。
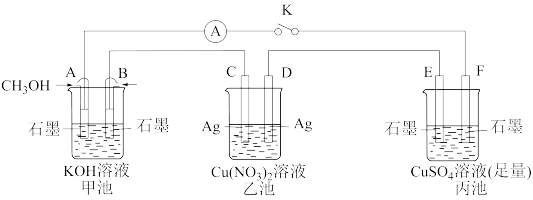
①放电时, 向
向_______ (填“A极”或“B极”)移动; 溶液过量时,甲池中负极的电极反应式为
溶液过量时,甲池中负极的电极反应式为_______ 。
②当乙池中C极质量减轻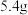 时,甲池中B极理论上消耗
时,甲池中B极理论上消耗 的体积为
的体积为_______  (标准状况)。
(标准状况)。
③一段时间后,断开电键K,欲使丙池恢复到反应前的浓度,可加入的试剂是_______ (填化学式)。
(2)氯碱工业是高耗能产业,将电解池与燃料电池相组合的新工艺可以节能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出所用的离子膜都只允许阳离子通过。

①图中Y是_______ (填化学式);X与 稀溶液反应的离子方程式为
稀溶液反应的离子方程式为_______ 。
②比较图示中氢氧化钠的质量分数a%与b%的大小:_______ 。
③若用装置B作为装置A的辅助电源,则每消耗标准状况下 氧气时,装置B可向装置A提供的电量约为
氧气时,装置B可向装置A提供的电量约为_______ (一个 的电量为
的电量为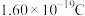 ,计算结果精确到0.01)。
,计算结果精确到0.01)。
(1)利用甲醇燃料电池(甲池)作电源同时电解乙池和丙池。

①放电时,
 向
向 溶液过量时,甲池中负极的电极反应式为
溶液过量时,甲池中负极的电极反应式为②当乙池中C极质量减轻
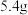 时,甲池中B极理论上消耗
时,甲池中B极理论上消耗 的体积为
的体积为 (标准状况)。
(标准状况)。③一段时间后,断开电键K,欲使丙池恢复到反应前的浓度,可加入的试剂是
(2)氯碱工业是高耗能产业,将电解池与燃料电池相组合的新工艺可以节能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出所用的离子膜都只允许阳离子通过。

①图中Y是
 稀溶液反应的离子方程式为
稀溶液反应的离子方程式为②比较图示中氢氧化钠的质量分数a%与b%的大小:
③若用装置B作为装置A的辅助电源,则每消耗标准状况下
 氧气时,装置B可向装置A提供的电量约为
氧气时,装置B可向装置A提供的电量约为 的电量为
的电量为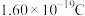 ,计算结果精确到0.01)。
,计算结果精确到0.01)。
您最近半年使用:0次
解题方法
4 . 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5% 溶液、足量
溶液、足量 溶液和100g10%
溶液和100g10% 溶液,a、b、c、d、e、f电极均为石墨电极。
溶液,a、b、c、d、e、f电极均为石墨电极。
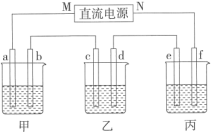
(1)接通电源一段时间后,测得丙中 溶液的质量分数为10.47%,乙中c电极质量增加。
溶液的质量分数为10.47%,乙中c电极质量增加。
①电源的N端为_______ 极;
②电极b上发生的电极反应为_______ ;
③电极b上生成的气体在标准状况下的体积为_______ L;
④电解后丙中溶液的pH_______ (填“增大”“减小”或“不变”)。
(2)乙装置中如果电解过程中铜全部析出,此时电解能否继续进行:_______ (填“能”或“不能”),原因是_______ 。
 溶液、足量
溶液、足量 溶液和100g10%
溶液和100g10% 溶液,a、b、c、d、e、f电极均为石墨电极。
溶液,a、b、c、d、e、f电极均为石墨电极。
(1)接通电源一段时间后,测得丙中
 溶液的质量分数为10.47%,乙中c电极质量增加。
溶液的质量分数为10.47%,乙中c电极质量增加。①电源的N端为
②电极b上发生的电极反应为
③电极b上生成的气体在标准状况下的体积为
④电解后丙中溶液的pH
(2)乙装置中如果电解过程中铜全部析出,此时电解能否继续进行:
您最近半年使用:0次
20-21高二上·重庆巫溪·阶段练习
名校
解题方法
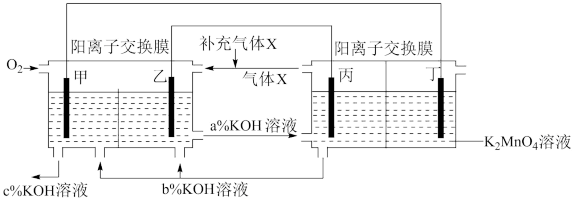
5 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为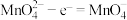 |
C.KOH溶液的质量分数: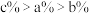 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近半年使用:0次
2022-05-29更新
|
663次组卷
|
7卷引用:卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)
名校
6 . I.某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
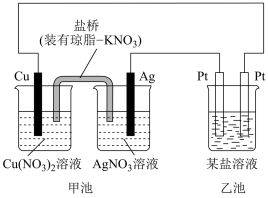
(1)甲池装置为_______ (填“原电池”或“电解池”)。
(2)甲池反应前两电极质量相等,一段时间后,两电极质量相差14g,导线中通过_______ mol电子。
(3)实验过程中,甲池左侧烧杯中 的浓度
的浓度_______ (填“增大”、“减小”或“不变”)。
(4)若乙池中溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中加入_______ 。(填化学式)
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。
II.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是_______ 。
(7)图中Y是_______ (填化学式),若电解产生11.2L(标准状况)该物质,则至少转移电子_______ mol;
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

(1)甲池装置为
(2)甲池反应前两电极质量相等,一段时间后,两电极质量相差14g,导线中通过
(3)实验过程中,甲池左侧烧杯中
 的浓度
的浓度(4)若乙池中溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中加入
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为
 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。| A.电解过程中,阳极减少的质量与阴极增加的质量相等 |
| B.乙池左侧电极为粗铜,发生氧化反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 |
| D.杂质都将以单质的形式沉淀到池底 |
II.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是
(7)图中Y是
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近半年使用:0次
解题方法
7 . 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上,并同时制得 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
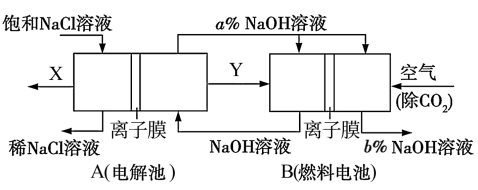
请回答下列问题:
(1)A池总反应的离子反应方程式为___________ 。燃料电池B中正极上发生的电极反应式为___________ 。
(2)装置中的离子膜是阳离子交换膜,当阴极产生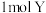 时,通过离子交换膜的
时,通过离子交换膜的 有
有___________  。
。
(3)装置图中氢氧化钠溶液质量分数的大小:
___________ 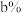 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
 和
和 溶液。相关物料的传输与转化关系如图所示:
溶液。相关物料的传输与转化关系如图所示:
请回答下列问题:
(1)A池总反应的离子反应方程式为
(2)装置中的离子膜是阳离子交换膜,当阴极产生
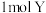 时,通过离子交换膜的
时,通过离子交换膜的 有
有 。
。(3)装置图中氢氧化钠溶液质量分数的大小:

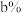 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
您最近半年使用:0次
解题方法
8 . 氯碱工业是高耗能产业,按下图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示(电极末标出),下列说法正确的是
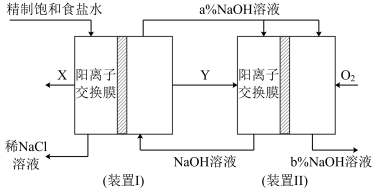

| A.图中装置I属于原电池 |
| B.X是氯气 |
C.Y在装置II中发生的电极反应为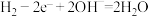 |
D.图中氢氧化钠质量分数大小关系为 |
您最近半年使用:0次
名校
解题方法
9 . 降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
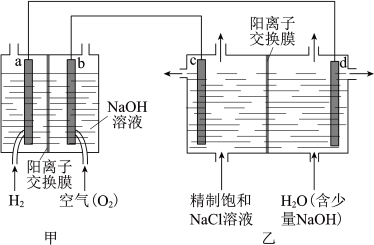
① 极为
极为_____ (填“正”或“负”)极。
②乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_____ 。
③下列说法正确的是_____ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动
C.乙装置中 极一侧流出的是淡盐水
极一侧流出的是淡盐水
④结合化学用语解释 极区产生
极区产生 的原因:
的原因:_____ 。
⑤实际生产中,阳离子交换膜的损伤会造成 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为_____ 。下列生产措施有利于提高 产量、降低阳极
产量、降低阳极 含量的是
含量的是_____ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_____ 。
(1)我国利用氯碱厂生产的
 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
①
 极为
极为②乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中
 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动C.乙装置中
 极一侧流出的是淡盐水
极一侧流出的是淡盐水④结合化学用语解释
 极区产生
极区产生 的原因:
的原因:⑤实际生产中,阳离子交换膜的损伤会造成
 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为 产量、降低阳极
产量、降低阳极 含量的是
含量的是A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用
 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入
 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近半年使用:0次
2023-10-01更新
|
48次组卷
|
3卷引用:北京市北京医学院附属中学2022-2023学年高二上学期期中考试化学试题
解题方法
10 . 氯碱工业是高能耗产业,节能技术的研发是当前的重要课题。
(1)一种节能技术是将电解池与燃料电池相组合,相关物料传输与转化关系如下图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。
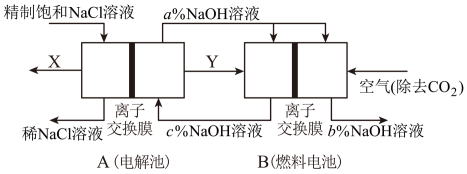
①当产生0.5molX时,A中通过离子交换膜的Na+有___________ mol。
②写出燃料电池B中负极上的电极反应式___________ 。
③比较图中NaOH质量分数a%、b%、c%由大到小的顺序___________ 。
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应式为___________ 。
(1)一种节能技术是将电解池与燃料电池相组合,相关物料传输与转化关系如下图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。

①当产生0.5molX时,A中通过离子交换膜的Na+有
②写出燃料电池B中负极上的电极反应式
③比较图中NaOH质量分数a%、b%、c%由大到小的顺序
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应式为
您最近半年使用:0次
2022-01-16更新
|
256次组卷
|
2卷引用:浙江省嘉兴市2021-2022学年高二上学期期末检测化学试题



