名校
1 . CO2的资源化利用不仅可以减少CO2的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:
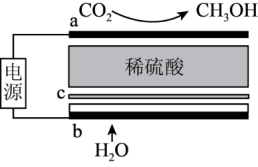
(1)a电极与电源的_______ 极相连,其中c为质子交换膜,写出b电极的电极反应式_______ 。
II. 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
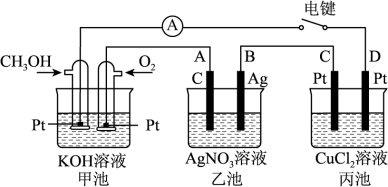
请回答下列问题:
(2)通入CH3OH电极的电极反应式为_______ 。
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出_______ gAg。
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后_______ (填C或D)极首先变红,写出电解时总离子反应式_______ 。
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
则CH4—CO2催化重整反应的ΔH=_______ kJ·mol-1。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:

(1)a电极与电源的
II.
 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入CH3OH电极的电极反应式为
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
| 物质 | CH4(g) | CO(g) | H2(g) |
| 燃烧热(ΔH/kJ·mol-1) | -890.3 | -283.0 | -285.8 |
您最近半年使用:0次
名校
解题方法
2 .  的资源化利用不仅可以减少
的资源化利用不仅可以减少 的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
Ⅰ.科学家致力于 电催化合成甲醇的研究,其工作原理如图:
电催化合成甲醇的研究,其工作原理如图:
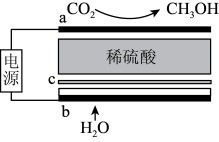
(1)b电极与电源的_______ 极相连,其中c为质子交换膜,写出a电极的电极反应式_______
Ⅱ. 燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
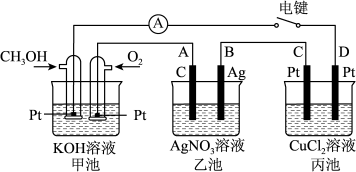
请回答下列问题:
(2)通入 电极的电极反应式为
电极的电极反应式为_______ 。
(3)当丙池某个电极增重38.4g时,乙池中收集到了标况下11.2L气体。则甲池中理论上消耗 的物质的量为
的物质的量为_______ mol,乙池中析出_______ gAg。
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后_______ (C或D)极首先变红,写出电解时总离子反应式_______
 的资源化利用不仅可以减少
的资源化利用不仅可以减少 的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。Ⅰ.科学家致力于
 电催化合成甲醇的研究,其工作原理如图:
电催化合成甲醇的研究,其工作原理如图:
(1)b电极与电源的
Ⅱ.
 燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入
 电极的电极反应式为
电极的电极反应式为(3)当丙池某个电极增重38.4g时,乙池中收集到了标况下11.2L气体。则甲池中理论上消耗
 的物质的量为
的物质的量为(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后
您最近半年使用:0次
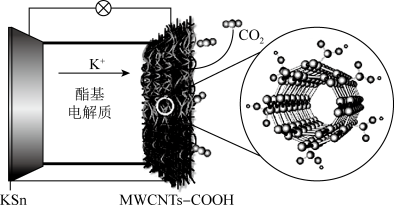
3 . 我国科研团队以聚氨酯为电解液(合成路线如图)实现了稳定高效且可遵循环的K— 电池。总反应为:
电池。总反应为: ,其中生成的
,其中生成的 附着在正极上。下列说法错误的是
附着在正极上。下列说法错误的是
 电池。总反应为:
电池。总反应为: ,其中生成的
,其中生成的 附着在正极上。下列说法错误的是
附着在正极上。下列说法错误的是
| A.放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管 |
B.电池的正极反应式为 |
| C.羧基化碳纳米管中引入的羧基可促进电子的转移 |
| D.充电时,电路中通过1mol电子,多壁碳纳米管减重36g |
您最近半年使用:0次
名校
4 . 我国科技工作者设计以CoP和Ni2P纳米片为催化电极材料,电催化合成偶氮化合物的新装置如图所示,下列说法正确的是
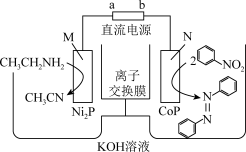

| A.电极a的电势低于b极 |
| B.该离子交换膜是阴离子交换膜 |
| C.M极的电极反应式为CH3CH2NH2+4e- +4OH-=CH3CN+4H2O |
| D.电子由直流电源出发,经电极b, KOH溶液,电极a回到直流电源 |
您最近半年使用:0次
名校
5 . 温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将CO2应用于生产中实现其综合利用是目前的研究热点。
I.在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。
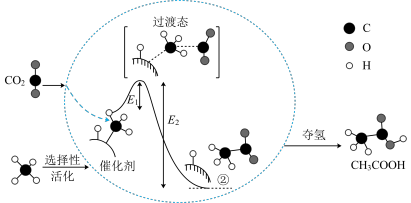
(1)在合成CH3COOH的反应历程中,下列有关说法正确的是_______(填字母)。
II.以CO2、H2为原料制备“21世纪的清洁燃料”二甲醚(CH3OCH3)涉及的主要反应如下:
①2CO2(g)+6 H2(g) CH3OCH3(g)+3H2O(g) ΔH1= -122.5kJ·mol-1。
CH3OCH3(g)+3H2O(g) ΔH1= -122.5kJ·mol-1。
②CO2(g)+ H2(g) CO (g)+ H2O(g) ΔH2 = +41.1kJ·mol-1。
CO (g)+ H2O(g) ΔH2 = +41.1kJ·mol-1。
(2)反应2CO(g)+4 H2(g) CH3OCH3(g)+ H2O(g) 的 ΔH=
CH3OCH3(g)+ H2O(g) 的 ΔH=_______ ;
(3)在压强、CO2和H2的起始投料一定的条件下,发生反应①、②,实验测得CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。
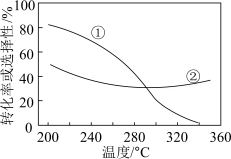
i.已知:CH3OCH3的选择性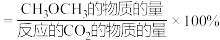 ,其中表示平衡时CH3OCH3的选择性的是曲线
,其中表示平衡时CH3OCH3的选择性的是曲线_______ (填“①”或“②”,下同);温度高于300℃时,曲线②随温度升高而升高的原因是高于300℃时,以反应_______ 为主,温度升高平衡正向移动,CO2的平衡转化增大。
ii.为同时提高CO2的平衡转化率和平衡时CH3OCH3的选择性,应选择的反应条件为_______ (填标号)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
III.以CO2、C2H6为原料合成的主要反应为:CO2(g) + C2H6(g) C2H4(g) + H2O(g)+CO(g) ΔH1= +177kJ·mol-1。
C2H4(g) + H2O(g)+CO(g) ΔH1= +177kJ·mol-1。
(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=_______ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
IV.以稀硫酸为电解质溶液,由甲醇(CH3OH)、O2构成的原电池作为电解饱和食盐水的电源(电解池中左右两室均为1L的NaCl溶液)。
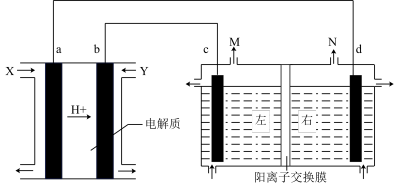
(5)a电极的电极反应式为_______ 。电解饱和食盐水装置溶液中的阳离子由_______ (填“左向右”或“右向左”)移动,
(6)室温下,当电解池中共产生224mL(已折算成标况下,不考虑气体溶解损失)气体时,右室溶液(体积变化忽略不计)的pH为_______ 。
I.在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。

(1)在合成CH3COOH的反应历程中,下列有关说法正确的是_______(填字母)。
| A.该催化剂使反应的平衡常数增大 |
| B.CH4 →CH3COOH过程中,有C-H键断裂和C-C键形成 |
| C.生成乙酸的反应原子利用率100% |
| D.ΔH =E2-E1 |
II.以CO2、H2为原料制备“21世纪的清洁燃料”二甲醚(CH3OCH3)涉及的主要反应如下:
①2CO2(g)+6 H2(g)
 CH3OCH3(g)+3H2O(g) ΔH1= -122.5kJ·mol-1。
CH3OCH3(g)+3H2O(g) ΔH1= -122.5kJ·mol-1。②CO2(g)+ H2(g)
 CO (g)+ H2O(g) ΔH2 = +41.1kJ·mol-1。
CO (g)+ H2O(g) ΔH2 = +41.1kJ·mol-1。(2)反应2CO(g)+4 H2(g)
 CH3OCH3(g)+ H2O(g) 的 ΔH=
CH3OCH3(g)+ H2O(g) 的 ΔH=(3)在压强、CO2和H2的起始投料一定的条件下,发生反应①、②,实验测得CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。

i.已知:CH3OCH3的选择性
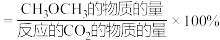 ,其中表示平衡时CH3OCH3的选择性的是曲线
,其中表示平衡时CH3OCH3的选择性的是曲线ii.为同时提高CO2的平衡转化率和平衡时CH3OCH3的选择性,应选择的反应条件为
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
III.以CO2、C2H6为原料合成的主要反应为:CO2(g) + C2H6(g)
 C2H4(g) + H2O(g)+CO(g) ΔH1= +177kJ·mol-1。
C2H4(g) + H2O(g)+CO(g) ΔH1= +177kJ·mol-1。(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6达到平衡时C2H4的物质的量分数为20%,该温度下反应的平衡常数Kp=
IV.以稀硫酸为电解质溶液,由甲醇(CH3OH)、O2构成的原电池作为电解饱和食盐水的电源(电解池中左右两室均为1L的NaCl溶液)。

(5)a电极的电极反应式为
(6)室温下,当电解池中共产生224mL(已折算成标况下,不考虑气体溶解损失)气体时,右室溶液(体积变化忽略不计)的pH为
您最近半年使用:0次
名校
解题方法
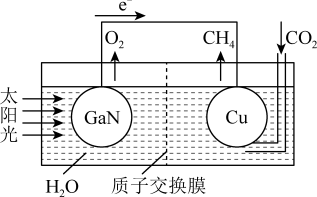
6 . 科学家用氮化镓材料与铜组装成如图的人工光合系统,实现了以 和
和 为原料合成
为原料合成 。下列有关说法不正确的是
。下列有关说法不正确的是
 和
和 为原料合成
为原料合成 。下列有关说法不正确的是
。下列有关说法不正确的是
| A.该装置是先将光能转化为电能,再将电能转化为化学能 |
B.氮化镓电极表面的电极反应式为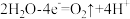 |
C.铜电极表面的 和 和 放电,生成 放电,生成 ,则铜电极是负极 ,则铜电极是负极 |
| D.该装置的电解液不能用盐酸,而用硫酸 |
您最近半年使用:0次
2022-02-16更新
|
120次组卷
|
2卷引用:湖南省名校联考联合体2021-2022学年高二上学期期末考试化学试题



