Ⅰ. 全钒液流电池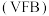 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为 放电工作原理。
放电工作原理。
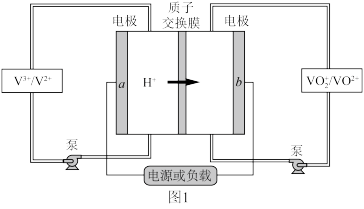
(1)电极 为
为___________ 极(填“正”或“负”),充电时, 电极的反应为
电极的反应为___________ 。
(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。
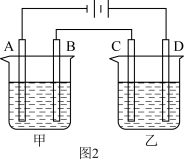
①甲槽是电极电解饱和食盐水的装置,产生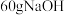 时,
时,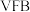 电池中消耗
电池中消耗___________ 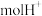 。
。
②乙槽为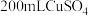 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为___________  。
。
③若通电一段时间后,向所得的乙槽溶液中加入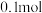 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为___________ (用 表示)。
表示)。
Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有 ,其中
,其中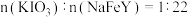 (其中
(其中 显
显 价);
价);
② 。
。
实验步骤:称取 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用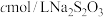 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。
(3)滴定终点的现象为___________ 。
(4)样品中铁元素的质量分数为___________ 。
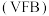 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为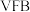 放电工作原理。
放电工作原理。
(1)电极
 为
为 电极的反应为
电极的反应为(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。

①甲槽是电极电解饱和食盐水的装置,产生
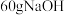 时,
时,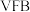 电池中消耗
电池中消耗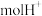 。
。②乙槽为
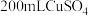 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为 。
。③若通电一段时间后,向所得的乙槽溶液中加入
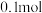 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为 表示)。
表示)。Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有
 ,其中
,其中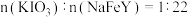 (其中
(其中 显
显 价);
价);②
 。
。实验步骤:称取
 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用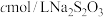 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。(3)滴定终点的现象为
(4)样品中铁元素的质量分数为
更新时间:2024-02-14 22:29:32
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池为_______ (填“原电池”或“电解池”),A电极的电极反应式为_______ 。
(2)丙池中E电极为_______ (填“正极”、“负极”、“阴极”或“阳极”),丙池总反应的离子方程式为_______ 。
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的物质的量为_______ mol
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______(填选项字母)。
(5)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
此装置中爱迪生蓄电池的正极是_______ (填“a”或“b”),该电池工作一段时间后必须充电,充电时阴极的电极反应式为_______ 。


(1)甲池为
(2)丙池中E电极为
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的物质的量为
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
 Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。此装置中爱迪生蓄电池的正极是

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】已知下列热化学为程式:
① Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H1=﹣25 kJ·mol-1
② 3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) △H2=﹣47 kJ·mol-1
③ Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) △H3=﹢19 kJ·mol-1
(1)写出 FeO(s)被CO还原成Fe和CO2的热化学方程式_______ 。
(2)常温常压下,一定量C2H5OH燃烧生成气态CO2和液态水时放出136.7kJ热量,将燃烧产物通入足量澄清石灰水生成20克沉淀,表示该反应的热化学方程式为_______ 。
(3)如图是乙醇燃料电池工作时的示意图,甲池使用Pt作电极材料,乙池中的两个电极一个是石墨,一个是铁,工作时M、N两个电极的质量都不减少,回答下列问题:

①乙池为_______ 装置,M的电极材料是_______ ,N为_______ 极,电极反应式为_______ ,甲池通入氧气的一端为_______ 极,通乙醇的电极上发生的电极反应式为_______ 。
②工作中当电路中通过0.04mol电子时,甲池中理论上消耗氧气_______ L(STP),乙池中的M极会得到 _______ (写出生成物质的名称及质量)。
① Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H1=﹣25 kJ·mol-1
② 3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) △H2=﹣47 kJ·mol-1
③ Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) △H3=﹢19 kJ·mol-1
(1)写出 FeO(s)被CO还原成Fe和CO2的热化学方程式
(2)常温常压下,一定量C2H5OH燃烧生成气态CO2和液态水时放出136.7kJ热量,将燃烧产物通入足量澄清石灰水生成20克沉淀,表示该反应的热化学方程式为
(3)如图是乙醇燃料电池工作时的示意图,甲池使用Pt作电极材料,乙池中的两个电极一个是石墨,一个是铁,工作时M、N两个电极的质量都不减少,回答下列问题:

①乙池为
②工作中当电路中通过0.04mol电子时,甲池中理论上消耗氧气
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。

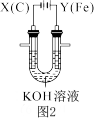
请回答:
用图1所示装置进行第一组实验(K闭合)
(1)Zn极为___ 极。实验过程中,甲中SO
___ (填“从左向右”、“从右问左”或“不”)移动;反应初期乙中N极发生的电极反应为____ 。
(2)反应一段时间后,打开K,向乙中加入0.1molCu(OH)2后恰好复原,则上述电解过程中转移的电子数为___ 。
(3)用图2所示装置进行第二组实验,实验中Y极区产生FeO ,溶液呈浅紫红色。Y极上的电极反应式为
,溶液呈浅紫红色。Y极上的电极反应式为___ 。
(4)电解过程中、X极区溶液的pH___ (填“增大”、“减小”或“不变”)。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应式为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO4,该电池正极发生的电极反应式为___ 。

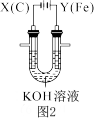
请回答:
用图1所示装置进行第一组实验(K闭合)
(1)Zn极为

(2)反应一段时间后,打开K,向乙中加入0.1molCu(OH)2后恰好复原,则上述电解过程中转移的电子数为
(3)用图2所示装置进行第二组实验,实验中Y极区产生FeO
 ,溶液呈浅紫红色。Y极上的电极反应式为
,溶液呈浅紫红色。Y极上的电极反应式为(4)电解过程中、X极区溶液的pH
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应式为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO4,该电池正极发生的电极反应式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某课外活动小组用如图所示装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则A极的电极反应式为___________ 。
(2)若开始时开关K与b极连接,则B极的电极反应式为___________ ,总反应的离子方程式为___________ 。
(3)若开始时开关K与b连接,下列说法正确的是___________  填字母
填字母 。
。
A.溶液中Cl-向B极移动。
B.该装置中电流的方向是:电源正极→石墨→饱和食盐水→ 铁。
C.反应一段时间后(食盐水的浓度足够大),加适量盐酸可恢复到电解前电解质溶液的浓度。
D.从A极处逸出的气体能使湿润的 淀粉试纸变蓝,但一段时间后蓝色褪去。
淀粉试纸变蓝,但一段时间后蓝色褪去。
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
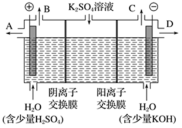
①该电解槽的阳极反应式为___________ 。
②制得的H2SO4溶液从出口___________  填“A”“B”“C”或“D”
填“A”“B”“C”或“D” 导出。
导出。
③在C出口收集到6.72 L(标况)的气体,则能制得___________ mol 的硫酸。

(1)若开始时开关K与a连接,则A极的电极反应式为
(2)若开始时开关K与b极连接,则B极的电极反应式为
(3)若开始时开关K与b连接,下列说法正确的是
 填字母
填字母 。
。A.溶液中Cl-向B极移动。
B.该装置中电流的方向是:电源正极→石墨→饱和食盐水→ 铁。
C.反应一段时间后(食盐水的浓度足够大),加适量盐酸可恢复到电解前电解质溶液的浓度。
D.从A极处逸出的气体能使湿润的
 淀粉试纸变蓝,但一段时间后蓝色褪去。
淀粉试纸变蓝,但一段时间后蓝色褪去。(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为
②制得的H2SO4溶液从出口
 填“A”“B”“C”或“D”
填“A”“B”“C”或“D” 导出。
导出。③在C出口收集到6.72 L(标况)的气体,则能制得
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】如下图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。
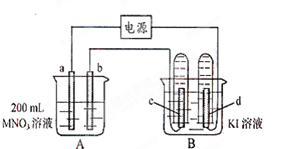
试回答:
(1)a为____ 极,c极的电极反应式为:_____________________________ 。
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现是____________ 。电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为:______________ 。
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了____ mol气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_______________ ;若要使A池中溶液恢复原浓度,应加_____________ 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3溶液的物质的量浓度为_______________ mol·L-1。

试回答:
(1)a为
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现是
(3)当d电极上收集到44.8 ml气体(标准状况)时停止电解,a极上放出了
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200 ml,取这种溶液加入到25.0 ml 0.100 mol·L-1的HCl溶液中,当加入31.25 ml 溶液时刚好沉淀完全。由此可知电解前A烧杯中MNO3溶液的物质的量浓度为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】碳氮及其化合物广泛存在于自然界中。
Ⅰ、(l)化学家Gethard Ertl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意如图:
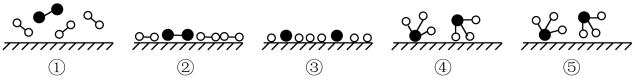
下列说法正确的是___________ (选填字母)。
A.①表示N2、H2分子中均是单键
B.②→③需要吸收能量
C.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(2)氨气分解反应的热化学方程式如下:2NH3(g)⇌N2(g)+3H2(g) △H。若:N≡N键、H-H键和N-H键的键能分别记作a、b和c(单位:kJ•mol﹣l),则上述反应的△H=___________ kJ•mol﹣1。
Ⅱ、(1)CO与H2在一定条件下可反应生成甲醇:CO(g)+2H2(g)=CH3OH(g)。以KOH溶液为电解质溶液,甲醇、空气构成的原电池(图2)作图3的电源,电极M与___________ (填“X”或“Y”)极相连,N极的电极反应式为___________ 。
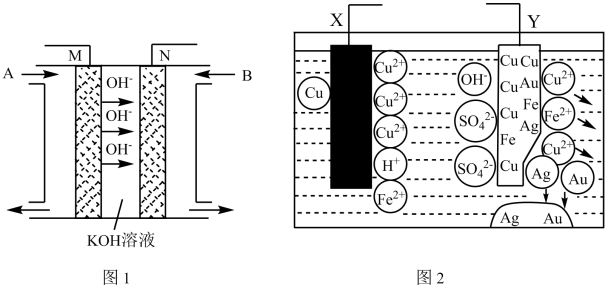
(2)若用图2燃料电池,以惰性电极电解100 mL 0.5 mol/L CuSO4溶液,阳极产生56 mL 标况下气体时,所得溶液的pH 为___________ (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入___________ (填序号)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
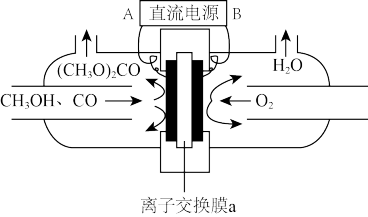
(3)以甲醇和CO为原料通过电化学合成碳酸二甲酯的工作原理如图所示。离子交换膜a为___________ (填“阳膜”或“阴膜”),阳极的电极反应式为___________ 。
Ⅰ、(l)化学家Gethard Ertl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意如图:

下列说法正确的是
A.①表示N2、H2分子中均是单键
B.②→③需要吸收能量
C.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(2)氨气分解反应的热化学方程式如下:2NH3(g)⇌N2(g)+3H2(g) △H。若:N≡N键、H-H键和N-H键的键能分别记作a、b和c(单位:kJ•mol﹣l),则上述反应的△H=
Ⅱ、(1)CO与H2在一定条件下可反应生成甲醇:CO(g)+2H2(g)=CH3OH(g)。以KOH溶液为电解质溶液,甲醇、空气构成的原电池(图2)作图3的电源,电极M与

(2)若用图2燃料电池,以惰性电极电解100 mL 0.5 mol/L CuSO4溶液,阳极产生56 mL 标况下气体时,所得溶液的pH 为
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(3)以甲醇和CO为原料通过电化学合成碳酸二甲酯的工作原理如图所示。离子交换膜a为

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:_______ 。
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是_______ 。
(3)“转化”在图所示的装置中进行。导管A的作用是_______ 。_______ 。
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度_______ (写出计算过程)。
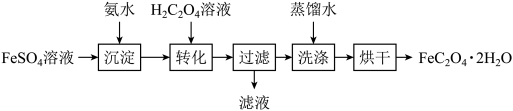
(2)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(3)“转化”在图所示的装置中进行。导管A的作用是
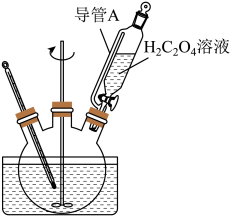
(5)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓H2SO4、磷酸,用0.04500mol·L-1KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00mL。计算样品中FeC2O4·2H2O的纯度
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。

(1)黄铁矿中硫元素的化合价为_______ 。
(2)由炉渣制备还原铁粉的化学方程式为_______ 。
(3)欲得到更纯的NaHSO3,反应①应通入_______ (填 “过量”或“不足量”)的气体。
(4)因为Na2S2O5具有_______ 性, 长期放置会导致商品Na2S2O5中不可避免地存在_______ 杂质,检验杂质的方法是_______ 。
(5)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的亚铁离子,反应离子方程式如下 。
。
某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为_______ %(精确到小数点后两位)。(假设杂质中无铁元素,杂质也不与标准重铬酸钾溶液反应,铁的相对原子质量为56)

(1)黄铁矿中硫元素的化合价为
(2)由炉渣制备还原铁粉的化学方程式为
(3)欲得到更纯的NaHSO3,反应①应通入
(4)因为Na2S2O5具有
(5)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的亚铁离子,反应离子方程式如下
 。
。某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)仪器A的名称为_______ 。
(2)ClO2可将废水中的CN-氧化成CO2和N2,该反应的离子方程式是_______ 。
(3)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2.某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。
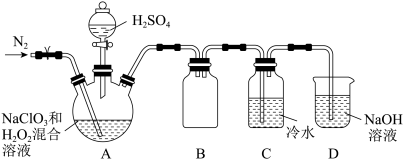
①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是_______ 。
②装置B的作用是_______ 。
③装置A用于生成ClO2气体,该反应的化学方程式是_______ 。
(4)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入_______ 作指示剂,用0.1000mol•L-1的Na2S2O3标准液滴定锥形瓶中的溶液(I2+2 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是_______ ,C中ClO2溶液的浓度是_______ mol•L-1。
(1)仪器A的名称为
(2)ClO2可将废水中的CN-氧化成CO2和N2,该反应的离子方程式是
(3)根据文献资料,用NaClO3和双氧水在酸性条件下可制得ClO2.某小组按照文献中制备ClO2的方法设计了如图所示的实验装置用于制备ClO2。

①通入氮气的主要作用有2个,一是可以起到搅拌作用,二是
②装置B的作用是
③装置A用于生成ClO2气体,该反应的化学方程式是
(4)测定装置C中ClO2溶液的浓度:取10.00mLC中溶液于锥形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入
 =2I-+
=2I-+ ),消耗标准溶液的体积为20.00mL。滴定终点的现象是
),消耗标准溶液的体积为20.00mL。滴定终点的现象是
您最近半年使用:0次



