解题方法
1 . 四乙氧基硅烷Si(OC2H5)4具有广泛工业用途。某小组用SiCl4和C2H5OH反应制备Si(OC2H5)4,并探究影响产率的因素。相关物质的沸点和水解性如下:
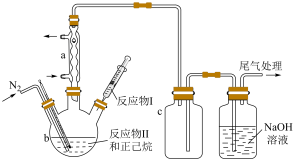
实验装置示意简图如图所示(加热及夹持装置略)。
(1)制备Si(OC2H5)4
①仪器a的名称是___________ ;c瓶的作用是___________ 。
②b中生成Si(OC2H5)4的化学方程式为___________ 。
③反应过程中有H2O和C2H5Cl生成,但混合物中未检出H2O的原因是___________ ;滤液质谱图中也无C2H5Cl的特征峰的原因是___________ 。
④当馏出液为产品时,蒸馏温度应控制在___________ ℃。
(2)影响产率的因素
①控制变量法可用于探究影响产率的因素,在设计实验时需要考虑的变量有___________ 。
A.反应温度 B.溶剂类型 C.加料顺序 D.滴加速率
②N2流速对产率也有影响,随着N2流速增大,产率先增大后减小,主要原因是___________ 。
| 物质 | SiCl4 | C2H5OH | Si(OC2H5)4 | 正己烷 | C2H5Cl |
| 沸点/℃ | 58 | 78 | 168 | 68 | 12 |
| 水解性 | 易水解 | — | 易水解 | 一 | — |
(1)制备Si(OC2H5)4
①仪器a的名称是
②b中生成Si(OC2H5)4的化学方程式为
③反应过程中有H2O和C2H5Cl生成,但混合物中未检出H2O的原因是
④当馏出液为产品时,蒸馏温度应控制在
(2)影响产率的因素
①控制变量法可用于探究影响产率的因素,在设计实验时需要考虑的变量有
A.反应温度 B.溶剂类型 C.加料顺序 D.滴加速率
②N2流速对产率也有影响,随着N2流速增大,产率先增大后减小,主要原因是
您最近一年使用:0次
2 . 氨的制备是当前研究的重要课题。
(1)CH4、N2偶联活化制NH3。研究发现,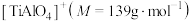 可以活化CH4,为合成氨提供活性氢原子。
可以活化CH4,为合成氨提供活性氢原子。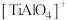 暴露在CH4中,反应产生微粒有
暴露在CH4中,反应产生微粒有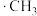 、
、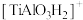 、
、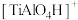 、
、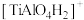 、
、 。实验过程中的质谱图如图1所示。图中质荷比为125对应的微粒为
。实验过程中的质谱图如图1所示。图中质荷比为125对应的微粒为___________ ,生成该微粒的同时,还生成___________ 。
②为探究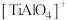 活化CH4的反应过程,研究人员从反应体系中不断去除
活化CH4的反应过程,研究人员从反应体系中不断去除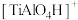 ,得到的质谱图如图2所示。
,得到的质谱图如图2所示。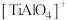 与CH4反应生成|
与CH4反应生成|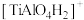 的过程可描述为
的过程可描述为___________ 。
③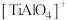 活化CH4后,产生活性H原子与N2反应生成NH3.活化过程中生成多种副产物导致NH3的选择性较低,其中不含非极性键的含氮副产物分子可能有
活化CH4后,产生活性H原子与N2反应生成NH3.活化过程中生成多种副产物导致NH3的选择性较低,其中不含非极性键的含氮副产物分子可能有___________ (写两种)。
(2)电催化还原N2制NH3。在碱性水溶液中,通过电催化使N2还原为NH3的电极反应式为___________ 。该制氨方法尚未能应用于工业生产,除因为N2的溶解度低、难吸附在电极和催化剂表面外,还有___________ 。
(3)电催化还原 制NH3。NF是一种电极载体,分别以Ni2P/NF、Fe/NF、NF为阴极材料,电解含
制NH3。NF是一种电极载体,分别以Ni2P/NF、Fe/NF、NF为阴极材料,电解含 的中性溶液(电极材料与溶液不发生反应)。控制电压恒定、催化剂的面积为0.25cm2,电解2小时后,不同电极上NH3的产率及NH3的选择性如图3所示。
的中性溶液(电极材料与溶液不发生反应)。控制电压恒定、催化剂的面积为0.25cm2,电解2小时后,不同电极上NH3的产率及NH3的选择性如图3所示。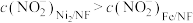 ,原因是
,原因是___________ 。
②已知:NH3的产率=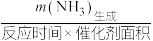 ;NH3的选择性
;NH3的选择性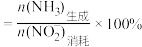 。以Ni2P/NF为电极电解NaNO2溶液2小时,消耗
。以Ni2P/NF为电极电解NaNO2溶液2小时,消耗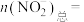
___________ mol。
(1)CH4、N2偶联活化制NH3。研究发现,
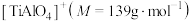 可以活化CH4,为合成氨提供活性氢原子。
可以活化CH4,为合成氨提供活性氢原子。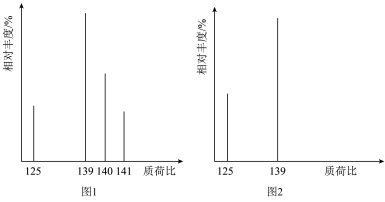
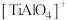 暴露在CH4中,反应产生微粒有
暴露在CH4中,反应产生微粒有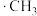 、
、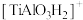 、
、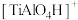 、
、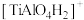 、
、 。实验过程中的质谱图如图1所示。图中质荷比为125对应的微粒为
。实验过程中的质谱图如图1所示。图中质荷比为125对应的微粒为②为探究
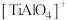 活化CH4的反应过程,研究人员从反应体系中不断去除
活化CH4的反应过程,研究人员从反应体系中不断去除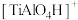 ,得到的质谱图如图2所示。
,得到的质谱图如图2所示。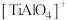 与CH4反应生成|
与CH4反应生成|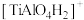 的过程可描述为
的过程可描述为③
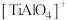 活化CH4后,产生活性H原子与N2反应生成NH3.活化过程中生成多种副产物导致NH3的选择性较低,其中不含非极性键的含氮副产物分子可能有
活化CH4后,产生活性H原子与N2反应生成NH3.活化过程中生成多种副产物导致NH3的选择性较低,其中不含非极性键的含氮副产物分子可能有(2)电催化还原N2制NH3。在碱性水溶液中,通过电催化使N2还原为NH3的电极反应式为
(3)电催化还原
 制NH3。NF是一种电极载体,分别以Ni2P/NF、Fe/NF、NF为阴极材料,电解含
制NH3。NF是一种电极载体,分别以Ni2P/NF、Fe/NF、NF为阴极材料,电解含 的中性溶液(电极材料与溶液不发生反应)。控制电压恒定、催化剂的面积为0.25cm2,电解2小时后,不同电极上NH3的产率及NH3的选择性如图3所示。
的中性溶液(电极材料与溶液不发生反应)。控制电压恒定、催化剂的面积为0.25cm2,电解2小时后,不同电极上NH3的产率及NH3的选择性如图3所示。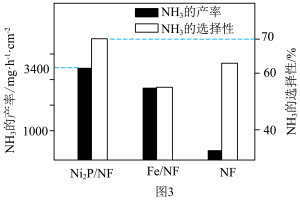
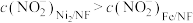 ,原因是
,原因是②已知:NH3的产率=
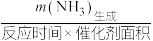 ;NH3的选择性
;NH3的选择性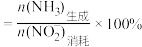 。以Ni2P/NF为电极电解NaNO2溶液2小时,消耗
。以Ni2P/NF为电极电解NaNO2溶液2小时,消耗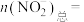
您最近一年使用:0次
解题方法
3 . 开瑞坦是一种重要的脱敏药物,可用于治疗过敏性鼻炎、荨麻疹等各类过敏性疾病。开瑞坦的前体K的合成路线如下: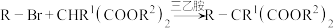
_________ 。
(2)B中含有 ,试剂a是
,试剂a是_________ 。
(3)D的结构简式是_________ 。
(4)E→F中,反应i的化学方程式为_________ 。
(5)下列关于有机物F和G的说法正确的是_________ (填字母)。
a.F和G均没有手性碳原子
b.F和G均能与 反应
反应
c.F和G均能与银氨溶液反应
(6)H与 反应得到I经历了下图所示的多步反应。其中,中间产物1有2个六元环,红外光谱显示中间产物2、3中均含
反应得到I经历了下图所示的多步反应。其中,中间产物1有2个六元环,红外光谱显示中间产物2、3中均含 键。
键。_________ 、_________ 。
(7)I→J的过程中, 转化为含
转化为含 价Se的化合物,反应中
价Se的化合物,反应中 和I的物质的量之比为
和I的物质的量之比为_________ 。
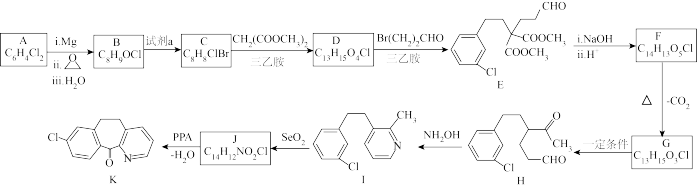
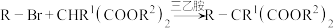
ii.R-NH2+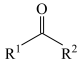

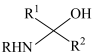
(2)B中含有
 ,试剂a是
,试剂a是(3)D的结构简式是
(4)E→F中,反应i的化学方程式为
(5)下列关于有机物F和G的说法正确的是
a.F和G均没有手性碳原子
b.F和G均能与
 反应
反应c.F和G均能与银氨溶液反应
(6)H与
 反应得到I经历了下图所示的多步反应。其中,中间产物1有2个六元环,红外光谱显示中间产物2、3中均含
反应得到I经历了下图所示的多步反应。其中,中间产物1有2个六元环,红外光谱显示中间产物2、3中均含 键。
键。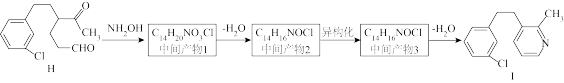
(7)I→J的过程中,
 转化为含
转化为含 价Se的化合物,反应中
价Se的化合物,反应中 和I的物质的量之比为
和I的物质的量之比为
您最近一年使用:0次
4 . 某课题组合成了一种非天然氨基酸X,合成路线如下(Ph—表示苯基):
(1)化合物F的一卤代物___________ (填有或无)手性碳原子;化合物X的分子式是___________ ;D分子中含有的官能团名称为___________ 。
(2)化合物A的结构简式是___________ ,化合物E的结构简式是___________ 。
(3)C→D的化学方程式是___________ 。
(4)分子式为 ,氨基与羧基连在同一个碳上的结构有
,氨基与羧基连在同一个碳上的结构有___________ 种(不考虑立体异构);其中核磁共振氢谱为1∶2∶3∶9的物质的结构简式为___________ 。
(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)___________ 。

已知:①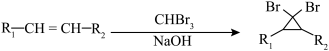
②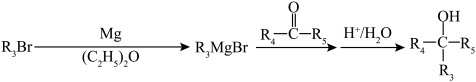
(1)化合物F的一卤代物
(2)化合物A的结构简式是
(3)C→D的化学方程式是
(4)分子式为
 ,氨基与羧基连在同一个碳上的结构有
,氨基与羧基连在同一个碳上的结构有(5)以化合物F、溴苯和甲醛为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)

您最近一年使用:0次
名校
解题方法
5 . 阿司匹林具有解热镇痛作用,科研工作者将阿司匹林与聚甲基丙烯酸借助乙二醇嫁接起来,合成长效缓释阿司匹林,从而减少了对肠胃的刺激,减少每天吃药次数,大大方便了人们对药物的使用。合成路线如下图所示:
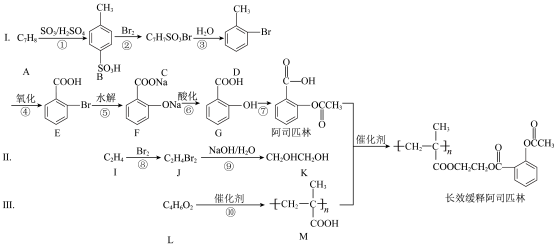
(1)阿司匹林的合成过程中间体B的名称是___________ 。
(2)由原料A制备中间体D不采取与 直接反应,而是经过①-③的目的是
直接反应,而是经过①-③的目的是___________ 。
(3)上述合成路径中阿司匹林实现了分子结构修饰,阿司匹林中发生分子结构修饰的官能团名称是___________ 。
(4)J→K的化学方程式是___________ 。
(5)L的结构简式为___________ 。
(6)请解释长效缓释阿司匹林的缓释原理是(用方程式表示)___________ 。
(7)下列说法正确的是___________。

(1)阿司匹林的合成过程中间体B的名称是
(2)由原料A制备中间体D不采取与
 直接反应,而是经过①-③的目的是
直接反应,而是经过①-③的目的是(3)上述合成路径中阿司匹林实现了分子结构修饰,阿司匹林中发生分子结构修饰的官能团名称是
(4)J→K的化学方程式是
(5)L的结构简式为
(6)请解释长效缓释阿司匹林的缓释原理是(用方程式表示)
(7)下列说法正确的是___________。
| A.阿司匹林中无手性碳原子 |
B.长效缓释阿司匹林单体的分子式是 |
| C.阿司匹林与长效缓释阿司匹林可通过红外光谱区别 |
| D.阿司匹林与化合物K、M通过加聚反应合成长效缓释阿司匹林 |
您最近一年使用:0次
解题方法
6 . 以乙烯和环戊烯E为主要原料合成功能高分子N的路线如下:
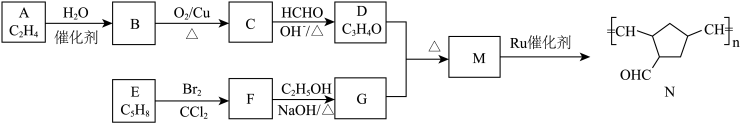
已知:①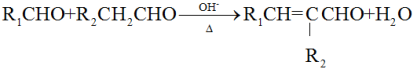
②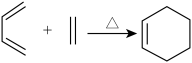
③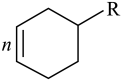

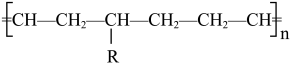
(1)B的核磁共振氢谱有三组峰,其峰面积之比为___________ 。
(2)B→C的反应类型是___________ ,D所含官能团的名称为___________ 。
(3)X是C的同分异构体,只有一种化学环境的氢原子,X的结构简式为___________ 。
(4)F→G反应的化学方程式为___________ ,M的结构简式为___________ 。

已知:①

②
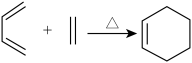
③


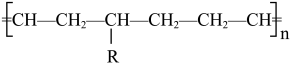
(1)B的核磁共振氢谱有三组峰,其峰面积之比为
(2)B→C的反应类型是
(3)X是C的同分异构体,只有一种化学环境的氢原子,X的结构简式为
(4)F→G反应的化学方程式为
您最近一年使用:0次
名校
解题方法
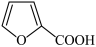
7 . 由呋喃甲醛可通过以下反应制备呋喃甲醇和呋喃甲酸。
2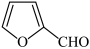 +NaOH
+NaOH
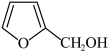 +
+ 
相关物质的部分理化信息如下:
王同学设计了如下实验流程:

(1)相应的操作名称:操作①_______ 、操作②_______ 。
(2)向操作①所得水溶液加盐酸控制pH为3,加入HCl后的离子方程式为_______ 。
(3)通过重结晶由粗产品提纯产品Y,操作如下:将过滤得到粗产品溶于5-7mL热水中,加活性炭,煮沸10min,趁热过滤,冷却滤液至低温,并在低温下过滤,得白色针状晶体产品Y。其中,趁热过滤的目的是_______ 。
(4)获得产品X和Y后,可通过下列手段分析生成物的结构,不能实现目的的有_______ 。
a.利用元素分析(李比希燃烧法)确定产品X和Y的分子式
b.利用红外光谱确定产品X和Y中含有的官能团种类及其个数
c.利用质谱仪确定产品X和Y的实验式
d.利用核磁共振氢谱仪确定产品X和Y的结构中存在几种环境的氢及其个数比
王同学在分析产品Y的质谱数据时,发现谱图中出现了质荷比(相对分子质量)为224的峰,该物质的可能结构为_______ 。
(5)经计算产品产率: 、
、 ,Y的产率高于X的原因是
,Y的产率高于X的原因是_______ 。
(6)将铜丝在空气中灼烧后变黑迅速伸入产品X中,铜丝重新变为红色。铜由黑色变成红色时发生的反应方程式为_______ 。
(7)产品Y在一定条件下可生成聚合物,该化学反应方程式为_______ 。
2
 +NaOH
+NaOH
 +
+ 
相关物质的部分理化信息如下:
| 物质 | 呋喃甲醛 | 呋喃甲醇 | 呋喃甲酸 | 乙醚 |
| 熔点/℃ | -36.5 | -29 | 133 | -116.3 |
| 沸点/℃ | 161.7 | 170 | 231 | 34.5 |
| 水溶性 | 0.084 | 微溶 | 4g/100mL(15℃) 25g/100mL(100℃) | 微溶 |
| 乙醚中溶解性 | 易溶 | 易溶 | 易溶 | |
| 相对分子质量 | 96 | 98 | 112 | 74 |

(1)相应的操作名称:操作①
(2)向操作①所得水溶液加盐酸控制pH为3,加入HCl后的离子方程式为
(3)通过重结晶由粗产品提纯产品Y,操作如下:将过滤得到粗产品溶于5-7mL热水中,加活性炭,煮沸10min,趁热过滤,冷却滤液至低温,并在低温下过滤,得白色针状晶体产品Y。其中,趁热过滤的目的是
(4)获得产品X和Y后,可通过下列手段分析生成物的结构,不能实现目的的有
a.利用元素分析(李比希燃烧法)确定产品X和Y的分子式
b.利用红外光谱确定产品X和Y中含有的官能团种类及其个数
c.利用质谱仪确定产品X和Y的实验式
d.利用核磁共振氢谱仪确定产品X和Y的结构中存在几种环境的氢及其个数比
王同学在分析产品Y的质谱数据时,发现谱图中出现了质荷比(相对分子质量)为224的峰,该物质的可能结构为
(5)经计算产品产率:
 、
、 ,Y的产率高于X的原因是
,Y的产率高于X的原因是(6)将铜丝在空气中灼烧后变黑迅速伸入产品X中,铜丝重新变为红色。铜由黑色变成红色时发生的反应方程式为
(7)产品Y在一定条件下可生成聚合物,该化学反应方程式为
您最近一年使用:0次
解题方法
8 . M是合成某种药物的中间体,其合成路线如图:
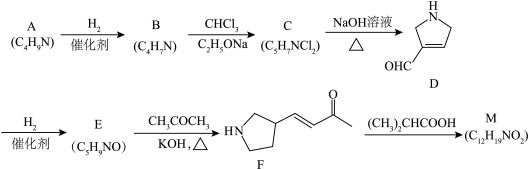
已知信息:A中存在大π键
回答下列问题:
(1)C的核磁共振氢谱有三组峰且峰面积之比为4∶2∶1,则C的结构简式_______ 。
(2)E中官能团名称为_______ 。
(3)写出F生成M的反应方程式_______ 。
(4) A、B、C、D、E、F、M中无碱性的是_______ (填字母)。
(5)根据上述信息,以2,7-辛二酮为主要原料制备 的合成路线
的合成路线______ 。

已知信息:A中存在大π键

回答下列问题:
(1)C的核磁共振氢谱有三组峰且峰面积之比为4∶2∶1,则C的结构简式
(2)E中官能团名称为
(3)写出F生成M的反应方程式
(4) A、B、C、D、E、F、M中无碱性的是
(5)根据上述信息,以2,7-辛二酮为主要原料制备
 的合成路线
的合成路线
您最近一年使用:0次
名校
9 . 青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,其分子结构如图所示,它可以用有机溶剂A从中药中提取。
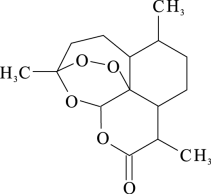
(1)下列关于青蒿素的说法不正确的是___________ (填字母)。
a.分子式为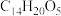 b.分子中含有酯基和醚键
b.分子中含有酯基和醚键
c.易溶于有机溶剂A,不易溶于水 d分子的空间结构不是平面形
(2)使用现代分析仪器对有机化合物A的分化结构进行测定,相关结果如下:


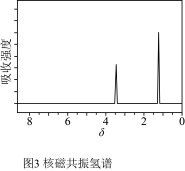
①根据图1,A的相对分子质量为___________ 。
②根据图2,推测A可能所属的有机化合物类别和其分子式___________ 、___________ 。
③根据以上结果和图3(两个峰的面积比为 ),推测A的结构简式
),推测A的结构简式___________ 。
(3)青蒿素中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取青蒿素样品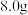 配制成
配制成 溶液,取
溶液,取 加入锥形瓶中,再加入足量的
加入锥形瓶中,再加入足量的 溶液和几滴淀粉溶液,用
溶液和几滴淀粉溶液,用 标准液滴定[已知:
标准液滴定[已知: ,M(青蒿素)=282g/mol]。
,M(青蒿素)=282g/mol]。
①滴定终点的颜色变化为___________ 。
②三次滴定数据记录如表:
则青蒿素的纯度为___________ 。

(1)下列关于青蒿素的说法不正确的是
a.分子式为
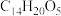 b.分子中含有酯基和醚键
b.分子中含有酯基和醚键c.易溶于有机溶剂A,不易溶于水 d分子的空间结构不是平面形
(2)使用现代分析仪器对有机化合物A的分化结构进行测定,相关结果如下:



①根据图1,A的相对分子质量为
②根据图2,推测A可能所属的有机化合物类别和其分子式
③根据以上结果和图3(两个峰的面积比为
 ),推测A的结构简式
),推测A的结构简式(3)青蒿素中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取青蒿素样品
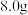 配制成
配制成 溶液,取
溶液,取 加入锥形瓶中,再加入足量的
加入锥形瓶中,再加入足量的 溶液和几滴淀粉溶液,用
溶液和几滴淀粉溶液,用 标准液滴定[已知:
标准液滴定[已知: ,M(青蒿素)=282g/mol]。
,M(青蒿素)=282g/mol]。①滴定终点的颜色变化为
②三次滴定数据记录如表:
| 滴定次数 | 待测液体 | 标准液读数(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 1.50 | 41.52 |
| 第二次 | 25.00 | 3.00 | 42.98 |
| 第三次 | 25.00 | 4.50 | 41.60 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
10 . 某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去)。
(1)该小组同学用该装置进行“H2的制取及燃烧性质验证”实验。他们设计了如下的实验步骤:
a.组装装置并检验气密性;
b.装入药品,关闭活塞m和n,固定在铁架台上;
c.打开分液漏斗活塞m,使反应开始;
d.当观察到B中有较多气体时,打开活塞n并点燃气体。
回答下列问题:
①以上某步骤中有一处明显的操作错误,请指错误之处_______ 。
②该小组同学在进行c步骤操作时,发现分液漏斗中的溶液不能滴下,你认为可能的原因有_______ 。
(2)该装置还可用于制取并收集少量其他气体,用字母代号填空:
①下列气体中哪些可以用该装置来制取和收集_______ ;
②若将装置B中的水换成CCl4,下列气体中哪些可以用该装置来制取和收集_______ 。
A.O2 B.NO C.SO2 D.NH3 E.C2H2 F.C2H4
(3)该小组同学用该装置进行定量实验,以确定某稳定饱和脂肪醇的结构。

①反应前,先对量气管进行第一次读数,读数为40.0mL,然后在A中加入5gNa和0.62g待测醇,充分反应后,再进行第二次读数,读数为264.0mL(所有数据均已换算成标准状况时的数值)。读数时要注意的是:一是使视线与凹液面最低处相平,二是_______ 。
②为了进一步确定该醇的结构,又将0.62g该醇充分燃烧,可以生成0.02mol的CO2和0.03mol的H2O,已知两个或者两个以上的羟基连在同一个C原子上不能形成稳定的醇,根据上述信息计算确定该饱和醇的结构简式为_______ 。
(1)该小组同学用该装置进行“H2的制取及燃烧性质验证”实验。他们设计了如下的实验步骤:
a.组装装置并检验气密性;
b.装入药品,关闭活塞m和n,固定在铁架台上;
c.打开分液漏斗活塞m,使反应开始;
d.当观察到B中有较多气体时,打开活塞n并点燃气体。
回答下列问题:
①以上某步骤中有一处明显的操作错误,请指错误之处
②该小组同学在进行c步骤操作时,发现分液漏斗中的溶液不能滴下,你认为可能的原因有
(2)该装置还可用于制取并收集少量其他气体,用字母代号填空:
①下列气体中哪些可以用该装置来制取和收集
②若将装置B中的水换成CCl4,下列气体中哪些可以用该装置来制取和收集
A.O2 B.NO C.SO2 D.NH3 E.C2H2 F.C2H4
(3)该小组同学用该装置进行定量实验,以确定某稳定饱和脂肪醇的结构。

①反应前,先对量气管进行第一次读数,读数为40.0mL,然后在A中加入5gNa和0.62g待测醇,充分反应后,再进行第二次读数,读数为264.0mL(所有数据均已换算成标准状况时的数值)。读数时要注意的是:一是使视线与凹液面最低处相平,二是
②为了进一步确定该醇的结构,又将0.62g该醇充分燃烧,可以生成0.02mol的CO2和0.03mol的H2O,已知两个或者两个以上的羟基连在同一个C原子上不能形成稳定的醇,根据上述信息计算确定该饱和醇的结构简式为
您最近一年使用:0次



