1 . 气态烃A在一定条件下和B发生下列反应生成物质C,已知烃A在标准状况下的密度为1.16g•L-1。

请回答:
(1)A的官能团名称为______________ 。
(2)上述有机反应类型为____________ 。
(3)下列说法正确的是________
a.C的密度比水大
b.A、B、C都能与溴水反应
c.C分子中所有碳原子处于同一个平面
d.C分子的一氯代物有5种(不考虑立体异构)

请回答:
(1)A的官能团名称为
(2)上述有机反应类型为
(3)下列说法正确的是
a.C的密度比水大
b.A、B、C都能与溴水反应
c.C分子中所有碳原子处于同一个平面
d.C分子的一氯代物有5种(不考虑立体异构)
您最近一年使用:0次
2 . 酸牛奶中含有乳酸,1mol丙酮酸( )在镍催化剂作用下加1mol氢气转变成乳酸。
)在镍催化剂作用下加1mol氢气转变成乳酸。
(1)乳酸的结构简式是_____________________ 。
(2)一个或两个乳酸分子在不同条件下可形成不同的酯,其酯的相对分子质量由小到大的结构简式依次为_____________________ 、_____________________ 、________________ 。
(3)与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式是________________________________ 。
(4)B的甲醇酯可以聚合,聚合物的结构简式是_____________________ 。
 )在镍催化剂作用下加1mol氢气转变成乳酸。
)在镍催化剂作用下加1mol氢气转变成乳酸。(1)乳酸的结构简式是
(2)一个或两个乳酸分子在不同条件下可形成不同的酯,其酯的相对分子质量由小到大的结构简式依次为
(3)与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式是
(4)B的甲醇酯可以聚合,聚合物的结构简式是
您最近一年使用:0次
解题方法
3 . 有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如图所示:
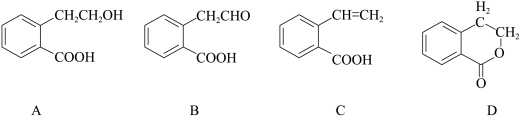
(1)A的分子式是______ ,B中的含氧官能团名称是______ 、________ 。
(2)A→B的反应类型是______ ;A—D中互为同分异构体的是______ (填代号)。

(1)A的分子式是
(2)A→B的反应类型是
您最近一年使用:0次
4 . 橡胶
①橡胶是一类具有高弹性的高分子材料,是制造汽车、飞机轮胎和各种密封材料所必需的原料。天然橡胶的主要成分是______ ,结构简式为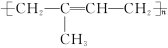 ,其单体为
,其单体为 ;天然橡胶分子中含有
;天然橡胶分子中含有 ,易发生
,易发生______ 反应和______ 反应。
②橡胶的分类
橡胶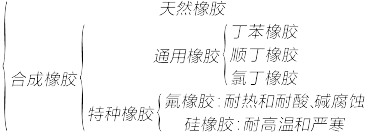
③性能:具有高弹性、绝缘性、气密性、耐油、耐高温或耐低温等性能。
④用途:制造汽车、飞机轮胎;各种密封材料。
①橡胶是一类具有高弹性的高分子材料,是制造汽车、飞机轮胎和各种密封材料所必需的原料。天然橡胶的主要成分是
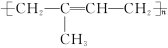 ,其单体为
,其单体为 ;天然橡胶分子中含有
;天然橡胶分子中含有 ,易发生
,易发生②橡胶的分类
橡胶
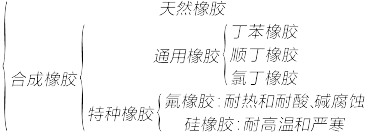
③性能:具有高弹性、绝缘性、气密性、耐油、耐高温或耐低温等性能。
④用途:制造汽车、飞机轮胎;各种密封材料。
您最近一年使用:0次
5 . A~G是几种烃的分子球棍模型,据此回答下列问题。
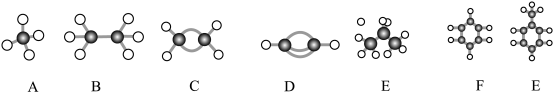
(1)这几种烃的结构简式分别是D:___ ,E:___ ,G:___ 。
(2)其中A分子的空间构型是___ ,C的官能团名称是___ (以下均用结构简式作答)。
(3)写出C与溴的四氯化碳溶液反应的化学方程式___ ,反应类型为___ 。
(4)写出F与液溴反应的化学方程式___ ,反应类型为___ 。
(5)等质量的B、C、D完全燃烧时耗去O2的量最多的是___ 。

(1)这几种烃的结构简式分别是D:
(2)其中A分子的空间构型是
(3)写出C与溴的四氯化碳溶液反应的化学方程式
(4)写出F与液溴反应的化学方程式
(5)等质量的B、C、D完全燃烧时耗去O2的量最多的是
您最近一年使用:0次
6 . 按要求回答下列问题:
(1)某有机物的结构简式为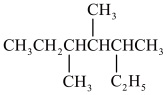
①该有机物系统命名法命名为____________ 。
②若该烷烃是由单炔烃和氢气加成得到的,则可能的单炔烃有________ 种。
③若该烷烃是由单烯烃和氢气加成得到的,则可能的烯烃有____ 种,任写一种烯烃的结构简式:________________________ 。
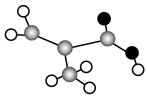
(2)某有机物只含C、H、O 三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),该物质的结构简式为___________ 。
(1)某有机物的结构简式为

①该有机物系统命名法命名为
②若该烷烃是由单炔烃和氢气加成得到的,则可能的单炔烃有
③若该烷烃是由单烯烃和氢气加成得到的,则可能的烯烃有
(2)某有机物只含C、H、O 三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),该物质的结构简式为

您最近一年使用:0次
7 . 羰基的加成反应
(1)乙醛与HCN加成:_______ 。
(2)丙酮与HCN加成:_______ 。
(1)乙醛与HCN加成:
(2)丙酮与HCN加成:
您最近一年使用:0次
8 . 氯乙烷是一种重要的化工产品。通过如下两个反应均可得到氯乙烷:
①CH3CH3+Cl2 ―→CH3CH2Cl+HCl
②CH2=CH2+HCl ―→ CH3CH2Cl
(1)①属于下列________ 反应;②属于下列________ 反应。
A.加成 B.取代 C.氧化
(2)你认为反应_______ 合理,原因是__________ 。
①CH3CH3+Cl2 ―→CH3CH2Cl+HCl
②CH2=CH2+HCl ―→ CH3CH2Cl
(1)①属于下列
A.加成 B.取代 C.氧化
(2)你认为反应
您最近一年使用:0次
9 . Ⅰ.乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式:_________________________________ 。
(2)已知:
甲醇脱水反应 2CH3OH(g) =CH3OCH3(g) + H2O(g) △H1=-23.9 kJ·mol—1
甲醇制烯烃反应 2CH3OH(g) =C2H4(g) + 2H2O(g) △H2=-29.1 kJ·mol—1
乙醇异构化反应 C2H5OH(g) =CH3OCH3(g) △H3=+ 50.7 kJ·mol—1[
则乙烯气相直接水合反应C2H4(g) + H2O(g)=C2H5OH(g)的△H =__________________________ 。与间接水合法相比,气相直接水合法的优点是__________________________________ 。
Ⅱ. 甲醇虽然毒性很强,但它是一种清洁燃料,也是一种重要的合成原料。工业甲醇的质量分数可以用下列方法测定:
①在稀硫酸中甲醇被Cr2O 氧化成CO2和H2O,其反应为:
氧化成CO2和H2O,其反应为:
CH3OH + Cr2O + 8H+=CO2↑+ 2Cr3++ 6H2O;
+ 8H+=CO2↑+ 2Cr3++ 6H2O;
②过量的Cr2O 可用Fe2+与之完全反应,反应如下所示:
可用Fe2+与之完全反应,反应如下所示:
____Cr2O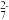 + ____Fe2+ +____H+――― ____Cr3++____Fe3+ +____H2O
+ ____Fe2+ +____H+――― ____Cr3++____Fe3+ +____H2O
现有0.12 g工业甲醇,在稀硫酸中与25.0 mL 0.2 mol/L K2Cr2O7溶液反应,多余的K2Cr2O7恰好与9.6 mL 1.0 mol/LFeSO4溶液完全反应。
(3)请配平第②步中离子方程式____ 。
(4)工业甲醇的质量分数为__________ 。
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式:
(2)已知:
甲醇脱水反应 2CH3OH(g) =CH3OCH3(g) + H2O(g) △H1=-23.9 kJ·mol—1
甲醇制烯烃反应 2CH3OH(g) =C2H4(g) + 2H2O(g) △H2=-29.1 kJ·mol—1
乙醇异构化反应 C2H5OH(g) =CH3OCH3(g) △H3=+ 50.7 kJ·mol—1[
则乙烯气相直接水合反应C2H4(g) + H2O(g)=C2H5OH(g)的△H =
Ⅱ. 甲醇虽然毒性很强,但它是一种清洁燃料,也是一种重要的合成原料。工业甲醇的质量分数可以用下列方法测定:
①在稀硫酸中甲醇被Cr2O
 氧化成CO2和H2O,其反应为:
氧化成CO2和H2O,其反应为:CH3OH + Cr2O
 + 8H+=CO2↑+ 2Cr3++ 6H2O;
+ 8H+=CO2↑+ 2Cr3++ 6H2O;②过量的Cr2O
 可用Fe2+与之完全反应,反应如下所示:
可用Fe2+与之完全反应,反应如下所示:____Cr2O
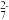 + ____Fe2+ +____H+――― ____Cr3++____Fe3+ +____H2O
+ ____Fe2+ +____H+――― ____Cr3++____Fe3+ +____H2O现有0.12 g工业甲醇,在稀硫酸中与25.0 mL 0.2 mol/L K2Cr2O7溶液反应,多余的K2Cr2O7恰好与9.6 mL 1.0 mol/LFeSO4溶液完全反应。
(3)请配平第②步中离子方程式
(4)工业甲醇的质量分数为
您最近一年使用:0次
名校
10 . 指出下列有关反应属哪个有机反应类型:
(1)乙酸与乙醇的反应,属_________ 反应。
(2)乙烯与酸性高锰酸钾溶液的反应,属_________ 反应。
(3)乙烯与溴水的反应,属__________ 反应。
(1)乙酸与乙醇的反应,属
(2)乙烯与酸性高锰酸钾溶液的反应,属
(3)乙烯与溴水的反应,属
您最近一年使用:0次
2017-07-23更新
|
326次组卷
|
2卷引用:黑龙江省伊春市第二中学2016-2017学年高一下学期期末考试(文)化学试题



