1 . C是一种高分子有机物,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

(1)写出A的电子式___________ ;A含有的共价键的类型有___________ (键的极性)D的结构简式___________ ;
(2)A→B的化学方程式___________ 反应类型为___________
(3)B→C的化学方程式为___________ 。反应类型为___________

(1)写出A的电子式
(2)A→B的化学方程式
(3)B→C的化学方程式为
您最近一年使用:0次
解题方法
2 . 用下图中的实验装置制取乙炔。
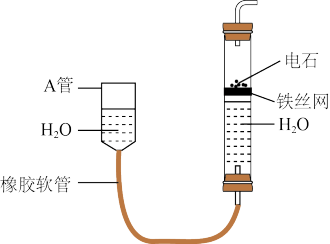
(1)图中,A管的作用是_______ ,制取乙炔的化学方程式是_______ 。
(2)乙炔通入酸性KMnO4溶液中观察到的现象是_______ ,乙炔发生了_______ 反应。
(3)乙炔通入溴的CCl4溶液中发生了_______ 反应。
(4)为了安全,点燃乙炔前应_______ ,乙炔燃烧时的实验现象是_______ 。

(1)图中,A管的作用是
(2)乙炔通入酸性KMnO4溶液中观察到的现象是
(3)乙炔通入溴的CCl4溶液中发生了
(4)为了安全,点燃乙炔前应
您最近一年使用:0次
解题方法
3 . 关于有机反应类型,下列判断不正确的是
A.CH≡CH+HCl CH2=CHCl(加成反应) CH2=CHCl(加成反应) |
B.CH3CH(Br)CH3+KOH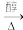 CH2=CHCH3↑+KBr+H2O(消去反应) CH2=CHCH3↑+KBr+H2O(消去反应) |
C.2CH3CH2OH+O2 2CH3CHO+2H2O(还原反应) 2CH3CHO+2H2O(还原反应) |
D. 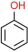  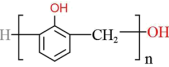 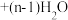 (缩聚反应) (缩聚反应) |
您最近一年使用:0次
解题方法
4 . 聚乙烯醇(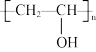 )是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
)是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
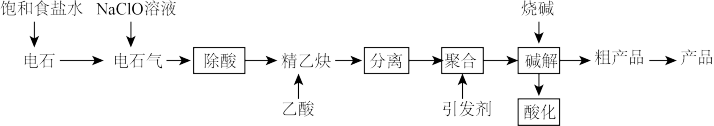
已知:①电石气中通常含有H2S、PH3等杂质②电石气通入次氯酸钠溶液后反应后,溶液仍澄清③乙炔较易与羧酸反应生成酯
回答下列问题:
(1)制取电石气时用饱和食盐水代替水的目的是____ ,电石气通入NaClO溶液发生的主要反应的离子方程式为____ (写一个即可)。
(2)分离过程中采取的主要操作名称为____ 。
(3)碱解时发生反应的化学方程式为____ ,流程图中可循环利用的物质为____ 。
(4)电石常用CaO与碳素材料在1800~2200℃的高温下制备,甲烷在高温下(1300~1500℃和氧不足的条件下燃烧时所放出的热量可使甲烷发生反应生成乙炔。与电石制乙炔相比,该方法的优点是___ (写一条即可),若标准状况下22.4m3甲烷可得到聚乙烯醇产品13.2kg,则甲烷的转化率为___ 。
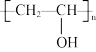 )是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
)是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
已知:①电石气中通常含有H2S、PH3等杂质②电石气通入次氯酸钠溶液后反应后,溶液仍澄清③乙炔较易与羧酸反应生成酯
回答下列问题:
(1)制取电石气时用饱和食盐水代替水的目的是
(2)分离过程中采取的主要操作名称为
(3)碱解时发生反应的化学方程式为
(4)电石常用CaO与碳素材料在1800~2200℃的高温下制备,甲烷在高温下(1300~1500℃和氧不足的条件下燃烧时所放出的热量可使甲烷发生反应生成乙炔。与电石制乙炔相比,该方法的优点是
您最近一年使用:0次
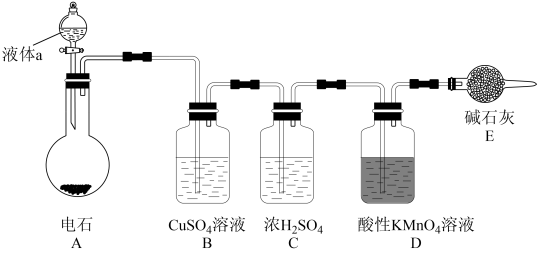
5 . 如图为实验室制取乙炔及其性质检验的装置图。(电石中含CaS等杂质)
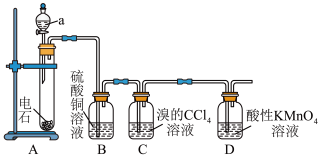
回答下列问题:
(1)仪器a的名称为_______ ;该仪器中盛放的试剂为_______ 。
(2)装置A中主要反应的化学方程式为_______ 。
(3)装置B的作用是_______ 。
(4)C中反应物之间按物质的量之比1∶1反应,其化学方程式为_______ 。
(5)D中观察到的现象是_______ 。

回答下列问题:
(1)仪器a的名称为
(2)装置A中主要反应的化学方程式为
(3)装置B的作用是
(4)C中反应物之间按物质的量之比1∶1反应,其化学方程式为
(5)D中观察到的现象是
您最近一年使用:0次
6 . 利用下列实验药品进行实验,能顺利达到实验目的的是
| 实验目的 | 实验药品 | |
| A | 证明乙炔能和 反应 反应 | 电石、饱和食盐水、 溶液和溴水 溶液和溴水 |
| B | 除去粗盐中的 、 、 和 和 | 粗盐、蒸馏水、 溶液和 溶液和 溶液 溶液 |
| C | 检验溴乙烷中的溴原子 | 溴乙烷、 溶液和 溶液和 溶液 溶液 |
| D | 验证乙醇消去产物有乙烯 | 乙醇、浓硫酸和酸性高锰酸钾溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 在一定条件下,反应I:2CH2=CH2
 、反应II:3HC≡CCH3
、反应II:3HC≡CCH3
 ,下列说法错误的是
,下列说法错误的是

 、反应II:3HC≡CCH3
、反应II:3HC≡CCH3
 ,下列说法错误的是
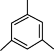
,下列说法错误的是| A.反应I和反应II的反应类型相同,且原子利用率都为100% |
B. 与环己烷互为同系物 与环己烷互为同系物 |
C.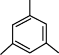 的二氯代物有5种 的二氯代物有5种 |
D. 和 和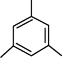 两种化合物中碳原子都是共平面的 两种化合物中碳原子都是共平面的 |
您最近一年使用:0次
名校
8 . 如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
(1)写出实验室制取乙炔的化学方程式_______ 。
(2)实验室制取乙炔时,分液漏斗中的液体a通常是_______ 。
(3)装置D中的现象是_______ 。
(4)若D装置中药品为溴水,其生成四溴代物的反应方程式为:_______ 。

(1)写出实验室制取乙炔的化学方程式
(2)实验室制取乙炔时,分液漏斗中的液体a通常是
(3)装置D中的现象是
(4)若D装置中药品为溴水,其生成四溴代物的反应方程式为:
您最近一年使用:0次
名校
解题方法
9 . 实验室常用如图中的装置制备乙炔并检验乙炔的性质
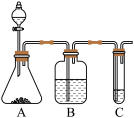
(1)实验室制备乙炔的化学方程式是_______ ;
(2)实验过程中,A中_______ (填仪器名称)中通常使用饱和食盐水,其目的是_______ ,B的作用是除去乙炔气体中的杂质,盛装的药品是_______ 溶液;
(3)若C中试剂是溴水,可以观察到的现象是_______ ;
(4)以乙炔为主要原料可合成聚氯乙烯等,其制备过程如下:
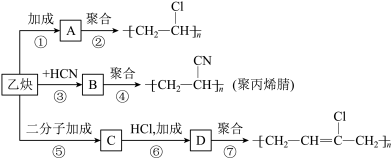
Ⅰ.试写出A、B和C的结构简式:A_______ ;B_______ ;C_______ 。
Ⅱ.反应③的反应类型为_______
Ⅲ.写出反应①和反应⑦的化学方程式
_______ ,
_______ 。
Ⅳ。三分子乙炔在一定条件下可聚合成环状分子E,该分子E可与硝酸在一定条件下发生取代反应,请写出该反应_______ 。

(1)实验室制备乙炔的化学方程式是
(2)实验过程中,A中
(3)若C中试剂是溴水,可以观察到的现象是
(4)以乙炔为主要原料可合成聚氯乙烯等,其制备过程如下:

Ⅰ.试写出A、B和C的结构简式:A
Ⅱ.反应③的反应类型为
Ⅲ.写出反应①和反应⑦的化学方程式
Ⅳ。三分子乙炔在一定条件下可聚合成环状分子E,该分子E可与硝酸在一定条件下发生取代反应,请写出该反应
您最近一年使用:0次
解题方法
10 . 以1,2—二溴乙烷为原料制备聚氯乙烯,为了提高原料利用率,有同学设计如下流程:1,2—二溴乙烷→A→B→聚氯乙烯。
(1)A→B___________ (填反应类型)
(2)A___________ (填结构式)
(3)B→聚氯乙烯___________ (填反应类型)
(4)写出1,2—二溴乙烷→A的化学方程式___________ 。
(1)A→B
(2)A
(3)B→聚氯乙烯
(4)写出1,2—二溴乙烷→A的化学方程式
您最近一年使用:0次



