1 . 端炔烃在催化剂存在下可发生偶联反应,成为Glaser反应。
2R—C≡C—H R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
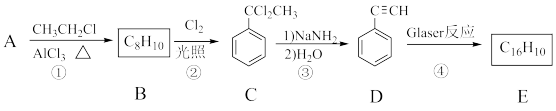
回答下列问题:
(1)B的结构简式为_______ ,D 的化学名称为_______ 。
(2)①和③的反应类型分别为_______ 、_______ 。
(3)E的结构简式为_______ 。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气_______ mol。
(4)B能和酸性高锰酸钾反应生成一种物质F,分离提纯含有少量氯化钠和泥沙的F常用的方法是_______ 。
(5)G是含有与D相同官能团的最简单的有机化合物,实验室制取该有机物的化学方程式_______ 。
2R—C≡C—H
 R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为
(2)①和③的反应类型分别为
(3)E的结构简式为
(4)B能和酸性高锰酸钾反应生成一种物质F,分离提纯含有少量氯化钠和泥沙的F常用的方法是
(5)G是含有与D相同官能团的最简单的有机化合物,实验室制取该有机物的化学方程式
您最近一年使用:0次
2 . 下列说法正确的是
A.相同条件下,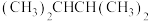 的熔点高于 的熔点高于 |
B.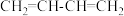 与氢气反应可以得到四种不同产物 与氢气反应可以得到四种不同产物 |
| C.工业上可以用乙炔和水反应制取乙醛 |
| D.溴水可以鉴别苯和甲苯 |
您最近一年使用:0次
3 . 下列实验对应的方程式及反应类型不完全正确的是
A.乙炔水化法制备乙醛含加成反应: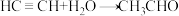 |
B.苯的磺化为取代反应:C6H6+H2SO4(浓) C6H5-SO3H+H2O C6H5-SO3H+H2O |
C.甲苯与氯气在光照条件下发生取代反应: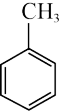 +Cl2 +Cl2 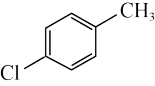 +HCl +HCl |
| D.向氨水中滴入少量硫酸铜溶液的总反应:Cu2++4NH3=[Cu(NH3)4]2+ |
您最近一年使用:0次
4 . 下列反应中,其有机产物含有两个官能团的是
| A.lmol乙炔与2mol溴化氢发生加成反应 |
| B.乙烯与H2O发生加成反应 |
| C.在FeBr3催化下,苯与液溴发生取代反应 |
| D.甲苯发生硝化反应生成梯恩梯(TNT) |
您最近一年使用:0次
5 . 由1L乙烯和乙炔的混合气体,在催化剂存在下与足量的H2发生加成反应,消耗H21.4L,则原混合气体中乙烯与乙炔的体积比为
| A.3:2 | B.2:3 | C.2:1 | D.1:2 |
您最近一年使用:0次
名校
6 . Ⅰ.现有下列六种烃:① ②
② ③乙烷④戊烷⑤
③乙烷④戊烷⑤ ⑥
⑥
(1)用系统命名法命名有机物①____ ,②③④⑤四种物质按它们的沸点由高到低的顺序排列____ (填序号),⑥的二氯代物有____ 种。
(2)Ⅱ.聚氯乙烯,简称PVC,是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔(CH≡CH)为原料合成聚氯乙烯,流程如图。
CH≡CH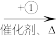
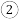
 PVC
PVC
乙炔与①反应的有机反应类型为____ ,②的官能团名称为____ 。写出由②生成PVC的反应方程式____ 。
(3)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到____ 种产物。若烃X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3—甲基—1,1,2,2—四溴丁烷,则烃X的结构简式为____ 。
 ②
② ③乙烷④戊烷⑤
③乙烷④戊烷⑤ ⑥
⑥
(1)用系统命名法命名有机物①
(2)Ⅱ.聚氯乙烯,简称PVC,是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔(CH≡CH)为原料合成聚氯乙烯,流程如图。
CH≡CH
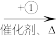
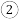
 PVC
PVC乙炔与①反应的有机反应类型为
(3)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到
您最近一年使用:0次
名校
7 . 近年来,由于石油价格上涨,以煤为原料制备一些化工产品的前景又被看好。如图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
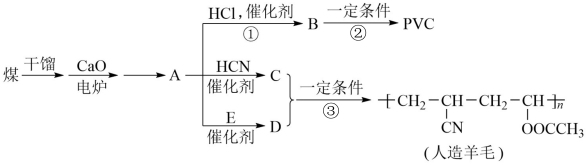
请回答下列问题:
(1)A的结构中含有三键,则A的结构式为_____ ,B的结构简式为____ 。
(2)写出反应类型:反应①____ ,反应③____ 。
(3)PVC的链节为____ ,写出B生成PVC的化学方程式:____ 。
(4)已知D的结构简式为CH2=CHOOCCH3,则E的结构简式为____ 。
(5)反应③中C、D两种单体按…CDCDCD…方式加聚,则C和D生成人造羊毛的化学方程式为____ 。

请回答下列问题:
(1)A的结构中含有三键,则A的结构式为
(2)写出反应类型:反应①
(3)PVC的链节为
(4)已知D的结构简式为CH2=CHOOCCH3,则E的结构简式为
(5)反应③中C、D两种单体按…CDCDCD…方式加聚,则C和D生成人造羊毛的化学方程式为
您最近一年使用:0次
2022·河北·模拟预测
解题方法
8 . 碳化锂(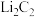 )是一种重要的化工试剂,在空气中易潮解。制备
)是一种重要的化工试剂,在空气中易潮解。制备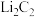 的一种原理是:
的一种原理是: 。实验室制备CO的一种原理是:
。实验室制备CO的一种原理是: 在浓硫酸、加热条件下生成CO、
在浓硫酸、加热条件下生成CO、 和
和 ,通过净化得到CO。某实验小组设计实验制备碳化锂并探究其性质,实验装置如下。
,通过净化得到CO。某实验小组设计实验制备碳化锂并探究其性质,实验装置如下。
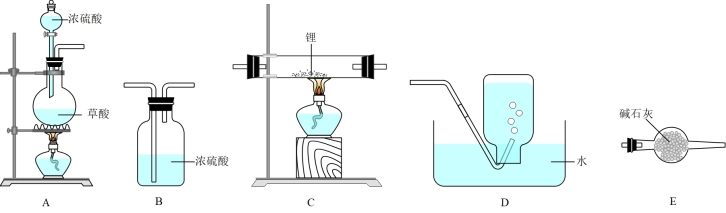
已知:碳化锂与水反应生成氢氧化锂和乙炔( )。回答下列问题:
)。回答下列问题:
(1)实验室里通常将金属锂保存在_______ 中。
(2)气流从左至右,装置连接顺序为A→_______ 。
(3)实验时,先点燃_______ (填“A”或“C”)处酒精灯,其目的是_______ 。
(4)装置D中集气瓶收集的气体经干燥后得到_______ (填化学式)。
(5)如果用甲酸(HCOOH)代替草酸(其他不变),也可以制备CO,用甲酸制备CO的化学方程式为_______ 。
(6)设计简单实验检验碳化锂产品中是否有锂单质:_______ 。
(7)取少量碳化锂投入酸性 溶液(含
溶液(含 )中,振荡,溶液由紫色变无色,产生的气体能使澄清石灰水变浑浊,写出化学方程式
)中,振荡,溶液由紫色变无色,产生的气体能使澄清石灰水变浑浊,写出化学方程式_______ 。
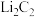 )是一种重要的化工试剂,在空气中易潮解。制备
)是一种重要的化工试剂,在空气中易潮解。制备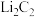 的一种原理是:
的一种原理是: 。实验室制备CO的一种原理是:
。实验室制备CO的一种原理是: 在浓硫酸、加热条件下生成CO、
在浓硫酸、加热条件下生成CO、 和
和 ,通过净化得到CO。某实验小组设计实验制备碳化锂并探究其性质,实验装置如下。
,通过净化得到CO。某实验小组设计实验制备碳化锂并探究其性质,实验装置如下。
已知:碳化锂与水反应生成氢氧化锂和乙炔(
 )。回答下列问题:
)。回答下列问题:(1)实验室里通常将金属锂保存在
(2)气流从左至右,装置连接顺序为A→
(3)实验时,先点燃
(4)装置D中集气瓶收集的气体经干燥后得到
(5)如果用甲酸(HCOOH)代替草酸(其他不变),也可以制备CO,用甲酸制备CO的化学方程式为
(6)设计简单实验检验碳化锂产品中是否有锂单质:
(7)取少量碳化锂投入酸性
 溶液(含
溶液(含 )中,振荡,溶液由紫色变无色,产生的气体能使澄清石灰水变浑浊,写出化学方程式
)中,振荡,溶液由紫色变无色,产生的气体能使澄清石灰水变浑浊,写出化学方程式
您最近一年使用:0次
9 . 乙炔是一种重要的化工原料,可以合成多种物质。
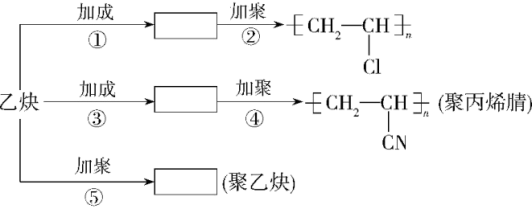
(1)实验室可用电石与水反应制取乙炔,写出反应的化学方程式:___________ 。
(2)写出③、④两个反应的化学方程式:③___________ ;④___________ 。

(1)实验室可用电石与水反应制取乙炔,写出反应的化学方程式:
(2)写出③、④两个反应的化学方程式:③
您最近一年使用:0次
10 . 如图所示实验装置可用于制取乙炔。请填空:
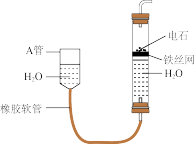
(1)图中,A管的作用是___________ ,制取乙炔的化学方程式是___________ 。
(2)乙炔通入酸性KMnO4溶液中观察到的现象是_______ ,乙炔发生了_________ 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是_______ ,乙炔发生了________ 反应。
(4)为了安全,点燃乙炔前应_____ ,乙炔燃烧时的实验现象是_______ 。
(5)若把乙炔与HCl加成,1mol乙炔最多可与____ molHCl加成,1mol其加成产物能和____ molCl2发生取代反应。

(1)图中,A管的作用是
(2)乙炔通入酸性KMnO4溶液中观察到的现象是
(3)乙炔通入溴的CCl4溶液中观察到的现象是
(4)为了安全,点燃乙炔前应
(5)若把乙炔与HCl加成,1mol乙炔最多可与
您最近一年使用:0次



