1 . 现有短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径如图所示,下列推断正确的是


| A.Y、Z组成的化合物只含离子键 |
| B.氢化物的沸点:R<X<Y |
| C.T的最高价氧化物的水化物酸性比R的强 |
| D.Y和Z分别与T、X组成的二元化合物的水溶液一定呈中性 |
您最近一年使用:0次
2010·安徽合肥·三模
2 . 以下是一些元素的信息,其中有一种元素不在短周期。根据信息完成问题:
(1)写出A元素基态原子的核外电子排布式____________________________________ 。
(2)B、C、X的简单离子半径由大到小的顺序为_______ (用元素离子符号表示)。
(3)化合物YZ4B化学键的类型是____________________________ ,检验该固体化合 物中阳离子的实验的方法和现象是______________________________ 。
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程____________________________________ 。
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5 mol·L-1 CB的水溶液时,两极共收集到气体22.4 L(标准状况下),计算电解后阴极区溶液的pH=________ (假设电解前后溶液体积不变)。
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中 键与 键与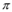 键数目比为1:2 键数目比为1:2 | 阳离子就是一个质子 |
(1)写出A元素基态原子的核外电子排布式
(2)B、C、X的简单离子半径由大到小的顺序为
(3)化合物YZ4B化学键的类型是
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5 mol·L-1 CB的水溶液时,两极共收集到气体22.4 L(标准状况下),计算电解后阴极区溶液的pH=
您最近一年使用:0次
11-12高一下·安徽淮北·阶段练习
名校
解题方法
3 . 某元素X的最高价含氧酸的化学式为HnXO2n﹣2,则在某气态氢化物中,X元素的化合价为
| A.5n﹣12 | B.3n﹣12 | C.3n﹣6 | D.n﹣10 |
您最近一年使用:0次
2016-07-08更新
|
97次组卷
|
4卷引用:2011-2012学年安徽省濉溪县临涣中学高一下学期第一次月考化学试卷
(已下线)2011-2012学年安徽省濉溪县临涣中学高一下学期第一次月考化学试卷2015-2016学年河北省保定三中高一下4月月考化学试卷广西柳州市第二中学2018-2019学年高一下学期第一次月考化学试题(已下线)【南昌新东方】2019-2020 南大附中 高一下 第三次月考
名校
4 . 已知W、X、Y、Z为原子序数依次递增的短周期主族元素,工业上通过分离液态空气获得W的单质;W、Z同主族,X、Y、Z同周期, X、Y为金属元素。下列说法正确的是
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X形成的化合物中只含离子键 |
| C.W 元素的氢化物的水溶液显碱性 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
您最近一年使用:0次
2017-11-30更新
|
100次组卷
|
3卷引用:安徽省六安市舒城中学2017-2018学年高一下学期第二次统考化学试题
解题方法
5 . W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
| A.金属性:Y>Z |
| B.氢化物的稳定性:X>W |
| C.离子的还原性:X>W |
| D.原子及离子半径:Z>Y>X |
您最近一年使用:0次
2016-04-20更新
|
77次组卷
|
4卷引用:安徽省砀山县第四中学2021-2022学年高一下学期第一阶段教学质量检测 化学试题
6 . 由部分短周期元素形成的单质或氧化物之间有以下关系
单质X + 氧化物M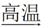 氧化物N
氧化物N
单质Y + 氧化物M 单质X + 氧化物R
单质X + 氧化物R
单质X + 氧化物Z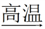 单质D + 氧化物N
单质D + 氧化物N
若X为非金属单质,则组成Y单质的元素在周期表的位置是( )
单质X + 氧化物M
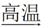 氧化物N
氧化物N 单质Y + 氧化物M
 单质X + 氧化物R
单质X + 氧化物R单质X + 氧化物Z
 单质D + 氧化物N
单质D + 氧化物N若X为非金属单质,则组成Y单质的元素在周期表的位置是( )
| A.第二周期ⅣA族 | B.第二周期ⅥA族 |
| C.第三周期ⅡA族 | D.第三周期ⅣA族 |
您最近一年使用:0次
名校
7 . 有X、Y、Z、M、N按原子序数依次递增的五种短周期元素,其中Z、M、N同周期,X、Z同主族且X是原子半径最小的原子;Y、N同主族,Z+与Y2—具有相同的电子层结构;M的单质晶体熔点高、硬度大,是一种重要的半导体材料。
(1)M的元素名称_______ ,N在元素周期表中的位置________ 。
(2)离子半径比较:r(Z+)___ r(Y2-)。
(3)X与Z形成的化合物A是___________ (填“离子化合物”或“共价化合物”),A与X2Y反应的化学方程式是_______________________________ 。
(1)M的元素名称
(2)离子半径比较:r(Z+)
(3)X与Z形成的化合物A是
您最近一年使用:0次
2016-12-09更新
|
159次组卷
|
4卷引用:2014-2015安徽省宣郞广三校高一下学期期中联考化学试卷
10-11高一下·安徽滁州·期中
8 . X、Y、Z三种短周期元素的原子序数之和为28,X、Y为相邻周期元素,X、Z为同周期元素,Y的质子数比X多5个,X的最外层电子数是Y的2倍,X和Z的最外层电子数之和为11。下列叙述中,不正确的是
| A.元素Z的气态氢化物和最高价氧化物的水化物水溶液均呈酸性 |
| B.X、Y、Z三种元素组成的化合物,其化学式为Y(ZX3)3 |
| C.元素Z可组成由共价键构成的单质 |
| D.X、Y两种元素构成一种阴离子,该阴离子与酸反应时,可能变成Y的阳离子 |
您最近一年使用:0次
2010·安徽安庆·一模
9 . 现有A─E五种元素,其中C、D、E三种是短周期元素。A、B的单质均为生活中常见的金属,A的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160,B的相对原子质量比A大8。C是金属元素,其原子的M层有一个未成对的p电子;D元素的主族序数是其所在周期序数的3倍;E的某种原子的原子核内没有中子。
(1)请写出A在元素周期表中的位置__________ ;写出C的核外电子排布式_________ ;D和E按1:1的原子个数比形成的化合物中含有的化学键为______ (填“极性键”、“非极性键”或“极性键和非极性键”)。
(2)①写出C单质与强碱溶液反应的离子方程式是__________________ 。
②在高温条件下,将D、E组成的气态化合物与A 的粉末充分反应,生成8g E的单质和相应的固态化合物时,放出akJ热量,此反应的热化学方程式是______________ 。
③A的某种氯化物溶液呈黄色,它与B的单质的反应工业上常用于腐蚀电路板,请写出反应的离子方程式____________________________ 。
(1)请写出A在元素周期表中的位置
(2)①写出C单质与强碱溶液反应的离子方程式是
②在高温条件下,将D、E组成的气态化合物与A 的粉末充分反应,生成8g E的单质和相应的固态化合物时,放出akJ热量,此反应的热化学方程式是
③A的某种氯化物溶液呈黄色,它与B的单质的反应工业上常用于腐蚀电路板,请写出反应的离子方程式
您最近一年使用:0次
2019·安徽·二模
10 . 短周期元素X、Y、Z、W、R的原子序数依次增大,元素Y的一种单质可以保护地球上的生物免受紫外线的伤害;X与Z同主族且二者可形成离子化合物;W的最外层电子数与电子层数相同;Z与R可形成化合物Z2R,其水溶液呈碱性。下列说法错误的是
| A.R的一种氧化物与其氢化物反应生成R的单质 |
| B.Y与Ⅹ、Z、R均可分别形成至少两种二元化合物 |
| C.Z、W的最高价氧化物对应的水化物能相互反应 |
| D.工业上可通过分别电解Z、W的熔融氯化物冶炼出它们的单质 |
您最近一年使用:0次



