1 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近半年使用:0次
2022-06-10更新
|
13590次组卷
|
46卷引用:上海行知中学 2023-2024学年高三上学期第一次月考化学试题
上海行知中学 2023-2024学年高三上学期第一次月考化学试题2022年新高考广东化学高考真题(已下线)2022年广东卷高考真题变式题(1-10)(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编(已下线)专题06 物质结构元素周期律-三年(2020-2022)高考真题分项汇编(已下线)第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)浙江省舟山中学2021-2022学年高一下学期学考考前质量检测化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第10练 元素周期律-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第16讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(全国通用)河南省郑州市第十九高级中学2022-2023学年高二上学期开学文理分科考试化学试题湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期第二次月考化学试题福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题广东省深圳市福田区红岭中学2022-2023学年高三上学期第一次统一考试化学试题(已下线)专题07 元素周期律与元素周期表(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)江西省南昌市第三中学2022-2023学年高一下学期3月月考化学试题天津市南开中学2022-2023学年高一下学期3月月考化学试题山东省菏泽市单县第二中学2022-2023学年高一下学期3月段考化学试题辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 (已下线)专题卷10 根据元素周期表片段和物质转化关系元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点05 元素周期律再熟悉-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第2讲 元素素周期表 元素周期律(已下线)热点题型训练 元素“位—构—性”的综合推断题(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷宁夏回族自治区中卫市中宁县第一中学2022-2023学年高三上学期10月月考化学试题广东省广州市越秀区2023-2024学年高二上学期开学考试化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏回族自治区石嘴山市平罗中学2023-2024学年高三上学期第四次月考理科综合试题河南省南阳市镇平县第一高级中学2023-2024学年高一下学期3月月考化学试题山东省高密市第一中学2023-2024学年高一下学期4月月考化学试题广东省汕头市潮阳实验学校2022-2023学年高一下学期第一次月考化学试题
真题
名校
2 . X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,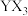 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
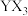 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是| A.X与Z形成的10电子微粒有2种 |
| B.Z与Q形成的一种化合物可用于饮用水的消毒 |
C.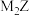 与 与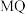 的晶体类型不同 的晶体类型不同 |
| D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性 |
您最近半年使用:0次
2022-06-14更新
|
9016次组卷
|
20卷引用:上海市建平中学2023届高三下学期3月月考化学试题
上海市建平中学2023届高三下学期3月月考化学试题2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题11-20(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第09练 原子结构与元素周期表-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第13讲 原子结构 化学键(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(练)-2023年高考化学一轮复习讲练测(全国通用)北京清华附中2022-2023学年高三上学期10月统练(三)化学试题(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题福建省厦门集美中学2022-2023学年高三上学期期中考试化学试题辽宁省沈阳市第二中学2022-2023学年高三上学期期中考试化学试题(已下线)江苏省南通市如皋市2022-2023学年高三上学期期末考试化学试题(已下线)专题07 元素周期律与元素周期表(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型10 物质结构与性质的综合分析与推断-高考必备50个题型(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
3 . W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。下列叙述正确的是
| A.非金属性:W> X>Y> Z | B.原子半径:Z>Y>X>W |
| C.元素X的含氧酸均为强酸 | D.Y的氧化物水化物为强碱 |
您最近半年使用:0次
2020-07-09更新
|
15783次组卷
|
63卷引用:上海市上海交通大学附属中学2020-2021学年高二上学期期中考试试题
上海市上海交通大学附属中学2020-2021学年高二上学期期中考试试题 上海市格致中学2022-2023学年高三上学期期中考试化学试题上海市实验学校2023届高三下学期3月月考化学试题2020年全国统一考试化学试题(新课标Ⅲ)陕西省延安市吴起高级中学2019-2020学年高一下学期第四次质量检测(期末)化学试题贵州省兴仁市凤凰中学2019-2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题(已下线)专题06 物质结构 元素周期律-2020年高考真题和模拟题化学分项汇编(已下线)第18讲 元素周期律和元素周期表(精讲)——2021年高考化学一轮复习讲练测(已下线)第17讲 原子结构 化学键(精讲)——2021年高考化学一轮复习讲练测河南省郑州市巩义市第四高级中学2021届高三上学期期中考试化学试题重庆市第七中学2021届高三上学期第一次月考化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)山西省长治市第二中学校2020-2021学年高二上学期第二次月考化学试题海南省北京师范大学万宁附属中学2019-2020学年高一下学期期末考试化学试题黑龙江省哈尔滨市第三十二中学2021届高三上学期期末考试化学试题 内蒙古四子王旗第一中学2021届高三上学期1月月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区(已下线)热点7 物质结构与元素周期律-2021年高考化学专练【热点·重点·难点】(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)专题04 物质结构和元素周期律——备战2021年高考化学纠错笔记(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练广西壮族自治区蒙山中学2020-2021学年高一下学期第一次月考化学试题河南省郑州市中牟县2020-2021学年高一下学期期中考试化学试题(已下线)押全国卷理综第10题 元素周期表元素周期律-备战2021年高考化学临考题号押题(课标全国卷)天津市实验中学滨海学校2021届高三上学期第一次月考化学试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题贵州省遵义市务川县汇佳中学2020-2021学年高二下学期第三次月考化学试题广西钦州市2020-2021学年高一下学期期末考试化学(文)试题(已下线)第16讲 元素周期律和元素周期表(精练)-2022年高考化学一轮复习讲练测(已下线)课时25 原子结构-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向16 元素周期表 元素周期律-备战2022年高考化学一轮复习考点微专题(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-练习2020年全国卷Ⅲ化学真题变式题广西梧州市2020-2021学年高一下学期第一次月考化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题(已下线)卷08 元素周期律-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点06 物质结构 元素周期律-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题06物质结构元素周期律-三年(2020~2022)高考真题汇编(全国卷)(已下线)第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第13讲 原子结构 化学键(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)内蒙古巴彦淖尔市临河区第三中学2021-2022学年高三上学期第二次阶段性测试理综化学试题四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题陕西省黄陵中学2021-2022学年高一下学期期中考试化学试题四川省成都东部新区养马中学2020-2021学年高一下学期期中考试化学试题(已下线)专题07 元素周期律与元素周期表(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型77 基于物质性质考查元素周期律山东省菏泽市单县第二中学2022-2023学年高一下学期3月段考化学试题(已下线)专题07 元素周期表与元素周期律(已下线)第2讲 元素素周期表 元素周期律云南省大理州实验中学2021-2022学年高二上学期化学期中考试题福建省漳州市第五中学2023-2024学年高一下学期第一次月考化学试卷
4 . 元素X、Y、Z和Q在周期表中的位置如图所示,其中元素Q位于第四周期,X、Y、Z原子的最外层电子数之和为17,下列说法不正确 的是
| X | |||
| Y | Z | ||
| Q |
| A.原子半径(r):r(Q)>r(Y)>r(Z) |
| B.元素X有 -4,+2、+4等多种价态 |
| C.Y、Z的氧化物对应的水化物均为强酸 |
| D.可以推测H3QO4是Q的最高价氧化物的水化物 |
您最近半年使用:0次
2018-11-07更新
|
4759次组卷
|
19卷引用:2019-2020学年上海各区(16区)高三化学一模选择题汇编-物质的组成与结构
2019-2020学年上海各区(16区)高三化学一模选择题汇编-物质的组成与结构上海市嘉定区2020届高三上学期一模化学试题2018年11月浙江省普通高校招生选考科目考试化学试题浙江省临海市白云高级中学2018-2019学年高一下学期3月月考化学试题辽宁省阜新市第二高级中学2018-2019学年高二下学期期末考试化学试题浙江省嘉兴市第一中学2020届高三上学期期中考试化学试题(已下线)【新东方】高中化学5025第1章原子结构与元素周期律 挑战区 模拟高考浙江省2019届高三11月选考科目考试化学试卷鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律第2节 元素周期律和元素周期表 方法帮 高考帮人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第二节 元素周期律 高考帮高一必修第一册(苏教2019)专题5 专题综合检测卷(已下线)【浙江新东方】在线化学 (23)(已下线)小题13 元素周期表、律(根据元素周期表片段推断) ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第10题 元素周期表元素周期律-备战2021年高考化学临考题号押题(课标全国卷)湖南省长沙市长郡中学2022届高三上学期第一次月考化学试题(已下线)专题07.物质结构 元素周期律-十年(2012-2021)高考化学真题分项汇编(浙江专用)浙江省绍兴市柯桥区2021-2022学年高一下学期期末(学考模拟)化学试题(已下线)专题07 元素周期表与元素周期律
名校
解题方法
5 . 短周期元素X、Y、Z、W原子序数依次增大。常温下,四种元素最高价氧化物对应水化物均能形成浓度为 的溶液,它们的
的溶液,它们的 分布如下图所示。下列说法正确的是
分布如下图所示。下列说法正确的是
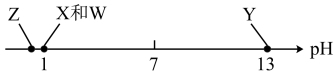
 的溶液,它们的
的溶液,它们的 分布如下图所示。下列说法正确的是
分布如下图所示。下列说法正确的是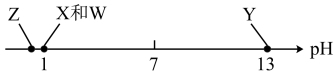
| A.X与W可能位于同一主族 |
B.最外层未成对电子数: |
| C.四种元素的简单离子中Y的半径最小 |
| D.四种元素的最高价氧化物对应水化物中Z的酸性最强 |
您最近半年使用:0次
2022-06-12更新
|
739次组卷
|
5卷引用:上海市虹口区2021-2022学年高三下学期学习能力诊断测试化学试题
上海市虹口区2021-2022学年高三下学期学习能力诊断测试化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(练)-2023年高考化学一轮复习讲练测(全国通用)广东省汕头市金山中学2022-2023学年高三上学期开学考试化学试题(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题河南省洛阳市第一高级中学2023-2024学年高三上学期开学摸底考试化学试题
6 . X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误的是
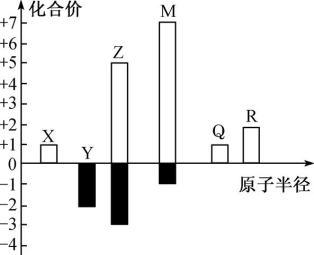

| A.X与Y组成的化合物中可能有非极性共价键 |
| B.X、Y、Z三种元素组成的化合物可能是酸、碱或盐 |
| C.简单离子半径:Q>Y |
| D.化合物R(YX)2是强碱 |
您最近半年使用:0次
22-23高一下·重庆沙坪坝·阶段练习
名校
解题方法
7 . W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足 ;化合物
;化合物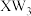 与WZ相遇会产生白烟。下列叙述正确的是
与WZ相遇会产生白烟。下列叙述正确的是
 ;化合物
;化合物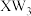 与WZ相遇会产生白烟。下列叙述正确的是
与WZ相遇会产生白烟。下列叙述正确的是| A.非金属性:W>X>Y>Z |
| B.原子半径:Z>Y>X>W |
| C.过量的X的简单氢化物与Z的单质,相遇也会产生白烟 |
| D.Y的最高价氧化物对应水化物为弱碱 |
您最近半年使用:0次
名校
解题方法
8 . 百余种不同的元素,是构成大千世界中所有物质的“基石”。科学家们根据元素的性质递变规律、电子排布规律等对元素进行编排设计元素周期表。请根据所学内容回答下列问题:
(1)地壳中含量最多的元素的基态原子的轨道表示式是___________ ,能量最高的电子所在的轨道呈___________ 形。
(2) 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是___________ 。
(3)研究发现,正离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是___________ 。
(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填___________ (填“有”或“无”)该元素在元素周期表中的位置:第___________ 周期,第___________ 族,该周期共有___________ 种元素。
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
预测X值的区间:___________ ;上表中五种元素的第一电离能由大到小的顺序是___________ 。(写元素符号)
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态 原子的外围电子排布式为
原子的外围电子排布式为___________ ; 位于周期表中
位于周期表中___________ 区,基态 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(7) 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是___________ 。
(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
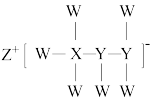
(1)地壳中含量最多的元素的基态原子的轨道表示式是
(2)
 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是(3)研究发现,正离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 |  , , |  , , |  , , |  |  |
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态
 原子的外围电子排布式为
原子的外围电子排布式为 位于周期表中
位于周期表中 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
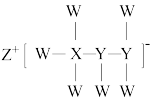
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.Y的最高化合价氧化物的水化物为强酸 |
D.X的氟化物 中原子均为8电子稳定结构 中原子均为8电子稳定结构 |
您最近半年使用:0次
21-22高三上·山东济宁·期中
名校
9 . 下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。请回答下列问题:
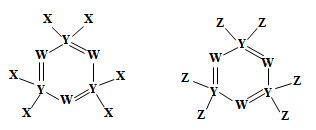
(1)元素Y在周期表中的位置为___________ ,元素Z的最高价氧化物的水化物的化学式为_____ 。
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为_____ 。
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为_____ 。
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
(5)许多含元素Z的化合物均可作为杀菌消毒剂,将ZO2通入到NaOH和H2O2混合溶液中,可制备NaZO2。
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式_____ 。
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,___________ ,___________ ,低于60℃干燥,得到NaZO2晶体 (补全实验步骤)。

(1)元素Y在周期表中的位置为
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
| A.比较其简单氢化物的沸点 | B.比较其单质与氢气反应的难易程度 |
| C.比较其简单阴离子的还原性 | D.比较其氧化物的水化物的酸性 |
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,
您最近半年使用:0次
名校
10 . 已知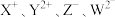 四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是
四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是
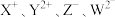 四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是
四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是A.原子半径: | B.原子序数: |
C.原子最外层电子数: | D.金属性: ,还原性: ,还原性: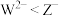 |
您最近半年使用:0次



