名校
解题方法
1 . 短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的某种化合物(如图所示)是一种优良的防龋齿剂(用于制含氟牙膏),其中Z元素的内层电子数之和为最外层电子数的2倍。下列说法错误的是
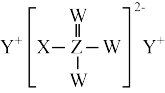
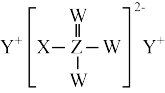
| A.Z的最高价氧化物对应的水化物为弱酸 | B.W、Y形成的化合物在熔融状态下能够导电 |
| C.X、Y形成的化合物为强电解质 | D.X、W、Z对应的单质熔沸点:X>W>Z |
您最近一年使用:0次
解题方法
2 . X、Q、Y、Z是核电荷数依次增大的1~18号元素,其信息如下:
(1)这四种元素的元素名称分别是X_______ ,Q_______ ,Y_______ ,Z_______ 。
(2)书写电子式: Y2-_______ ;Z+_______ 。离子半径大小为:Y2-_______ Z+(填“>” “<”或“=”),从原子结构角度说明原因_______ 。
(3)用一个化学反应方程式比较Q和碳元素的非金属性强弱:_______ 。
(4)QX3 能与硫酸生成盐类物质,请写出其中一种的化学式_______ , 请简述检验该盐中阳离子的方法_______ ,请写出该检验原理的离子方程式_______ 。
(5)从周期表说明Si可做半导体材料的原因:_______ 。
| 元素 | 信息 |
| X | X2是密度最小的气体。 |
| Q | 与X可形成QX3的10电子结构分子 |
| Y | 带两个负电荷的负离子与氖原子结构相同 |
| Z | 原子的M层电子层最多只能失去1个电子 |
| Si | 单质硅是一种常见的半导体材料 |
(2)书写电子式: Y2-
(3)用一个化学反应方程式比较Q和碳元素的非金属性强弱:
(4)QX3 能与硫酸生成盐类物质,请写出其中一种的化学式
(5)从周期表说明Si可做半导体材料的原因:
您最近一年使用:0次
名校
3 . 元素A-D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
(1)写出四种元素的元素符号:A___________ 、B___________ 、C___________ 、D___________ 。
(2)A原子最外层有___________ 个电子;写出D离子的结构示意图___________ 。
(3)比较A离子与D离子半径大小,并从原子结构角度说明___________ 。
(4)A的金属性比D强,写出能证明该结论的一个事实___________ 。
| A | B | C | D |
| 单质银白色,燃烧时火焰呈黄色。 | 其单质是空气的主要成分,化学性质非常稳定。 | 第三周期原子半径最小的元素(稀有气体除外)。 | +2价阳离子的核外电子数与氖原子相同。 |
(2)A原子最外层有
(3)比较A离子与D离子半径大小,并从原子结构角度说明
(4)A的金属性比D强,写出能证明该结论的一个事实
您最近一年使用:0次
名校
解题方法
4 . 第三周期元素X、Y、Z、W的最高价氧化物分别溶于水得溶液,0.010mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是( )


| A.Y可能是硅元素 |
| B.简单离子半径:Z>W>X |
| C.气态氢化物的稳定性:Y>W |
| D.非金属性:Y>Z |
您最近一年使用:0次
2020-01-04更新
|
333次组卷
|
7卷引用:上海市静安区2020届高三上学期第一次模拟考试化学试题
名校
解题方法
5 . 短周期主族元素 X、Y、Z、W 原子序数依次增大,X 原子的最外层有 6 个电子,Y 是迄今发现的非金属性最强的元素,在周期表中 Z 位于 IA 族,W 与 X 属于同一主族。下列说法正确的是( )
| A.熔沸点:Z2X<Z2W | B.元素最高价:Y<Z |
| C.气态氢化物的热稳定性:Y<W | D.原子半径:X<Y<Z<W |
您最近一年使用:0次
2020-02-14更新
|
258次组卷
|
4卷引用:上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题
上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题2019-2020学年上海各区(16区)高三化学一模选择题汇编-物质的组成与结构(已下线)二轮拔高卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)上海市久隆模范中学2022-2023学年高二上学期期末考试(等级考)化学试题
14-15高三上·上海宝山·阶段练习
名校
解题方法
6 . 有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子。下列说法中不正确的是


| A.X元素位于ⅥA | B.A能溶解于B中 |
| C.B的沸点大于C的沸点 | D.A和C不可能发生氧化还原反应 |
您最近一年使用:0次
真题
名校
7 . 短周期元素甲、乙、丙、丁的原子序数依次增大,甲和丁的原子核外均有两个未成对电子,乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应。下列说法错误的是
| A.元素丙的单质可用于冶炼金属 |
| B.甲与丁形成的分子中有非极性分子 |
| C.简单离子半径:丁 > 乙 > 丙 |
| D.甲与乙形成的化合物均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
1393次组卷
|
8卷引用:2015年全国普通高等学校招生统一考试化学(上海卷)
2015年全国普通高等学校招生统一考试化学(上海卷)2016届黑龙江省哈尔滨第六中学高三上期中测试化学试卷2016届山西省山西大学附属中学高三上12月月考化学试卷(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分四川省武胜烈面中学校2019-2020学年高二下学期期中考试化学试题江苏省南通市2023-2024学年高三下学期化学调研测试卷
8 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E 元素的周期序数与主族序数相等。
(1)E 元素在周期表中的位置___________ 。
(2)写出A2W2的电子式为____________ 。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式________ 。
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是_________ (标准状况下)。
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为_____________ 。
(1)E 元素在周期表中的位置
(2)写出A2W2的电子式为
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式
(4)元素D的单质在一定条件下,能与 A 单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,若将1molDA和1molE 单质混合加入足量的水,充分反应后成气体的体积是
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为
您最近一年使用:0次
2019-07-02更新
|
331次组卷
|
2卷引用:沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题3
11-12高三上·北京东城·期末
名校
9 . W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
| A.Y的低价氧化物与O3漂白的原理相同 |
| B.Y的氢化物和W2Y所含化学键的类型相同 |
| C.上述三种元素形成的简单离子,X离子半径最小 |
| D.工业上常用电解相应的盐溶液制备W、X的单质 |
您最近一年使用:0次
2016-12-09更新
|
843次组卷
|
9卷引用:2014届上海市十三校高三12月联考化学试卷
(已下线)2014届上海市十三校高三12月联考化学试卷(已下线)2011届北京市东城区高三第一学期期末考试化学试卷(已下线)2013届湖南省蓝山二中高三第五次月考化学试卷【全国百强校】黑龙江省哈尔滨市第三中学校2019届高三上学期第一次调研考试化学试题河北省隆化县存瑞中学2019届高三上学期第一次质检化学试题【全国百强校】吉林省实验中学2019届高三上学期第三次月考化学试题【全国百强校】宁夏回族自治区银川一中2019届高三上学期第五次月考理科综合化学试题重庆南开中学高2022届高一化学(必修2)物质结构元素周期律专题训练安徽省怀宁县新安中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
10 . W、X、Y、Z均为短周期元素,X、W可形成两种液态化合物甲和乙,其原子个数比分别为1∶1(甲)和2∶1(乙),且分子中电子总数分别为18(甲)和10(乙)。X与Z能形成一种极易溶于水的碱性气体丙X与Y能形成极易溶于水的酸性气体丁,丁分子中的电子数为18。X、Y、Z能形成一种离子化合物,其水溶液呈弱酸性。请写出:
(1)W的元素符号___ ,其核外共有___ 种运动状态不同的电子。
(2)甲物质的结构式为___ ;乙物质的空间构型为___ 。
(3)Z元素核外共有___ 种能量不同的电子,碱性气体甲的电子式为___ 。
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是___ 。
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为___ 。
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因___ 。
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。___ 。
(1)W的元素符号
(2)甲物质的结构式为
(3)Z元素核外共有
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。
您最近一年使用:0次



