1 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
2022-06-10更新
|
14008次组卷
|
46卷引用:上海行知中学 2023-2024学年高三上学期第一次月考化学试题
上海行知中学 2023-2024学年高三上学期第一次月考化学试题湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期第二次月考化学试题福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题广东省深圳市福田区红岭中学2022-2023学年高三上学期第一次统一考试化学试题江西省南昌市第三中学2022-2023学年高一下学期3月月考化学试题天津市南开中学2022-2023学年高一下学期3月月考化学试题山东省菏泽市单县第二中学2022-2023学年高一下学期3月段考化学试题宁夏回族自治区中卫市中宁县第一中学2022-2023学年高三上学期10月月考化学试题宁夏回族自治区石嘴山市平罗中学2023-2024学年高三上学期第四次月考理科综合试题河南省南阳市镇平县第一高级中学2023-2024学年高一下学期3月月考化学试题山东省高密市第一中学2023-2024学年高一下学期4月月考化学试题广东省汕头市潮阳实验学校2022-2023学年高一下学期第一次月考化学试题 2022年新高考广东化学高考真题(已下线)2022年广东卷高考真题变式题(1-10)(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编(已下线)专题06 物质结构元素周期律-三年(2020-2022)高考真题分项汇编(已下线)第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)浙江省舟山中学2021-2022学年高一下学期学考考前质量检测化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第10练 元素周期律-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第16讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(全国通用)河南省郑州市第十九高级中学2022-2023学年高二上学期开学文理分科考试化学试题(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题(已下线)专题07 元素周期律与元素周期表(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 (已下线)专题卷10 根据元素周期表片段和物质转化关系元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点05 元素周期律再熟悉-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第2讲 元素素周期表 元素周期律(已下线)热点题型训练 元素“位—构—性”的综合推断题(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷广东省广州市越秀区2023-2024学年高二上学期开学考试化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
真题
名校
2 . X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,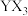 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
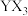 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是
分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是| A.X与Z形成的10电子微粒有2种 |
| B.Z与Q形成的一种化合物可用于饮用水的消毒 |
C.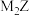 与 与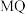 的晶体类型不同 的晶体类型不同 |
| D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性 |
您最近一年使用:0次
2022-06-14更新
|
9177次组卷
|
20卷引用:上海市建平中学2023届高三下学期3月月考化学试题
上海市建平中学2023届高三下学期3月月考化学试题北京清华附中2022-2023学年高三上学期10月统练(三)化学试题2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题11-20(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第09练 原子结构与元素周期表-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第13讲 原子结构 化学键(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题福建省厦门集美中学2022-2023学年高三上学期期中考试化学试题辽宁省沈阳市第二中学2022-2023学年高三上学期期中考试化学试题(已下线)江苏省南通市如皋市2022-2023学年高三上学期期末考试化学试题(已下线)专题07 元素周期律与元素周期表(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型10 物质结构与性质的综合分析与推断-高考必备50个题型(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
3 . W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。下列叙述正确的是
| A.非金属性:W> X>Y> Z | B.原子半径:Z>Y>X>W |
| C.元素X的含氧酸均为强酸 | D.Y的氧化物水化物为强碱 |
您最近一年使用:0次
2020-07-09更新
|
15926次组卷
|
63卷引用:上海市实验学校2023届高三下学期3月月考化学试题
上海市实验学校2023届高三下学期3月月考化学试题重庆市第七中学2021届高三上学期第一次月考化学试题山西省长治市第二中学校2020-2021学年高二上学期第二次月考化学试题内蒙古四子王旗第一中学2021届高三上学期1月月考化学试题广西壮族自治区蒙山中学2020-2021学年高一下学期第一次月考化学试题天津市实验中学滨海学校2021届高三上学期第一次月考化学试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题贵州省遵义市务川县汇佳中学2020-2021学年高二下学期第三次月考化学试题上海市上海交通大学附属中学2020-2021学年高二上学期期中考试试题 广西梧州市2020-2021学年高一下学期第一次月考化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题内蒙古巴彦淖尔市临河区第三中学2021-2022学年高三上学期第二次阶段性测试理综化学试题上海市格致中学2022-2023学年高三上学期期中考试化学试题山东省菏泽市单县第二中学2022-2023学年高一下学期3月段考化学试题福建省漳州市第五中学2023-2024学年高一下学期第一次月考化学试卷2020年全国统一考试化学试题(新课标Ⅲ)陕西省延安市吴起高级中学2019-2020学年高一下学期第四次质量检测(期末)化学试题贵州省兴仁市凤凰中学2019-2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题(已下线)专题06 物质结构 元素周期律-2020年高考真题和模拟题化学分项汇编(已下线)第18讲 元素周期律和元素周期表(精讲)——2021年高考化学一轮复习讲练测(已下线)第17讲 原子结构 化学键(精讲)——2021年高考化学一轮复习讲练测河南省郑州市巩义市第四高级中学2021届高三上学期期中考试化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)海南省北京师范大学万宁附属中学2019-2020学年高一下学期期末考试化学试题黑龙江省哈尔滨市第三十二中学2021届高三上学期期末考试化学试题 (人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区(已下线)热点7 物质结构与元素周期律-2021年高考化学专练【热点·重点·难点】(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)专题04 物质结构和元素周期律——备战2021年高考化学纠错笔记(已下线)解密05 物质结构元素周期律(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练河南省郑州市中牟县2020-2021学年高一下学期期中考试化学试题(已下线)押全国卷理综第10题 元素周期表元素周期律-备战2021年高考化学临考题号押题(课标全国卷)广西钦州市2020-2021学年高一下学期期末考试化学(文)试题(已下线)第16讲 元素周期律和元素周期表(精练)-2022年高考化学一轮复习讲练测(已下线)课时25 原子结构-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向16 元素周期表 元素周期律-备战2022年高考化学一轮复习考点微专题(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-练习2020年全国卷Ⅲ化学真题变式题(已下线)卷08 元素周期律-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点06 物质结构 元素周期律-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题06物质结构元素周期律-三年(2020~2022)高考真题汇编(全国卷)(已下线)第07练 以元素“位—构—性”综合推断突破元素周期表、律-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第13讲 原子结构 化学键(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题陕西省黄陵中学2021-2022学年高一下学期期中考试化学试题四川省成都东部新区养马中学2020-2021学年高一下学期期中考试化学试题(已下线)专题07 元素周期律与元素周期表(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型77 基于物质性质考查元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第2讲 元素素周期表 元素周期律云南省大理州实验中学2021-2022学年高二上学期化学期中考试题
名校
解题方法
4 . X、Y、Z、R、T为短周期主族元素,其中R原子的最外层电子数是电子层数的2倍;Y与Z能形成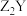 、
、 型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断不正确的是
型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断不正确的是
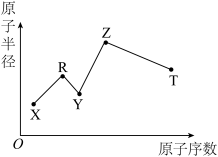
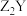 、
、 型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断不正确的是
型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断不正确的是
A.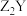 和 和 的阴阳离子个数比相同 的阴阳离子个数比相同 |
| B.简单氢化物的稳定性:Y<T |
| C.最高价氧化物对应水化物的酸性:T>R |
| D.由X、Y、Z、T四种元素组成的常见化合物溶液显酸性 |
您最近一年使用:0次
2024-02-11更新
|
274次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期11月考化学试卷
21-22高三上·山东济宁·期中
名校
5 . 下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。请回答下列问题:
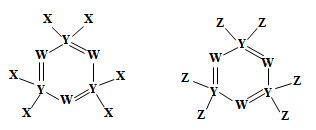
(1)元素Y在周期表中的位置为___________ ,元素Z的最高价氧化物的水化物的化学式为_____ 。
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为_____ 。
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为_____ 。
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
(5)许多含元素Z的化合物均可作为杀菌消毒剂,将ZO2通入到NaOH和H2O2混合溶液中,可制备NaZO2。
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式_____ 。
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,___________ ,___________ ,低于60℃干燥,得到NaZO2晶体 (补全实验步骤)。

(1)元素Y在周期表中的位置为
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
| A.比较其简单氢化物的沸点 | B.比较其单质与氢气反应的难易程度 |
| C.比较其简单阴离子的还原性 | D.比较其氧化物的水化物的酸性 |
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,
您最近一年使用:0次
名校
6 . 已知X、Y和Z三种元素的原子序数之和等于42,X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X与Y可形成化合物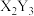 ,Z元素可形成负一价离子。下列说法正确的是
,Z元素可形成负一价离子。下列说法正确的是
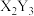 ,Z元素可形成负一价离子。下列说法正确的是
,Z元素可形成负一价离子。下列说法正确的是A.X元素基态原子的价电子排布式为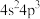 |
| B.X元素是第四周期第VA族元素 |
C.Y元素原子的轨道表示式为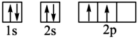 |
| D.Z元素的单质在氧气中不能燃烧 |
您最近一年使用:0次
2023-12-29更新
|
176次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期9月月考化学试卷
名校
解题方法
7 . W、X、Y、Z、Q五种元素的原子结构与性质如表所示,其中前四种是常见的短周期主族元素。回答下列问题:
(1)W在元素周期表中的位置为___________ ,写出其基态原子的轨道表示式___________ 。
(2) 与足量的
与足量的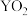 的水溶液发生反应生成两种强酸,该反应的化学方程式为
的水溶液发生反应生成两种强酸,该反应的化学方程式为___________ 。将足量单质X通入含有2mol 溶液中充分反应,转移电子的数目为
溶液中充分反应,转移电子的数目为___________ ( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(3)与Q同周期的元素的基态原子中,最外层电子数与Q原子相同的元素有哪些?___________
(4)将W、X、Y、Z的简单离子,按照微粒半径由小到大的顺序排列___________ (用元素符号表示)
(5)关于元素Z的判断,正确的是___________
(6)Z元素的一种相邻元素,其基态原子的轨道表示式是下图中的___________ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合___________ (填字母)。

A.能量最低原理 B.泡利原理 C.洪特规则 D.构造原理
(7)对于基态Q原子,下列叙述正确的是___________。
(8)阅读以下核电荷数为21-25的元素的最高正化合价,回答下列问题:
对比上述五种元素原子的核外电子排布与元素的最高正化合价,你发现的规律是___________
| 元素编号 | 元素的性质与原子结构 |
| W | 基态原子有5个原子轨道填充有电子,有3个未成对电子 |
| X | 最外层电子数为奇数的第三周期元素,其气态氢化物遇W的气态氢化物产生大量白烟 |
| Y | 基态原子有16个不同运动状态的电子 |
| Z | 周期数=族序数,简单离子最外层电子数为8 |
| Q | 基态原子在前四周期中未成对电子数最多 |
(2)
 与足量的
与足量的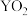 的水溶液发生反应生成两种强酸,该反应的化学方程式为
的水溶液发生反应生成两种强酸,该反应的化学方程式为 溶液中充分反应,转移电子的数目为
溶液中充分反应,转移电子的数目为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(3)与Q同周期的元素的基态原子中,最外层电子数与Q原子相同的元素有哪些?
(4)将W、X、Y、Z的简单离子,按照微粒半径由小到大的顺序排列
(5)关于元素Z的判断,正确的是___________
| A.Z元素的焰色反应为黄色 |
| B.Z元素最高价氧化物对应水化物为强碱 |
| C.Z元素的第一电离能高于同周期左右相邻元素 |
| D.Z元素在失去第三个电子之后,电离能发生突变 |

A.能量最低原理 B.泡利原理 C.洪特规则 D.构造原理
(7)对于基态Q原子,下列叙述正确的是___________。
| A.因为轨道处于半充满时体系总能量低,所以Q核外电子排布结果中未成对电子数最多。 |
| B.因为4s电子能量较高,一定在比3s电子离核更远的地方运动 |
| C.Q电负性比钾高,原子对键合电子的吸引力比钾大 |
| D.Q的价电子排布与钾原子相同 |
| 元素名称 | 钪 | 钛 | 钒 | 铬 | 锰 |
| 元素符号 | Sc | Ti | V | Cr | Mn |
| 核电荷数 | 21 | 22 | 23 | 24 | 25 |
| 最高正价 | +3 | +4 | +5 | +6 | +7 |
您最近一年使用:0次
真题
名校
8 . X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是
| A.X的原子半径一定大于Y的原子半径 |
| B.X与Y的简单离子不可能具有相同的电子层结构 |
| C.两元素形成的化合物中,原子个数比不可能为1 :1 |
| D.X2Y可能是离子化合物,也可能是共价化合物 |
您最近一年使用:0次
2019-01-30更新
|
2132次组卷
|
48卷引用:上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题1
上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题1上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题2上海交通大学附属中学2017-2018学年高二上学期第一次月考化学试题上海市交通大学附属中学2017-2018学年高二上学期第一次月考化学试题3(已下线)上海市上海交通大学附属中学2017-2018学年高二10月月考化学试题(已下线)2014届上海市长宁区高三上学期期末(一模)考试化学试卷2014-2015陕西省宝鸡市扶风高中高一4月月考化学试卷2016届河北省行唐启明中学高三上学期12月月考化学试卷2015-2016学年山西省右玉一中高二5月月考化学试卷2015-2016学年福建省南平市建瓯二中高一下学期第一次月考化学试卷2015-2016学年山西省朔州市右玉一中高二下5月月考化学试卷2017届河北省定州中学高三上第一次月考化学试卷宁夏石嘴山市第三中学2016-2017学年高一下学期第二次(5月)月考化学试题上海市高二上学期第二章《初识元素周期律》综合测试题河北省宣化市第一中学2019-2020学年高一11月月考化学试题安徽省滁州市明光市明光中学2019-2020高一下学期第二次月考化学试题上海市曹杨第二中学2021-2022学年高二上学期期末考试化学试题2007年普通高等学校招生全国统一考试(北京卷)理综化学部分(已下线)2010-2011学年辽宁省师大附中高一下学期期中考试化学试卷(已下线)2010-2011年北京市师大附中高一下学期期中考试化学试卷(已下线)2011-2012学年福建省南安一中高一下学期期末考试化学试卷(已下线)2011-2012学年甘肃省武威五中高一下学期期末考试化学试卷(已下线)2012-2013学年北京市房山区房山中学高一下学期期中考试化学试卷(已下线)2012-2013学年云南省昆明三中高一下学期期末考试文科化学试卷(已下线)2012-2013学年山东省菏泽市牡丹区高一下学期期末考试化学试卷(已下线)2012-2013学年北京市西城区(南区)高一下学期期末考试化学试卷2015-2016学年福建省厦门六中高一下学期期中化学试卷2015-2016学年河北省唐山一中高一下期中化学试卷2015-2016学年河北省广平县一中高一下学期期中考试化学试卷2015-2016学年江苏省宿迁市沭阳县高一下学期期中考试化学试卷2015-2016学年山西省长治一中高一平行班下期中化学试卷2015-2016学年重庆一中高一下期末化学试卷12015-2016学年陕西省西安七十中高一下学期期末化学试卷2015-2016学年重庆一中高一下期末化学试卷2河北省张家口市第一中学2016-2017学年高一下学期期中考试(实验班、普通班)(文)化学试题陕西省西安市碑林区西安建筑科技大学附属中学2016-2017学年高一下学期期末考试化学试题山东省惠民县第一中学2018-2019学年高一下学期联考化学试题湖南省湘南中学2018-2019学年高一下学期期中考试化学试题吉林省长春市九台区第四中学2018-2019学年高一下学期期中考试化学试题2020届高三化学选修三二轮专题复习—— 离子键、离子化合物专题1微观结构与物质的多样性易错疑难集训(二)河北省唐山遵化市2018-2019学年高一下学期期中考试化学试题高一必修第一册(苏教2019版)专题5 易错疑难集训(二)安徽省池州市东至二中2020-2021学年高二下学期开年考化学试题(已下线)第1章 物质结构 元素周期律(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)江西省抚州市南城一中2020-2021学年高一下学期5月月考化学试题(已下线)专题5 微观结构与物质的多样性 综合评价(2)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)四川省眉山市仁寿县2023-2024学年高一上学期1月期末化学试题
名校
解题方法
9 . 短周期主族元素W、X、Y、Z的原子序数依次增大,某研究团队以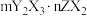 (固态物质)为载体,利用Au-Pd纳米颗粒催化气态单质W2、X2合成W2X2,其原理如图所示。下列说法错误的是
(固态物质)为载体,利用Au-Pd纳米颗粒催化气态单质W2、X2合成W2X2,其原理如图所示。下列说法错误的是
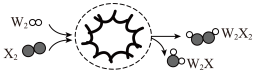
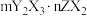 (固态物质)为载体,利用Au-Pd纳米颗粒催化气态单质W2、X2合成W2X2,其原理如图所示。下列说法错误的是
(固态物质)为载体,利用Au-Pd纳米颗粒催化气态单质W2、X2合成W2X2,其原理如图所示。下列说法错误的是
| A.简单离子半径:X>Y | B.化合物ZW4中原子均满足最外层8电子结构 |
| C. Y2X3、ZX2均具有较高熔点 | D.工业上常用电解熔融Y2X3的方法冶炼Y |
您最近一年使用:0次
名校
解题方法
10 . 图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A.原子半径:Z>Y>X |
| B.气态氢化物稳定性:R<W |
| C.WX3和水反应生成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
您最近一年使用:0次
2020-03-25更新
|
684次组卷
|
47卷引用:上海市行知中学2021届高三下学期3月月考化学试题
上海市行知中学2021届高三下学期3月月考化学试题(已下线)2014届上海市长宁区高三上学期期末(一模)考试化学试卷(已下线)2014届江西省南昌一中、南昌十中高三上学期联考化学试卷2014-2015学年河北省广平县第一中学高一4月月考理科化学试卷2015-2016学年上海市理工大学附属中学高二上学期期中测试化学试卷2015-2016学年河北省定兴三中高一下3月月考(文)化学试卷辽宁省葫芦岛高级中学2015-2016学年高一下第一次月考化学卷2015-2016学年陕西西安长安一中高一下第一次月考化学卷2015-2016学年福建省清流一中高一实验班下第三段测化学试卷2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷2016-2017学年江西省南昌市第二中学高一下学期第一次月考化学试卷2016-2017学年上海市金山区高三上期期末质量调研化学试卷山西省大同市第一中学2017-2018学年高一3月月考化学试题福建省莆田第六中学2017-2018学年高一6月月考B化学试题山西省实验中学2017-2018学年高一下学期第一次月考化学试题安徽省砀山县第二中学2018-2019学年高一下学期第一次月考化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高二下学期4月月考化学试题上海市向明中学2018-2019学年高二第一学期期末考试化学试题(已下线)上海市宝山区2014届高三上学期期末教学质量监测化学试题上海市宝山区交大附中2017-2018学年高三上学期期中考试化学试题江苏省苏州市西安交通大学苏州附属中学2019-2020学年高一下学期自主检测化学试题山西省运城市永济涑北中学2019-2020学年高一下学期3月月考化学试题(已下线)2011-2012年黑龙江龙东地区高一下学期期末考试化学试卷(已下线)2011-2012学年吉林省长春市十一高中高一下学期期末考试化学试卷(已下线)2013届黑龙江省大庆实验中学高三上学期开学考试化学试卷(已下线)2012-2013学年湖北省黄冈中学高二上学期期中考试化学试卷(已下线)2012-2013学年四川省成都外国语学校高一下学期期中考试化学试卷(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2013届山东省泰安市高三第二轮复习质量检测理综化学试卷(已下线)2014年高考化学一轮复习课后规范训练5-2练习卷(已下线)2013-2014湖北省黄石市三中高一下学期期中考试化学试卷2014-2015学年吉林省长春市十一中高一下期中化学试卷2014-2015学年内蒙古霍林郭勒市第三中学高一下期中考试化学试卷2014-2015学年福建省永春美岭中学高一下学期期中考试化学试卷2015-2016学年江苏省清江中学高一下学期周练化学试卷2015-2016学年河南省周口市商水一中高一下学期期中考试化学试卷河北省石家庄市第一中学2016-2017学年高一下学期期中考试化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题(已下线)【新东方】2020-82广东省茂名市信宜中学2019-2020学年高一下学期级线上段考化学试题北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题(已下线)5.1.2 元素周期表 元素周期表的应用练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)第04章 物质结构 元素周期律(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)第18讲 元素周期律和元素周期表(精练)-2021年高考化学一轮复习讲练测甘肃省会宁县第一中学2020-2021学年高一下学期期中考试化学试题河南省洛阳市2021-2022学年高一上学期期末考试化学试题



