名校
1 . I.金属在生活中有着广泛的应用,人们甚至根据使用材料的种类,将人类漫长的历史分为了三个大的时代,分别是石器时代、青铜器时代,而后是铁器时代,直到19世纪早期,戴维组装了一个特别大的电池用于实验,先后发现了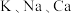 等许多金属。
等许多金属。
(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
(2)1827年维勒用金属钾还原熔融的无水氯化铝得到较纯的金属铝单质,但今天人们早已舍弃这种制备金属铝的方法,你认为可能的原因有_______ (写出一种合理原因即可)。写出现代工业上获得金属铝的化学反应方程式_______ 。
(3)已知铍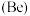 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。
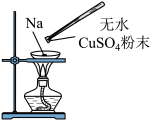
(4)钠是一种活泼的金属,将绿豆大的钠块投入如图所示的烧杯中,可能出现的现象_______。

(5)在蒸发皿中放一小块钠,加热至熔化成小球时,用玻璃棒蘸取少量无水 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
(6)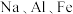 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。
(7)类推的思维方法在化学学习中有时会产生错误结论,因此结论最终要经过实践的检验,才能决定其正确与否,下列几种关于金属的类推结论中,错误的是_______。
①钠与水反应生成 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③ 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④ 受热易分解,
受热易分解,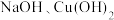 受热也易分解
受热也易分解
(8)单质A的燃烧热大。已知A为短周期元素,其气态原子逐个失去1~4个电子所需吸收能量如表所示。若该原子核外电子有三层,则该元素位于周期表_______ 族,写出A燃烧后形成的氧化物的电子式:_______ 。
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应: 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。
(9)根据上述反应,固体质量每减轻 ,将产生
,将产生
_______ L(S.T.P)。
(10)上述反应形成的固体混和物中, 不可能是_______。
不可能是_______。
(11) 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式_______ 。
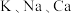 等许多金属。
等许多金属。(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
| A.地壳中金属元素的含量 | B.金属的延展性 |
| C.金属的导电性 | D.金属活泼性的差异 |
(3)已知铍
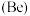 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。| A.铍遇冷水剧烈反应 | B.氧化铍的化学式为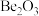 |
| C.氢氧化铍能与氢氧化钠溶液反应 | D. 能置换出 能置换出 中的镁单质 中的镁单质 |

| A.钠块在煤油、水两液体界面处反应,上下跳动,水层变红 |
| B.钠块只在煤油层中游动,并放出气体 |
| C.钠块只在水层中游动,钠块熔化,水层变红 |
| D.钠块在四氯化碳、水两液体界面处反应,熔化成小球并上下跳动,水层变红 |
 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
| A.钠受热易熔成小球说明其熔点低 |
B.钠与 粉末反应时放出大量热 粉末反应时放出大量热 |
C.一定条件下, 可与 可与 反应生成 反应生成 |
D.将无水 粉末改为 粉末改为 溶液,反应现象相同 溶液,反应现象相同 |
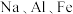 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。| A.三者的最高价氧化物对应水化物均为碱性 | B.三者的氢氧化物都是白色固体 |
| C.三者的氯化物都可用化合反应制得 | D.三者的单质在空气中最终都生成氧化物 |
①钠与水反应生成
 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③
 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④
 受热易分解,
受热易分解,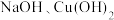 受热也易分解
受热也易分解| A.①② | B.③④ | C.①②③ | D.①②③④ |
 |  |  |  | …后续省略 | |
电离能( ) ) | 738 | 1451 | 7733 | 10540 | … |
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应:
 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。(9)根据上述反应,固体质量每减轻
 ,将产生
,将产生
(10)上述反应形成的固体混和物中,
 不可能是_______。
不可能是_______。| A.21∶9 | B.21∶7.5 | C.21∶5 | D.21∶8 |
 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
您最近一年使用:0次
名校
2 . 有H、C、O、Na、Mg、Al、P、Cl、Ar等9种元素或它们的原子。如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:(1)原子核对核外电子的吸引力(2)形成稳定结构的倾向。下表是一些气态原子失去核外不同电子所需的能量( ):
):
(1)通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______ 。
(2)表中X可能为以上9种元素中的_______ (填写元素符号)元素。用元素符号表示X和地壳中含量占第一位的元素形成化合物的化学式_______ 。
(3)Y是周期表中_______ 族元素。
(4)以上9种元素中,_______ (填写字母)元素原子失去核外第一个电子需要的能量最多。
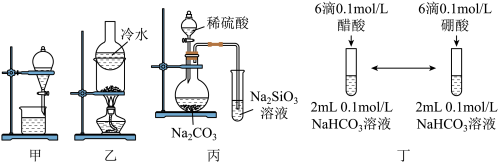
(5)下列实验装置符合题意且能达到相应实验目的的是_______。
 ):
):| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
(2)表中X可能为以上9种元素中的
(3)Y是周期表中
(4)以上9种元素中,
(5)下列实验装置符合题意且能达到相应实验目的的是_______。

A.装置甲利用 提取苯中溶解的 提取苯中溶解的 |
B.装置乙分离 和 和 固体 固体 |
| C.装置丙验证非金属性S>C>Si(已知硅酸不溶于水) |
| D.装置丁比较醋酸与硼酸酸性(已知酸性醋酸>碳酸) |
您最近一年使用:0次
名校
3 . 下列各元素中,一定属于主族元素的是
| A.最高价氧化物是酸性氧化物 |
| B.原子最外层电子数为2 |
| C.能形成+7价的含氧酸及其盐 |
| D.简单阴离子最外层满足8个电子稳定结构 |
您最近一年使用:0次
2021-12-24更新
|
379次组卷
|
5卷引用:上海市长宁区2022届高三一模化学试题
上海市长宁区2022届高三一模化学试题(已下线)一轮巩固卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)上海市七宝中学 2021-2022学年高一下学期期中考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第16讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(全国通用)
名校
解题方法
4 . 某短周期元素X的最高价是+6,X的氢化物的化学式是
| A.HX | B.H2X | C.XH3 | D.XH4 |
您最近一年使用:0次
名校
5 . A、B、C、D、E五种原子序数均小于18的元素,且原子序数依次增大,其中B与C的电子层数相同,D与E的电子层数相同,A与D的最外层电子数相同,C与E的最外层电子数相同,E元素的原子最外层电子数是电子层数的2倍,D与其他具有相同电子层数的原子相比半径最大。又知由B元素组成的单质是空气中的主要成分。
(1)B的元素名称是_______ ,该元素的原子结构示意图为_______ ,核外有___ 个未成对电子,用电子式表示B的简单氢化物的形成过程_________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是________ (用离子符号表示)。
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)_____ 。
(4)以下说法正确的是________ 。
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
(1)B的元素名称是
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)
(4)以下说法正确的是
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
您最近一年使用:0次
2024-01-21更新
|
131次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期期末考试化学试题
6 . 火星气体及岩石中富含X、Y、Z、W四种元素。已知:X、Y、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,X、W为同一主族元素,Y为地壳中含量最高的元素,火星岩石含有W的最高价化合物:Z2WY3,下列判断正确的是
| A.原子半径:Z>W>Y>X |
| B.W位于元素周期表第三周期VIIA族 |
| C.最高价氧化物对应水化物的酸性:W>X |
| D.X、Y、Z形成的化合物熔融状态下能够导电 |
您最近一年使用:0次
名校
解题方法
7 . W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y的周期数是族序数的3倍;X与Z同主族。下列叙述正确的是
| A.Y与X形成的化合物都只含有离子键 |
| B.X与Z形成的化合物的排放会导致酸雨 |
| C.四种元素的简单离子具有相同的电子层结构 |
| D.Z的氧化物对应的水化物均为强酸 |
您最近一年使用:0次
2021-04-30更新
|
324次组卷
|
4卷引用:上海市市西中学2021-2022学年高三下学期 4月月考(期中)化学试题
上海市市西中学2021-2022学年高三下学期 4月月考(期中)化学试题广东省普宁市华美实验学校2020-2021学年高一下学期期中考试化学试题(已下线)专题01 硫及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)广东省普宁市2020-2021学年高一下学期期中考试化学试题
22-23高一下·上海浦东新·期中
名校
8 . X、Y、Z、W为原子序数依次增大的短周期主族元素。Y、Z的单质常温下均为气体,W的单质可用于饮用水消毒。由X、Y、Z、W组成的某化合物结构如图所示,分子中所有原子均达到8电子稳定结构。下列说法正确的是
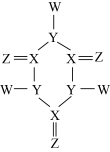
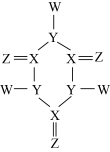
| A.元素非金属性:X>Y>Z |
| B.氧化物对应的水化物的酸性:W>X |
| C.氢元素与X、Y、Z均能形成两种或两种以上的二元化合物 |
D.Z元素气态氢化物的沸点比 低 低 |
您最近一年使用:0次
名校
9 . Q、R、X、Y、Z、A是原子序数依次增大的短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小(不包括稀有气体),R、X、Y三种元素的原子核外电子层数相同,同一周期中R的一种单质的熔点最高,Y与Q、R、X、Z均能形成多种常见化合物。元素A、Y在周期表中位于同一主族。
(1)X原子核外有_______ 种不同形状的电子云。这六种元素中,最外层有两个未成对电子的元素是_______ (用元素符号表示)。
(2)Q分别与X、Y形成的最简单化合物的稳定性_______ >_______ (用分子式表示)。
(3)Q与R两元素组成的分子构型可能是_______(填写序号)。
(4)化合物 和
和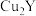 可发生如下转化(其中D是淀粉水解的最终产物):
可发生如下转化(其中D是淀粉水解的最终产物):
Cu2A 澄清溶液
澄清溶液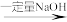 悬浊液
悬浊液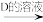 Cu2Y
Cu2Y
澄清溶液呈_______ 色,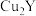 显
显_______ 色。
 的氧化性随pH的减小而增大。其在酸性介质中还原产物是
的氧化性随pH的减小而增大。其在酸性介质中还原产物是 ;在中性或碱性介质中还原产物主要是
;在中性或碱性介质中还原产物主要是 。
。
(5)应该在_______ (选填“酸性”、“碱性”或“中性”)介质中制备 。
。
(6)三氯乙烯 是地下水有机污染物的主要成分,研究显示在地下水中加入
是地下水有机污染物的主要成分,研究显示在地下水中加入 溶液可将其中的三氯乙烯除去,氧化产物只有
溶液可将其中的三氯乙烯除去,氧化产物只有 ,完成反应的化学方程式
,完成反应的化学方程式_______
_______ _______
_______ _______KCl+_______
_______KCl+_______ _______
_______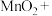 _______HCl
_______HCl
(7)加入过量的 才能将水中的三氯乙烯彻底除去。已知
才能将水中的三氯乙烯彻底除去。已知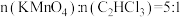 时,水样中的三氯乙烯基本完全去除。某地下水样品中三氯乙烯的质量浓度为
时,水样中的三氯乙烯基本完全去除。某地下水样品中三氯乙烯的质量浓度为 ,计算每处理
,计算每处理 该地下水,需
该地下水,需
_______ g。
(1)X原子核外有
(2)Q分别与X、Y形成的最简单化合物的稳定性
(3)Q与R两元素组成的分子构型可能是_______(填写序号)。
| A.直线型 | B.平面形 | C.三角锥形 | D.正四面体 |
 和
和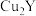 可发生如下转化(其中D是淀粉水解的最终产物):
可发生如下转化(其中D是淀粉水解的最终产物):Cu2A
 澄清溶液
澄清溶液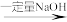 悬浊液
悬浊液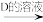 Cu2Y
Cu2Y澄清溶液呈
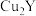 显
显 的氧化性随pH的减小而增大。其在酸性介质中还原产物是
的氧化性随pH的减小而增大。其在酸性介质中还原产物是 ;在中性或碱性介质中还原产物主要是
;在中性或碱性介质中还原产物主要是 。
。(5)应该在
 。
。(6)三氯乙烯
 是地下水有机污染物的主要成分,研究显示在地下水中加入
是地下水有机污染物的主要成分,研究显示在地下水中加入 溶液可将其中的三氯乙烯除去,氧化产物只有
溶液可将其中的三氯乙烯除去,氧化产物只有 ,完成反应的化学方程式
,完成反应的化学方程式_______
 _______
_______ _______KCl+_______
_______KCl+_______ _______
_______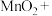 _______HCl
_______HCl(7)加入过量的
 才能将水中的三氯乙烯彻底除去。已知
才能将水中的三氯乙烯彻底除去。已知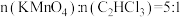 时,水样中的三氯乙烯基本完全去除。某地下水样品中三氯乙烯的质量浓度为
时,水样中的三氯乙烯基本完全去除。某地下水样品中三氯乙烯的质量浓度为 ,计算每处理
,计算每处理 该地下水,需
该地下水,需
您最近一年使用:0次
名校
10 . X、Y、Z、M为四种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L。下列说法正确的是
| A.原子半径比较:Z>Y>X>M |
| B.元素的氧化物对应的水化物的酸性比较:Z>Y>X |
| C.由Y、Z、M三种元素可形成一 种常见的离子化合物 |
| D.M2Z较稳定是由于分子间存在氢键 |
您最近一年使用:0次
2021-03-11更新
|
323次组卷
|
6卷引用:上海市奉贤区曙光中学2021-2022学年高一下学期期中检测化学试题
上海市奉贤区曙光中学2021-2022学年高一下学期期中检测化学试题浙江省宁波市2020-2021学年高一上学期期末九校联考化学试题(已下线)【浙江新东方】高中化学20210304-029湖南省武冈市第二中学2020-2021学年高一下学期开学考试化学试题云南省曲靖市会泽县茚旺高级中学2020-2021学年高一下学期3月月考化学试题(已下线)【浙江新东方】在线化学53高一上



