21-22高三上·山东济宁·期中
名校
1 . 下图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。请回答下列问题:
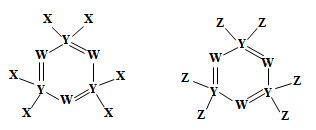
(1)元素Y在周期表中的位置为___________ ,元素Z的最高价氧化物的水化物的化学式为_____ 。
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为_____ 。
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为_____ 。
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
(5)许多含元素Z的化合物均可作为杀菌消毒剂,将ZO2通入到NaOH和H2O2混合溶液中,可制备NaZO2。
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式_____ 。
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,___________ ,___________ ,低于60℃干燥,得到NaZO2晶体 (补全实验步骤)。

(1)元素Y在周期表中的位置为
(2)元素W、X、Y、Z的简单阴离子半径由大到小的顺序为
(3)Z、W和氢三种元素形成的同时含有离子键和共价键化合物的电子式为
(4)研究Y、Z非金属性强弱的方案中不可行的是___________(填序号)。
| A.比较其简单氢化物的沸点 | B.比较其单质与氢气反应的难易程度 |
| C.比较其简单阴离子的还原性 | D.比较其氧化物的水化物的酸性 |
查阅资料:NaZO2晶体易溶于水,难溶于乙醇。NaZO2饱和溶液在温度低于38 ℃时析出NaZO2·3H2O晶体,高于38 ℃时析出NaZO2晶体,高于60 ℃时NaZO2分解成NaZO3和NaZ。
①写出由ZO2制备NaZO2的离子方程式
②从上述NaZO2溶液获得干燥的NaZO2晶体的操作步骤为:将溶液在减压和55 ℃条件下蒸发至大量晶体析出后,
您最近一年使用:0次
名校
2 . A、B、C、D、E五种原子序数均小于18的元素,且原子序数依次增大,其中B与C的电子层数相同,D与E的电子层数相同,A与D的最外层电子数相同,C与E的最外层电子数相同,E元素的原子最外层电子数是电子层数的2倍,D与其他具有相同电子层数的原子相比半径最大。又知由B元素组成的单质是空气中的主要成分。
(1)B的元素名称是_______ ,该元素的原子结构示意图为_______ ,核外有___ 个未成对电子,用电子式表示B的简单氢化物的形成过程_________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是________ (用离子符号表示)。
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)_____ 。
(4)以下说法正确的是________ 。
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
(1)B的元素名称是
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)
(4)以下说法正确的是
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
您最近一年使用:0次
2024-01-21更新
|
131次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期期末考试化学试题
解题方法
3 . 下表为部分短周期元素的性质或原子结构
下列说法正确的是
| 元素编号 | 元素性质或原子结构 |
X | 原子核外p电子数比s电子数多1 |
Y | 最高价氧化物对应水化物为一元强酸 |
Z | 所形成的的离子与氖原子核外电子排布相同且带2个单位电荷 |
| A.若原子半径X<Y,则相应气态氢化物的热稳定性一定有X>Y |
| B.若原子序数X>Z,则相应简单离子半径一定有X<Z |
| C.若Y与Z位于同一周期,则原子半径一定有Y<Z |
| D.若X与Z位于同一周期,则原子核外未成对电子数一定有X<Z |
您最近一年使用:0次
14-15高三上·上海宝山·阶段练习
名校
解题方法
4 . 有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子。下列说法中不正确的是


| A.X元素位于ⅥA | B.A能溶解于B中 |
| C.B的沸点大于C的沸点 | D.A和C不可能发生氧化还原反应 |
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z均为短周期元素,X、W可形成两种液态化合物甲和乙,其原子个数比分别为1∶1(甲)和2∶1(乙),且分子中电子总数分别为18(甲)和10(乙)。X与Z能形成一种极易溶于水的碱性气体丙X与Y能形成极易溶于水的酸性气体丁,丁分子中的电子数为18。X、Y、Z能形成一种离子化合物,其水溶液呈弱酸性。请写出:
(1)W的元素符号___ ,其核外共有___ 种运动状态不同的电子。
(2)甲物质的结构式为___ ;乙物质的空间构型为___ 。
(3)Z元素核外共有___ 种能量不同的电子,碱性气体甲的电子式为___ 。
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是___ 。
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为___ 。
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因___ 。
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。___ 。
(1)W的元素符号
(2)甲物质的结构式为
(3)Z元素核外共有
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。
您最近一年使用:0次
解题方法
6 . 部分中学化学常见元素原子结构及性质如表所示:
(1)A元素在周期表中的位置为____________________________________________ 。
(2)B与C形成的化合物的化学式为________ ,它属于________ (填“离子”或“共价”)化合物。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是____________________
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显________ 性,N的结构式为________ 。
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱____ 。
(5)有人认为B、D的单质用导线连接后插入氯化钠溶液中可以形成原电池,你认为是否可以,若可以,试写出正极的电极方程式(若认为不行可不写)___________________
| 序号 | 元素 | 结构及性质 |
| A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 | |
| B | B原子最外层电子数是内层电子总数的1/5 | |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ① | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ② | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A元素在周期表中的位置为
(2)B与C形成的化合物的化学式为
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱
(5)有人认为B、D的单质用导线连接后插入氯化钠溶液中可以形成原电池,你认为是否可以,若可以,试写出正极的电极方程式(若认为不行可不写)
您最近一年使用:0次
名校
7 . 如图是常温下部分短周期元素,最高价氧化物对应水化物的等物质的量浓度稀溶液的pH(pH=-lgc(H+) )与原子序数的关系图,其中H的氧化物是两性氧化物。下列说法正确的是
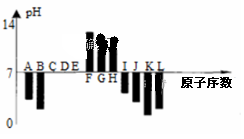

| A.元素B对应的氢化物比J对应的氢化物熔沸点更高,原因是B的氢化物中的键能比J中的大 |
| B.根据图形分析可知,K、L两种元素最高价氧化物对应的水化物的酸性,前者较强 |
| C.IC2熔化时克服的化学键和KL2与水反应时克服的化学键类型相同 |
| D.元素K、H、G分别形成的简单离子的半径逐渐减少 |
您最近一年使用:0次
2017-12-13更新
|
497次组卷
|
4卷引用:上海市上海交通大学附属中学2018届高三10月月考化学试题
2011·上海长宁·二模
8 . 下表为周期表前20号元素中某些元素的有关数据:
试回答下列问题:(以下各题回答,可能的话,均用对应的元素符号或物质的化学式表示)
(1)写出⑦⑨与氢元素形成的常见离子化合物的电子式_____________________
(2)上述⑤、⑥、⑦号元素中某2种元素形成的化合物中,每一个原子都满足最
外层为8电子稳定结构的物质可能是_________ 、__________ ;
(3)某元素R的原子半径为1.04× m,该元素在周期表中的位置是
m,该元素在周期表中的位置是______________
(4)以上10种元素的原子中,失去核外第一个电子所需能量最少的是_______
(5)④、⑦、⑧、⑩四种元素形成的离子,其半径由小到大的顺序为_________________
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
原子半径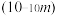 | 1.86 | 1.52 | 0.66 | 1.43 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| 最高价态 | +1 | +1 | —— | +3 | +4 | +5 | +7 | +1 | +5 | —— |
| 最低价态 | —— | —— | -2 | —— | -4 | -3 | -1 | —— | -3 | -1 |
试回答下列问题:(以下各题回答,可能的话,均用对应的元素符号或物质的化学式表示)
(1)写出⑦⑨与氢元素形成的常见离子化合物的电子式
(2)上述⑤、⑥、⑦号元素中某2种元素形成的化合物中,每一个原子都满足最
外层为8电子稳定结构的物质可能是
(3)某元素R的原子半径为1.04×
 m,该元素在周期表中的位置是
m,该元素在周期表中的位置是(4)以上10种元素的原子中,失去核外第一个电子所需能量最少的是
(5)④、⑦、⑧、⑩四种元素形成的离子,其半径由小到大的顺序为
您最近一年使用:0次



