上海市嘉定区第一中学2022-2023学年高二下学期期中考试化学(等级考)试题
上海
高二
期中
2023-04-17
213次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学反应原理、有机化学基础
上海市嘉定区第一中学2022-2023学年高二下学期期中考试化学(等级考)试题
上海
高二
期中
2023-04-17
213次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学反应原理、有机化学基础
一、填空题 添加题型下试题
1. 18世纪末,化学家在总结许多物质与氧的反应后,发现这类反应具有一些相似特征,提出了氧化还原反应的概念。19世纪发现化合价的概念后,完善了氧化还原反应的概念;20世纪初,成键的电子理论被建立,进一步完善了相关氧化还原的理论。请用学到的知识,回答下列问题。
(1)某反应中反应物与生成物有: 、
、 、
、 、
、 、
、 、
、 和一种未知物质X。
和一种未知物质X。
①已知 在反应中得到电子,则该反应的还原剂是
在反应中得到电子,则该反应的还原剂是___________ 。
②已知2个 在反应中得到10个电子生成一个X,则X的化学式为
在反应中得到10个电子生成一个X,则X的化学式为___________ 。
③根据上述反应可推知___________ 。
A.氧化性: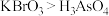 B.氧化性:
B.氧化性: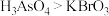
C.还原性: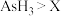 D.还原性:
D.还原性: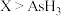
④将氧化剂和还原剂的化学式及其配平后的系数填入下列横线中,并用单线桥法标出电子转移的方向和数目:__________
___________+___________
(2)已知下列3个变化: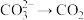 、
、 、
、 ,找出其中一个变化与“
,找出其中一个变化与“ ”组成一个反应。
”组成一个反应。
①写出该反应的离子方程式并配平___________ 。
②上述反应中的高锰酸钾在不同条件下可发生如下反应: ;
; ;
; ,由此可知,
,由此可知, 反应后的产物与
反应后的产物与___________ 有关。
(3)高锰酸钾溶液与亚硝酸钠发生如下反应: (未配平)
(未配平)
①写出上述反应中的半反应:氧化反应:___________ 。
②该反应当消耗 亚硝酸钠时,需消耗
亚硝酸钠时,需消耗
___________  。
。
(1)某反应中反应物与生成物有:
 、
、 、
、 、
、 、
、 、
、 和一种未知物质X。
和一种未知物质X。①已知
 在反应中得到电子,则该反应的还原剂是
在反应中得到电子,则该反应的还原剂是②已知2个
 在反应中得到10个电子生成一个X,则X的化学式为
在反应中得到10个电子生成一个X,则X的化学式为③根据上述反应可推知
A.氧化性:
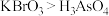 B.氧化性:
B.氧化性: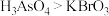
C.还原性:
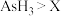 D.还原性:
D.还原性: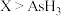
④将氧化剂和还原剂的化学式及其配平后的系数填入下列横线中,并用单线桥法标出电子转移的方向和数目:
___________+___________
(2)已知下列3个变化:
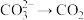 、
、 、
、 ,找出其中一个变化与“
,找出其中一个变化与“ ”组成一个反应。
”组成一个反应。①写出该反应的离子方程式并配平
②上述反应中的高锰酸钾在不同条件下可发生如下反应:
 ;
; ;
; ,由此可知,
,由此可知, 反应后的产物与
反应后的产物与(3)高锰酸钾溶液与亚硝酸钠发生如下反应:
 (未配平)
(未配平)①写出上述反应中的半反应:氧化反应:
②该反应当消耗
 亚硝酸钠时,需消耗
亚硝酸钠时,需消耗
 。
。
您最近一年使用:0次
填空题
|
适中(0.65)
名校
解题方法
2. 百余种不同的元素,是构成大千世界中所有物质的“基石”。科学家们根据元素的性质递变规律、电子排布规律等对元素进行编排设计元素周期表。请根据所学内容回答下列问题:
(1)地壳中含量最多的元素的基态原子的轨道表示式是___________ ,能量最高的电子所在的轨道呈___________ 形。
(2) 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是___________ 。
(3)研究发现,正离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是___________ 。
(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填___________ (填“有”或“无”)该元素在元素周期表中的位置:第___________ 周期,第___________ 族,该周期共有___________ 种元素。
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
预测X值的区间:___________ ;上表中五种元素的第一电离能由大到小的顺序是___________ 。(写元素符号)
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态 原子的外围电子排布式为
原子的外围电子排布式为___________ ; 位于周期表中
位于周期表中___________ 区,基态 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(7) 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是___________ 。
(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
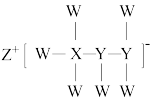
(1)地壳中含量最多的元素的基态原子的轨道表示式是
(2)
 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是(3)研究发现,正离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 |  , , |  , , |  , , |  |  |
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态
 原子的外围电子排布式为
原子的外围电子排布式为 位于周期表中
位于周期表中 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
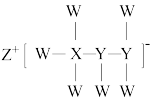
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.Y的最高化合价氧化物的水化物为强酸 |
D.X的氟化物 中原子均为8电子稳定结构 中原子均为8电子稳定结构 |
您最近一年使用:0次



