解题方法
1 . X、Y、Z、M、W为五种原子序数递增的前20号元素。X、Y是同周期元素,原子序数相差2,族序数之和为10;Z原子最外层电子数等于其最内层电子数,M在地壳中含量居第二位;W的某种盐常用作加碘盐的碘制剂。下列说法错误的是
| A.原子半径:W>Z>M>X>Y |
| B.最高价氧化物对应的水化物的酸性:X>M |
| C.ZXY3含离子键和共价键,0.1molW2Y2含有0.4mol离子 |
| D.Z与XY2反应可置换出X单质,X与MY2反应可置换出M单质 |
您最近一年使用:0次
2 . 短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是

| A.氢化物沸点:X<Z |
| B.最高价氧化物对应水化物的酸性:Y>W |
C.化合物熔点: |
| D.简单离子的半径:Y<X |
您最近一年使用:0次
2020-10-12更新
|
170次组卷
|
2卷引用:广东省肇庆市广宁第一中学2021届高三上学期9月月考化学试题
解题方法
3 . 短周期主族元素A、B、C、D、E的原子序数依次增大。常温下,A、B组成的化合物是常见液体,C的原子半径是短周期主族元素中最大的,D最外层电子数等于电子层数的2倍。回答下列问题:
(1)B在元素周期表中的位置为________ ;A、B组成的原子个数比为1:1的化合物的电子式为________ 。
(2)B、C的简单离子中,半径较大的是________ (填离子符号);A、B、C三种元素组成的化合物中含有的化学键类型是________ 。
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为________ 。
(4)下列叙述能说明E的非金属性强于D的是________ (填序号)。
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
(1)B在元素周期表中的位置为
(2)B、C的简单离子中,半径较大的是
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为
(4)下列叙述能说明E的非金属性强于D的是
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
您最近一年使用:0次
名校
4 . 短周期元素a、b、c、d、e的原子序数依次增大,由它们中的部分元素形成的化合物X、Y、Z、W在一定条件下的相互转化关系如图所示。已知X、Y、Z均含有d元素;Y是两性氢氧化物;W是一种焰色反应呈黄色的强碱;e原子的得电子能力在同周期中最强。下列说法正确的是


| A.a、c分别与e形成的化合物的化学键类型相同 |
| B.b元素的单质和氢化物可能具有强氧化性和漂白性 |
| C.c的简单离子的氧化性强于d的 |
| D.d元素的单质不能与W溶液反应 |
您最近一年使用:0次
2020-08-06更新
|
85次组卷
|
2卷引用:山东省日照市莒县2018-2019学年高一下学期期中考试化学试题
解题方法
5 . 短周期元素X、Y、Z、W在周期表中的位置如图所示,X通过共用3对电子形成X2分子,下列说法不正确的是


| A.4种元素的简单氢化物中,Y的沸点最高 |
| B.X、Z、W均为活泼非金属元素,其含氧酸都是强酸 |
| C.W的单质能与水反应,生成一种具有漂白性的物质 |
| D.化合物XW3中各原子均满足最外层8电子的稳定结构 |
您最近一年使用:0次
名校
解题方法
6 . 短周期元素A、B、C在周期表中所处的位置如图所示。A、B、C三种元素原子的质子数和为32。D元素原子的最外层电子数是其次外层电子数的2倍。则下列说法正确的是( )


| A.四种元素形成的气态氢化物中,C元素的氢化物的稳定性最强 |
| B.元素D的某种同位素质量数为14,则其中子数为6 |
| C.B、C两种元素可形成BC6型化合物,该化合物属于离子化合物 |
| D.A、B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且都属于氧化还原反应 |
您最近一年使用:0次
2020-05-18更新
|
159次组卷
|
13卷引用:山东省日照市2018届高三11月校际联合期中考试化学试题
山东省日照市2018届高三11月校际联合期中考试化学试题【全国百强校】山东省济南市第一中学2019届高三上学期期中考试化学试题山东省德州市夏津县第一中学2019届高三上学期12月月考化学试题(已下线)2019年9月5日《每日一题》2020一轮复习—元素“位?构?性”的综合推断福建省莆田市莆田第二十五中学2020届高三上学期期中考试化学试题山东省泰安第一中学2019-2020学年高一下学期期中考试化学试题黑龙江省鸡西市第一中学2019-2020学年高一下学期期中考试化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)山东省泰安市宁阳一中2020-2021学年高一下学期第一次考试化学试题四川省资阳市雁江区中和中学2020-2021学年高一下学期期中考试化学试题(已下线)考向16 元素周期表 元素周期律-备战2022年高考化学一轮复习考点微专题江西省赣州市第四中学2023-2024学年高三上学期开学考试化学试题(已下线)BBWYhjhx1009.pdf
名校
解题方法
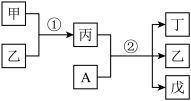
7 . 短周期元素a、b、c、d的原子序数依次增大。其中A为d元素组成的单质;甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物,常温下乙为液体。下列说法正确的是
| A.简单离子半径:c >b |
| B.反应①为吸热反应 |
| C.②在常温下反应时,氧化剂与还原剂物质的量之比为1:1 |
| D.b、d分别与a形成的化合物中,化学键类型一定完全相同 |
您最近一年使用:0次
2020-01-27更新
|
278次组卷
|
4卷引用:山东省日照一中2021届高三11月份第二次调研考试化学试题
名校
8 . X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y 原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是
| A.X、Z、W三元素所形成的化合物一定为共价化合 物 |
| B.原子半径:r(M)>r(Y) >r(Z) >r(W) >r(X) |
| C.W和M形成的化合物不能与强碱反应 |
| D.Y、Z的最高价含氧酸的酸性:Y>Z |
您最近一年使用:0次
2019-05-28更新
|
236次组卷
|
6卷引用:山东省日照第一中学2021届高三上学期10月份第一次调研考试化学试题
名校
9 . 已知短周期元素的四种离子aA2+、bB+、cC3-、dD-具有相同的电子层结构,则下列叙述中正确的是
| A.原子半径:B>A>C>D | B.原子序数:D>C>B>A |
| C.离子半径:C3->D->A2+>B+ | D.氧化性:A2+>B+,还原性:C3-<D- |
您最近一年使用:0次
2019-03-22更新
|
894次组卷
|
27卷引用:2016-2017学年江西省南昌市第二中学高一下学期第一次月考化学试卷
2016-2017学年江西省南昌市第二中学高一下学期第一次月考化学试卷北京四中2017-2018学年高一下学期第一次月考化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一4月月考化学试题山东省菏泽市第一中学2017-2018学年高一自主检测化学试题【全国校级联考】湖北省襄阳市四校(襄州一中、枣阳一中、宜城一中、曾都一中)2017-2018学年高一下学期期中联考化学试题【全国校级联考】湖北省宜昌市县域优质高中协同发展共合体2017-2018学年高一下学期期末考试化学试题(已下线)2018年9月5日《每日一题》一轮复习-微粒半径大小的比较【校级联考】湖北省孝感市六校2018-2019学年高二上学期12月月考化学试题(已下线)考点07 元素周期律和元素周期表——备战2019年浙江新高考化学考点山西省晋中市和诚高中有限公司2018-2019学年高一下学期3月月考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一下学期4月月考化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题安徽省滁州市明光中学2018-2019学年高一下学期第一次月考化学试题四川省威远中学2018-2019学年高一下学期第二次月考化学试题(已下线)2019年9月4日《每日一题》2020一轮复习—微粒半径大小的比较湖北省宜昌市葛洲坝中学2019-2020学年高二8月月考化学试题(已下线)【南昌新东方】2019 南昌二中 高一下 第一次月考(已下线)专题5.2 元素周期律和元素周期表(讲)——2020年高考化学一轮复习讲练测(已下线)第18讲 元素周期律和元素周期表(精讲)——2021年高考化学一轮复习讲练测山东省日照市国开中学2021-2022学年高一下学期第一次月考化学试题江西省赣州市潭口中学2020-2021学年高一下学期第一次月考化学试题(已下线)第14讲 元素周期律和元素周期表(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)四川省峨眉第二中学校2021-2022学年高一下学期3月月考化学试题(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)四川省内江市2022-2023学年高一上学期期末考试化学试题云南迪庆藏族自治州民族中学2022-2023学年高一下学期期末考试化学试题
10 . X、Y、Z、M、W、Q是6种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是_____ 。
(2)X2Q2为______ 化合物(填“离子”或“共价”)。
(3)Z元素的单质是黑火药的主要成分之一,在反应中Z元素的单质表现了_____ 性。
(4)下列能说明M元素比z元素非金属性强的是_____ (填字母标号)。
a.M的气态氢化物的沸点强于Z的
b.M的氧化物对应水化物的酸性强于Z的
c.M的单质与Z的气态氢化物的水溶液反应,使其变浑浊
d.一 定条件下Z、M的单质与Fe反应,产物中铁的价态前者比后者低
(5)科学家们认为存在含氢量最高的化合物WH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式__________ 。
| 元素代号 | X | Y | Z | M | W | Q |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,- 1 | +5,- 3 | -2 |
(1)上述元素中,金属性最强的在周期表中的位置是
(2)X2Q2为
(3)Z元素的单质是黑火药的主要成分之一,在反应中Z元素的单质表现了
(4)下列能说明M元素比z元素非金属性强的是
a.M的气态氢化物的沸点强于Z的
b.M的氧化物对应水化物的酸性强于Z的
c.M的单质与Z的气态氢化物的水溶液反应,使其变浑浊
d.一 定条件下Z、M的单质与Fe反应,产物中铁的价态前者比后者低
(5)科学家们认为存在含氢量最高的化合物WH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式
您最近一年使用:0次



