名校
解题方法
1 . 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为___________________ 。
(2)关于B2A2的下列说法中正确的是________________ 。
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是________________ 。
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因__________ 。
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有____________ 键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,N的 结构式为________ 。
(6) E的氢化物的价层电子对互斥理论模型为________ ,E 原子的杂化方式为________ 杂化。
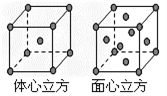
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为_________ ,F原子配位数之比为__________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有
(6) E的氢化物的价层电子对互斥理论模型为
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为

您最近一年使用:0次
2017-05-18更新
|
512次组卷
|
2卷引用:黑龙江省大庆实验中学2017届高三考前得分训练(一)理科综合化学试题2
名校
2 . X、Y、Z、W是四种原子序数依次增大的主族元素。已知X、Y、Z是短周期中的三种非金属元素,X元素原子的核外电子数等于所在周期数;Y单质为无色气体,性质稳定,常用作保护气;Z元素原子的最外层电子数是内层电子数的3倍;W是地壳中含量最高的金属元素。下列说法中正确的是
| A.四种元素的原子半径从大到小的顺序是W>Z>Y>X |
| B.元素X、Y和Z可以组成共价化合物,也可以组成离子化合物 |
| C.化合物YX3水溶液能导电,所以YX3属于电解质 |
| D.工业上采用电解WCl3溶液的方法制取W单质 |
您最近一年使用:0次
2017-12-13更新
|
174次组卷
|
2卷引用:安徽省蒙城县第一中学、淮南第一中学等2018届高三上学期“五校”联考化学试题
名校
3 . 短周期元素W、X、Y和Z的原子序数依次增大。元素W是形成化合物数量众多,且分布极广的元素,X原子的最外层电子数是其电子层数的3倍,元素Y是地壳中含量最丰富的金属元素,Z元素的单质易溶于WZ2中。下列说法错误的是( )
| A.元素X、Y与Z的原子半径大小:Y>Z>X |
| B.元素W、Z的氯化物中,化学键类型相同,且各原子均满足8电子 |
| C.元素X与元素Y形成的化合物是一种较好的耐火材料 |
| D.元素X可与元素Z可组成3种二价阴离子 |
您最近一年使用:0次
2017-03-17更新
|
490次组卷
|
3卷引用:2017届辽宁省沈阳市东北育才学校高三第五次模拟考试理综化学试卷
名校
解题方法
4 . M、N、Q、R为原子序数依次增大的短周期主族元素,N是形成有机物基本骨架的元素,M与N、Q可分别形成共价化合物S、T,且S、T分子中含相同的电子数。金属单质R在Q的单质中燃烧生成的化合物W可与T发生氧化还原反应。下列说法正确的是
| A.原子半径大小:M<N<Q<R |
| B.W中的阴阳离子个数比为1:1,属于离子化合物 |
| C.Q的某单质可作水的消毒剂,该单质在大气中含量越多,对人体越有益 |
| D.M和N、Q均能形成既含极性键又含非极性键的分子 |
您最近一年使用:0次
2017-03-11更新
|
354次组卷
|
2卷引用:2017届山西省名校高三下学期联考理综化学试卷
名校
5 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素; Z原子的最外层电子数是其最内层电子数的 ;W的最高正价和最低负价的代数和为0。下列说法正确的是
;W的最高正价和最低负价的代数和为0。下列说法正确的是
 ;W的最高正价和最低负价的代数和为0。下列说法正确的是
;W的最高正价和最低负价的代数和为0。下列说法正确的是| A.原子半径:X<Y<Z<W |
| B.Z的氢化物中只含离子键 |
| C.最高价氯化物对应水化物的酸性:Y>W |
| D.X和W两种元素形成的化合物,既能与强酸反应又能与强碱反应 |
您最近一年使用:0次
2014·广东深圳·一模
名校
6 . W、X、Y、Z是短周期元素,其部分性质如下表:
下列说法正确的是
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的 错误!未找到引用源。 错误!未找到引用源。 |
| Z | 第三周期原子半径最小的金属元素 |
| A.气态氢化物的热稳定性:X>W | B.Z的氧化物中含有非极性共价键 |
| C.离子半径:Z>W | D.最高价氧化物对应水化物的酸性:Y>X |
您最近一年使用:0次
2017-04-21更新
|
309次组卷
|
3卷引用:2014届广东省深圳市高三一模考试理综化学试卷
7 . a、b、c、d为四种短周期元素,a的原子M电子层有l个电子,b是地壳中含量最多的金属元素,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。关于这四种元素下列叙述错误的是
| A.a、c、d均存在两种以上的氧化物 |
| B.b的氧化物与d的最高价氧化物对应水化物反应后的溶液呈酸性 |
| C.a是短周期中金属性最强的元素 |
| D.工业上是通过电解b、d形成的化合物制取b单质 |
您最近一年使用:0次
名校
8 . 短周期主族元素W、R、X、Y、Z的原子序数依次增大,W的原子半径是周期表中所有元素中最小的,R是地壳中含量最多的元素,X与W同主族,Y的最外层电子数是最内层电子数的3倍。下列说法正确的是( )
| A.原子半径:R<Y<Z |
| B.简单气态氢化物的热稳定性:R>Y |
| C.R与Y只能形成一种化合物 |
| D.最高价氧化物对应水化物的酸性:Y>Z |
您最近一年使用:0次
2016-12-09更新
|
574次组卷
|
7卷引用:【全国百强校】江苏省扬州中学2018-2019学年高二第二学期开学测试化学试题
9 . X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是
| A.原子半径的大小顺序: r(X)>r(Y)>r(Z)>r(R) |
| B.含有Y、Z、R三种元素的化合物最多只有2种 |
| C.元素R和Y形成的化合物RY2是一种高效安全灭菌消毒剂 |
| D.Y与Z形成的两种化合物中的化学键和晶体类型均相同 |
您最近一年使用:0次
2016-12-09更新
|
167次组卷
|
3卷引用:2015届江苏省淮安市高三第五次模拟考试化学试卷
10 . 短周期元素A、B、C、D的原子序数依次增大.它们的原子序数之和为36,且原子的最外层电子数之和为14; A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D分别为同主族元素。下列叙述正确的是
| A.在地壳中,B元素的含量位于第二位 |
| B.C元素的单质熔点低,在空气中加热时先熔化后燃烧 |
| C.A、B、D三种元素形成的化合物一定是强酸 |
| D.B元素与A元素形成的物质一定是纯净物 |
您最近一年使用:0次



