1 . 下列8种化学符号: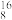 O2、
O2、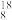 O2、
O2、 H、
H、 C、
C、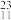 Na、
Na、 N、
N、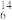 C、
C、 Mg。
Mg。
(1)表示核素的符号共_______ 种。
(2)互为同位素的是_______ 。
(3)质量相同的H216O和D216O所含中子数之比为_______ 。
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:Be(OH)2与Mg(OH)2可用_______ 试剂鉴别。
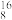 O2、
O2、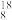 O2、
O2、 H、
H、 C、
C、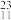 Na、
Na、 N、
N、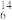 C、
C、 Mg。
Mg。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:Be(OH)2与Mg(OH)2可用
您最近一年使用:0次
名校
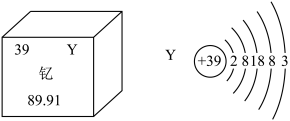
2 . 新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:_______ 个质子,左图中89.91表示的是_______ ;
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据_______ 个电子层;
(3)钇元素形成氧化物的化学式是_______ 。
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据
(3)钇元素形成氧化物的化学式是
您最近一年使用:0次
2022-10-08更新
|
327次组卷
|
3卷引用:新疆和田地区第一中学2022-2023学年高一上学期开学考试化学试题
解题方法
3 . 在 ,
, ,
, ,
,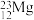 ,
, ,
, ,
, ,
, 中共有
中共有___________ 种元素,___________ 种原子,中子数最多的是___________ ,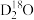 的相对分子质量是
的相对分子质量是___________ 。
 ,
, ,
, ,
,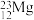 ,
, ,
, ,
, ,
, 中共有
中共有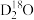 的相对分子质量是
的相对分子质量是
您最近一年使用:0次
名校
4 . 完成表格
(1)①_______ ②_______ ③_______ ④_______
(2)①_______ ②_______
(3)①_______ ②_______
(4)①_______ ② _______
(5)①_______ ②_______ ③_______
| 小题序号 | 化学符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1) |  C C | ①_______ | ②_______ | ③_______ | ④_______ |
| (2) | ①_______ | 8 | 10 | 10 | ②_______ |
| (3) | ①_______ | 12 | 12 | 10 | ②_______ |
| (4) | H3O+ | ①_______ | / | ②_______ | / |
| (5) | TD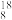 O O | ①_______ | ②_______ | ③_______ | / |
(1)①
(2)①
(3)①
(4)①
(5)①
您最近一年使用:0次
5 . 请根据题中提供的信息,填写空格。
(1) H、
H、 H、
H、 H互为
H互为___________ ;O2、O3互为___________ 。
(2)下列8种化学符号:① O2、②
O2、②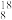 O2、③
O2、③ H、④
H、④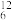 C、⑤
C、⑤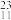 Na、⑥
Na、⑥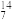 N、⑦
N、⑦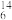 C、⑧
C、⑧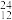 Mg.表示核素的符号共
Mg.表示核素的符号共___________ 种。
(3)⑥在元素周期表中的位置是___________ ;⑧的粒子结构示意图___________ 。
(4)写出单质⑤的最高价氧化物对应水化物与铝反应的离子方程式___________ 。
(5)质量相同的H216O和D216O所含中子数之比为___________ 。
(1)
 H、
H、 H、
H、 H互为
H互为(2)下列8种化学符号:①
 O2、②
O2、②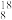 O2、③
O2、③ H、④
H、④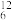 C、⑤
C、⑤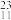 Na、⑥
Na、⑥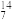 N、⑦
N、⑦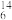 C、⑧
C、⑧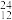 Mg.表示核素的符号共
Mg.表示核素的符号共(3)⑥在元素周期表中的位置是
(4)写出单质⑤的最高价氧化物对应水化物与铝反应的离子方程式
(5)质量相同的H216O和D216O所含中子数之比为
您最近一年使用:0次
2022-03-29更新
|
288次组卷
|
2卷引用:四川省内江市资中县球溪中学2021-2022学年高一下学期3月月考化学试题
名校
6 . 有下列四种微粒:① ②
② ③
③ ④
④ 。(只填序号,下同)。
。(只填序号,下同)。
(1)按原子半径由大到小的顺序排列为_______ ;微粒中质子数小于中子数的是_______ 。
(2)能形成 型化合物的是
型化合物的是_______ ;通常情况下,化合价有零价、正价和负价的是_______ 。
 ②
② ③
③ ④
④ 。(只填序号,下同)。
。(只填序号,下同)。(1)按原子半径由大到小的顺序排列为
(2)能形成
 型化合物的是
型化合物的是
您最近一年使用:0次
名校
解题方法
7 . 根据下表中的电子、质子和中子的基本数据,讨论回答问题:
(1)决定原子质量的主要微粒是___________ 。
(2)原子相对质量的计算方法是___________ 。
(3)如果1个质子和1个中子的相对质量都近似等于1,其原子的相对质量近似等于___________ 。
(4)原子中质子数、中子数、质量数之间的关系是___________ 。
(5)确定原子中质子数的方法是___________ 。
(6)原子显电中性的原因是___________ 。
| 微粒 | 电子 | 质子 | 中子 |
| 质量/kg | 9.109×10-31 | 1.637×10-27 | 1.675×10-27 |
| 相对质量 | 0.548×10-3 | 1.007 | 1.008 |
| 电量(C) | 1.602×10-19 | 1.602×10-19 | 0 |
| 电荷 | -1 | +1 | 0 |
| 氧原子序数为8 | 8 | 8 |
(2)原子相对质量的计算方法是
(3)如果1个质子和1个中子的相对质量都近似等于1,其原子的相对质量近似等于
(4)原子中质子数、中子数、质量数之间的关系是
(5)确定原子中质子数的方法是
(6)原子显电中性的原因是
您最近一年使用:0次
8 . 【情境问题思考】
道尔顿提出的原子学说曾引起很大的轰动,因而他被誉为“近代化学之父”。他的学说中有下述两个观点:原子是微小的实心球体;原子是不能再分的粒子。通过你初中对原子结构的学习,你认为上述两个观点正确吗?请大家结合课本“联想质疑”栏目—— 卢瑟福的 粒子散射实验,思考完成以下问题:
粒子散射实验,思考完成以下问题:
①绝大多数α粒子穿过金箔后仍沿原来的方向前进,原因是什么?
②为什么有少数α粒子却发生了较大的偏转?
③极少数的α粒子几乎象是被金箔弹了回来,原因是什么?
(1)卢瑟福α离子散射实验结论:
卢瑟福的原子核式模型:原子由_____________ 和_____________ 构成,_____________ 带正电荷,位于原子的中心;带负电荷的_____________ 在原子核周围的空间做高速运动。
【交流研讨】
1.在原子中,质子数、核电荷数和核外电子数之间存在着什么关系?为什么?
2.原子的质量主要由哪些微粒决定?
3.如果忽略电子的质量,质子、中子的相对质量分别取其近似整数值,那么,原子的相对质量在数值上与原子核内的质子数和中子数有什么关系?
【归纳小结】
(2)①数量关系:________ = _____________ = ____________ 。
②质量关系:_______ =____________ + _____________ 。
③质量数定义__________________ ,符号________ 。
④ X中A代表
X中A代表___________ ,Z代表______________ ,中子数=______________ 。
道尔顿提出的原子学说曾引起很大的轰动,因而他被誉为“近代化学之父”。他的学说中有下述两个观点:原子是微小的实心球体;原子是不能再分的粒子。通过你初中对原子结构的学习,你认为上述两个观点正确吗?请大家结合课本“联想质疑”栏目—— 卢瑟福的
 粒子散射实验,思考完成以下问题:
粒子散射实验,思考完成以下问题:①绝大多数α粒子穿过金箔后仍沿原来的方向前进,原因是什么?
②为什么有少数α粒子却发生了较大的偏转?
③极少数的α粒子几乎象是被金箔弹了回来,原因是什么?
(1)卢瑟福α离子散射实验结论:
卢瑟福的原子核式模型:原子由
【交流研讨】
1.在原子中,质子数、核电荷数和核外电子数之间存在着什么关系?为什么?
2.原子的质量主要由哪些微粒决定?
3.如果忽略电子的质量,质子、中子的相对质量分别取其近似整数值,那么,原子的相对质量在数值上与原子核内的质子数和中子数有什么关系?
【归纳小结】
(2)①数量关系:
②质量关系:
③质量数定义
④
 X中A代表
X中A代表
您最近一年使用:0次
9 . 观察课本附录元素周期表,思考完成以下问题。
(1)元素周期表共有多少个周期?每个周期各有多少种元素?_____
(2)以第2周期、第3周期元素为例分析:元素周期表中,位于同一周期的元素的原子结构有什么相同之处?它们又是怎样递变的?______
(3)以第1纵列、第17纵列为例分析:元素周期表中,位于同一纵列的元素的原子结构有什么相同之处?它们又是怎么递变的?_____
(4)总结周期表中周期和族划分的依据是什么?关于周期表,你还能提出哪些问题?_______
(1)元素周期表共有多少个周期?每个周期各有多少种元素?
(2)以第2周期、第3周期元素为例分析:元素周期表中,位于同一周期的元素的原子结构有什么相同之处?它们又是怎样递变的?
(3)以第1纵列、第17纵列为例分析:元素周期表中,位于同一纵列的元素的原子结构有什么相同之处?它们又是怎么递变的?
(4)总结周期表中周期和族划分的依据是什么?关于周期表,你还能提出哪些问题?
您最近一年使用:0次
解题方法
10 . 原子序数:_______ 。
您最近一年使用:0次



