1 . 在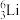 、
、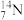 、
、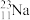 、
、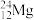 、
、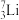 、
、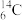 中:
中:
(1)________ 和________ 互为同位素。
(2)________ 和________ 质量数相等,但不能互称同位素。
(3)________ 和________ 的中子数相等,但质子数不相等,所以不是同一种元素。
(4)填写下列表格:
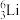 、
、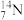 、
、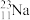 、
、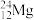 、
、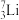 、
、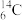 中:
中:(1)
(2)
(3)
(4)填写下列表格:
| 原子组成 | N中子数 | A质量数 |
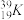 | ① | |
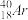 | ② |
您最近一年使用:0次
名校
2 . 联合国将2019年定为“国际化学元素周期表年”,2018年中国化学会制作了新版周期表,包含118种元素。回答下列问题:

(1)碳元素在周期表中的位置是______________ 。
(2)将硅的元素符号填写在上述周期表相应的空格中。________
(3)在上述周期表中,用实线画出周期表的上方边界。_______
(4)第118号元素为Og(中文名“ ”,ào),下列说法不正确的是
”,ào),下列说法不正确的是____ 。
a.Og是第七周期0族元素
b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强
d.中子数为179的Og核素符号是

(1)碳元素在周期表中的位置是
(2)将硅的元素符号填写在上述周期表相应的空格中。
(3)在上述周期表中,用实线画出周期表的上方边界。
(4)第118号元素为Og(中文名“
 ”,ào),下列说法不正确的是
”,ào),下列说法不正确的是a.Og是第七周期0族元素
b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强
d.中子数为179的Og核素符号是

您最近一年使用:0次
名校
3 . 按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是_____
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)极性共价键与非极性共价键的判断方法_____________________
(3)写出下列物质的电子式:CaF2:_______ CO2:_______ NH4Cl:__________
(4) 用电子式表示下列化合物的形成过程
H2S:__________________________________
MgF2:___________
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题_______________
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程
H2S:
MgF2:
请归纳物质电子式的书写及用电子式表示化合物的形成过程应注意哪些问题
您最近一年使用:0次
名校
4 . (1)微粒AXn-核外有18个电子,则它的核电荷数为________ ,核内中子数为_______ 。
(2)由1H216O与2H217O所代表的物质中,共有__________ 种元素,_________ 种原子,16O、17O的关系为________ 。
(3)已知:碳元素有12C、13C、14C;氧元素有16O、18O,则它们能够形成______ 种CO2分子。
(2)由1H216O与2H217O所代表的物质中,共有
(3)已知:碳元素有12C、13C、14C;氧元素有16O、18O,则它们能够形成
您最近一年使用:0次
名校
5 . 元素的同位素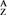 X,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应。若这种同位素中有20个中子,求:
X,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应。若这种同位素中有20个中子,求:
(1)Z和A的值:Z:________ 、A:________ 。
(2)X元素在周期表中的位置:________ 。
(3)写出XCl2与AgNO3反应的化学方程式____________________ 。
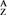 X,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应。若这种同位素中有20个中子,求:
X,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应。若这种同位素中有20个中子,求:(1)Z和A的值:Z:
(2)X元素在周期表中的位置:
(3)写出XCl2与AgNO3反应的化学方程式
您最近一年使用:0次
名校
6 . 有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A_______ ,B_______ ,C_______ ,D______ ,E_______ 。
(2)B微粒的结构示意图________ ,D微粒的结构示意图_________ 。
(3)A的单质与EB溶液反应的离子方程式:_______________ 。
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A
(2)B微粒的结构示意图
(3)A的单质与EB溶液反应的离子方程式:
您最近一年使用:0次
2018-03-14更新
|
439次组卷
|
5卷引用:山东省寿光现代中学2017-2018学年高一下学期开学考试化学试题
名校
7 . 有①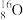 、
、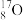 、
、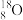 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
(1)分别写出氢元素三种同位素的名称:______ 、_______ 、______ 。写出用做制造氢弹原料的同位素原子:______ (填原子符号)。
(2)互为同位素的是________ (填编号,下同)。
(3)互为同素异形体的是_______ 。
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是_____________ 。
(5)质量相同的H216O 和D216O 所含质子数之比为_______ ,中子数之比为_______ 。
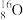 、
、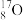 、
、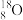 ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:(1)分别写出氢元素三种同位素的名称:
(2)互为同位素的是
(3)互为同素异形体的是
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是
(5)质量相同的H216O 和D216O 所含质子数之比为
您最近一年使用:0次
8 . I.  U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:
(1) U表示的含义是
U表示的含义是________________ 。
(2)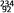 U、
U、 U、
U、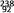 互为同位素,下列对同位素的理解不正确的是
互为同位素,下列对同位素的理解不正确的是________ (填序号,下同)。
A.元素符号相同 B.物理性质相同
C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关 U说法不正确的是
U说法不正确的是________ 。
A. U原子核的中子数与质子数之差为51
U原子核的中子数与质子数之差为51
B. U与
U与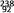 U的质子数、电子数都相等
U的质子数、电子数都相等
C. U与
U与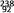 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子
D. U与
U与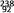 U是同种原子
U是同种原子
Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)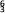 Li和
Li和 Li作核反应堆最佳载热体,
Li作核反应堆最佳载热体, LiH和
LiH和 LiD作高温堆减速剂。下列说法中 正确的是
LiD作高温堆减速剂。下列说法中 正确的是________ (填序号,下同)。
A.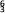 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.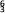 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质
(2)下列说法不正确的是________ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
(3)锂是碱金属族首元素,其性质明显不同于其他碱金属性质,下列能支持这一观点的性质是________ 。
A.碱金属与水反应 B.碱金属在氧气中燃烧
C.碱金属与氢气反应 D.碱金属与氯气反应
 U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:(1)
 U表示的含义是
U表示的含义是(2)
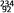 U、
U、 U、
U、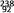 互为同位素,下列对同位素的理解不正确的是
互为同位素,下列对同位素的理解不正确的是A.元素符号相同 B.物理性质相同
C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关
 U说法不正确的是
U说法不正确的是A.
 U原子核的中子数与质子数之差为51
U原子核的中子数与质子数之差为51 B.
 U与
U与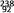 U的质子数、电子数都相等
U的质子数、电子数都相等C.
 U与
U与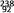 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子 D.
 U与
U与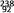 U是同种原子
U是同种原子Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)
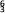 Li和
Li和 Li作核反应堆最佳载热体,
Li作核反应堆最佳载热体, LiH和
LiH和 LiD作高温堆减速剂。下列说法中 正确的是
LiD作高温堆减速剂。下列说法中 正确的是A.
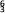 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.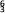 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质(2)下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
(3)锂是碱金属族首元素,其性质明显不同于其他碱金属性质,下列能支持这一观点的性质是
A.碱金属与水反应 B.碱金属在氧气中燃烧
C.碱金属与氢气反应 D.碱金属与氯气反应
您最近一年使用:0次
9 . 科学家发现:具有2、8、20、28、50、82、114、126、184等数目的质子或中子的原子核具有特别的稳定性,并将这些数称为“幻数”,而具有双幻数的 He、
He、 Ni、
Ni、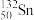 、
、 等尤为稳定。根据此信息回答下列问题:
等尤为稳定。根据此信息回答下列问题:
(1)写出元素周期表中前三种质子数为“幻数”的元素原子的结构示意图,并标明元素符号:_____________ 、______________ 、___________ 。
(2)已知氧有三种同位素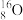 、
、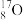 、
、 ,根据上述“幻数”规律,氧的同位素中原子核最稳定的是
,根据上述“幻数”规律,氧的同位素中原子核最稳定的是__________ 。
(3)根据现有元素周期律推算, R位于元素周期表的第
R位于元素周期表的第________ 周期第________ 族,核稳定性 R
R________  R(填“>”、“<”或“=”)。
R(填“>”、“<”或“=”)。
 He、
He、 Ni、
Ni、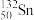 、
、 等尤为稳定。根据此信息回答下列问题:
等尤为稳定。根据此信息回答下列问题:(1)写出元素周期表中前三种质子数为“幻数”的元素原子的结构示意图,并标明元素符号:
(2)已知氧有三种同位素
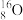 、
、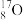 、
、 ,根据上述“幻数”规律,氧的同位素中原子核最稳定的是
,根据上述“幻数”规律,氧的同位素中原子核最稳定的是(3)根据现有元素周期律推算,
 R位于元素周期表的第
R位于元素周期表的第 R
R R(填“>”、“<”或“=”)。
R(填“>”、“<”或“=”)。
您最近一年使用:0次
解题方法
10 . 4g D2和20g18O2化合时最多能生成__________ g D218O,1mol D218O中含____ mol质子,含_____ mol中子。
您最近一年使用:0次



