名校
1 .  粒子是带有2个单位正电荷、质量数为4的
粒子是带有2个单位正电荷、质量数为4的 离子,由此推断
离子,由此推断 粒子含有
粒子含有___________ 个质子和___________ 中子。  粒子是
粒子是___________ (填正或负)离子。
 粒子是带有2个单位正电荷、质量数为4的
粒子是带有2个单位正电荷、质量数为4的 离子,由此推断
离子,由此推断 粒子含有
粒子含有 粒子是
粒子是
您最近一年使用:0次
2 . 下列8种化学符号: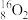 、
、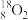 、
、 、
、 、
、 、
、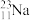 、
、 、
、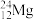 。
。
(1)表示核素的符号共___________ 种。
(2)互为同位素的是___________ 。
(3)质量相同的H216O和D216O所含中子数之比为___________ 。
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:___________ 。
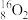 、
、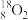 、
、 、
、 、
、 、
、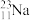 、
、 、
、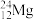 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:
您最近一年使用:0次
名校
3 . 元素周期表是学习化学的工具,也为化学的进一步探索与研究提供了理论指导,化学学习者和研究者一直关注周期表的运用与发展。试回答下列问题:
(1)“大爆炸理论”指出:200亿年以前,宇宙中所有物质都包含在一个密度无限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就产生了元素。你由此可知最先产生的元素是_____ (填写元素符号)。
(2)2006年11月16日美国和俄罗斯科学家联合宣布,他们合成出了118号元素,新原子的质量数为297,则该新原子中子数与质子数之差为_____ 。
(3)人们研究发现第一周期与第二周期一些元素的性质与同族元素性质共性很少,有人建议将氢放在VIIA,写出一种能支持该观点的化合物:______ 。
(4)研究周期表发现存在对角线规则,处于对角线上的元素性质相似,如硼与硅处于对角线,请写出硼和氢氧化钠溶液反应的离子方程式:______ 。
(1)“大爆炸理论”指出:200亿年以前,宇宙中所有物质都包含在一个密度无限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就产生了元素。你由此可知最先产生的元素是
(2)2006年11月16日美国和俄罗斯科学家联合宣布,他们合成出了118号元素,新原子的质量数为297,则该新原子中子数与质子数之差为
(3)人们研究发现第一周期与第二周期一些元素的性质与同族元素性质共性很少,有人建议将氢放在VIIA,写出一种能支持该观点的化合物:
(4)研究周期表发现存在对角线规则,处于对角线上的元素性质相似,如硼与硅处于对角线,请写出硼和氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)___________ ;
(2)由极性键构成的非极性分子有___________ ;
(3)与 可直接形成配位键的分子有
可直接形成配位键的分子有___________ ;
(4)分子中不含孤电子对的分子有___________ ,它的立体构型为___________ ;
(5)极易溶于水、且水溶液呈碱性的物质的分子是___________ ,它极易溶于水的原因是___________ 。
| 目前空气的成分 |  、 、 、 、 、水蒸气及稀有气体(如He、Ne等) 、水蒸气及稀有气体(如He、Ne等) |
| 原始大气的主要成分 |  、 、 、CO、 、CO、 等 等 |
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)
(2)由极性键构成的非极性分子有
(3)与
 可直接形成配位键的分子有
可直接形成配位键的分子有(4)分子中不含孤电子对的分子有
(5)极易溶于水、且水溶液呈碱性的物质的分子是
您最近一年使用:0次
2023-05-08更新
|
58次组卷
|
2卷引用:四川省巴中市恩阳区2022-2023学年高二下学期4月期中考试化学试题
名校
5 . 根据下列叙述,回答下列问题:
(1)A元素原子的最外层电子数为电子层数的3倍,写出A的原子结构示意图_____ 。
(2)与Ar原子电子层结构相同的-1价阴离子,则其离子符号为_________ 。
(3)质量数为23,中子数为12的原子,写出其在周期表中的位置_________ 。
(4)《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
①26Al和27Al______ (选填编号)。
A.是同一种元素 B.是同一种核素
C.具有相同的中子数 D.具有相同的化学性质
②碳元素的一种核素也可以考古断代,其原子符号为______ 。
③10g10Be所含的中子数与质子数之差为______ 个。
(1)A元素原子的最外层电子数为电子层数的3倍,写出A的原子结构示意图
(2)与Ar原子电子层结构相同的-1价阴离子,则其离子符号为
(3)质量数为23,中子数为12的原子,写出其在周期表中的位置
(4)《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
①26Al和27Al
A.是同一种元素 B.是同一种核素
C.具有相同的中子数 D.具有相同的化学性质
②碳元素的一种核素也可以考古断代,其原子符号为
③10g10Be所含的中子数与质子数之差为
您最近一年使用:0次
2023-01-06更新
|
166次组卷
|
3卷引用:黑龙江省富锦市第一中学2022-2023学年高一上学期期末考试化学试题
6 . 能量最低原理
(1)内容:在构建基态原子时,电子将尽可能地占据_______ 的原子轨道,使整个原子的能量最_______ 。
(2)因素:整个原子的能量由_______ 、_______ 和_______ 三个因素共同决定。
(1)内容:在构建基态原子时,电子将尽可能地占据
(2)因素:整个原子的能量由
您最近一年使用:0次
7 . 已知 R2+核内共有 12 个中子,R 的质量数为 24,则:
(1)该元素为______ 元素?
(2)4g R 的氧化物含有电子数为_____
(3)若2.4g的 R 单质溶于 200mL的盐酸溶液中,形成溶液溶质的物质的量浓度为______ ?(假设反应前后溶液体积无变化)
(1)该元素为
(2)4g R 的氧化物含有电子数为
(3)若2.4g的 R 单质溶于 200mL的盐酸溶液中,形成溶液溶质的物质的量浓度为
您最近一年使用:0次
8 . 某元素的同位素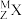 ,已知 M=30,且 M−Z=16,则:
,已知 M=30,且 M−Z=16,则:
(1)X 元素为_______
(2)X 的气态氢化物电子式_______
(3)X 氧化物与强碱 NaOH 溶液反应的化学方程式_______ 。
(4)X 氧化物与酸反应的化学方程式_______ 。
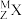 ,已知 M=30,且 M−Z=16,则:
,已知 M=30,且 M−Z=16,则:(1)X 元素为
(2)X 的气态氢化物电子式
(3)X 氧化物与强碱 NaOH 溶液反应的化学方程式
(4)X 氧化物与酸反应的化学方程式
您最近一年使用:0次
解题方法
9 . 有A.质子数、B.中子数、C.核外电子数、D.最外层电子数、E.电子层数,用代表上述概念的序号,完成下列问题:
(1)原子种类由_______ 决定。
(2)元素种类由_______ 决定。
(3)同位素相对原子质量由_______ 决定。
(4)元素的化合价主要由_______ 决定。
(1)原子种类由
(2)元素种类由
(3)同位素相对原子质量由
(4)元素的化合价主要由
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
10 . 电子云
①定义:处于一定空间_______ 的电子在原子核外空间的概率密度分布的形象化描述。
②含义:用单位体积内小黑点的疏密程度表示电子在原子核外出现概率大小,小黑点越_______ ,表示概率密度越_______ 。
③形状
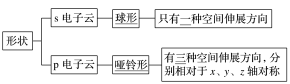
①定义:处于一定空间
②含义:用单位体积内小黑点的疏密程度表示电子在原子核外出现概率大小,小黑点越
③形状

您最近一年使用:0次



