地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)___________ ;
(2)由极性键构成的非极性分子有___________ ;
(3)与 可直接形成配位键的分子有
可直接形成配位键的分子有___________ ;
(4)分子中不含孤电子对的分子有___________ ,它的立体构型为___________ ;
(5)极易溶于水、且水溶液呈碱性的物质的分子是___________ ,它极易溶于水的原因是___________ 。
| 目前空气的成分 |  、 、 、 、 、水蒸气及稀有气体(如He、Ne等) 、水蒸气及稀有气体(如He、Ne等) |
| 原始大气的主要成分 |  、 、 、CO、 、CO、 等 等 |
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)
(2)由极性键构成的非极性分子有
(3)与
 可直接形成配位键的分子有
可直接形成配位键的分子有(4)分子中不含孤电子对的分子有
(5)极易溶于水、且水溶液呈碱性的物质的分子是
更新时间:2023-05-08 16:22:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)1 mol NH3中所含质子数与____ molH2O、___ mol HF中所含质子数相等。
(2)和Ne原子具有相同电子数和质子数的多核微粒有____________ 。
(2)和Ne原子具有相同电子数和质子数的多核微粒有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成电石(CaC2),电石与水反应生成Ca(OH)2和一种4原子气体分子。
①写出电石与水反应的化学方程式_______ ;反应制得的气体中通常会含有硫化氢等杂质气体,可用_______ 吸收。
②CaCO3中阴离子的空间构型为_______ 。
③该气体分子中σ键与π键的数目之比为_______ 。
④写出2种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(3)工业上电解CaCl2制Ca而不采用电解CaO的原因是_______ 。
(4)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为_______ 、_______ 。

(1)基态铜原子的价电子排布式为
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成电石(CaC2),电石与水反应生成Ca(OH)2和一种4原子气体分子。
①写出电石与水反应的化学方程式
②CaCO3中阴离子的空间构型为
③该气体分子中σ键与π键的数目之比为
④写出2种与
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(3)工业上电解CaCl2制Ca而不采用电解CaO的原因是
(4)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】光刻机是生成计算机芯片的机器。某光刻胶(X)的合成反应如图:
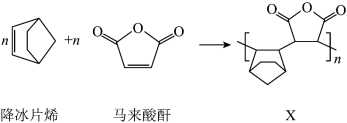
下列说法正确的是_______ 。
A.马来酸酐中C原子有sp2和sp3两种杂化方式
B.1molX最多可与2molNaOH反应
C.马来酸酐的某种同分异构体中所有碳原子共线
D.降冰片烯能发生加成反应,不能发生取代反应
E.马来酸酐的分子式为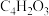

下列说法正确的是
A.马来酸酐中C原子有sp2和sp3两种杂化方式
B.1molX最多可与2molNaOH反应
C.马来酸酐的某种同分异构体中所有碳原子共线
D.降冰片烯能发生加成反应,不能发生取代反应
E.马来酸酐的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据VSEPR,确定CO2、SO2、CO 、H2O、NH3、CH4、NH
、H2O、NH3、CH4、NH 分子的空间结构。
分子的空间结构。
 、H2O、NH3、CH4、NH
、H2O、NH3、CH4、NH 分子的空间结构。
分子的空间结构。| 分子或离子 | 孤电子对数 | 价层电子对数 | VSEPR模型名称 | 分子或离子的空间结构名称 |
| CO2 | ||||
| SO2 | ||||
CO | ||||
| H2O | ||||
| NH3 | ||||
| CH4 | ||||
NH |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】配合物在生产生活中应用广泛,配合物的种类超过了百万,是一个庞大的化合物家族。回答下列问题:
(1)向 溶液中加入足量的氨水,先生成蓝色沉淀,后蓝色沉淀溶解可得到深蓝色
溶液中加入足量的氨水,先生成蓝色沉淀,后蓝色沉淀溶解可得到深蓝色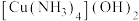 溶液。
溶液。
①蓝色沉淀溶于氨水的离子方程式为___________ 。
②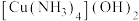 中所含配位键是通过配体分子中的
中所含配位键是通过配体分子中的___________ 原子给出孤电子对,___________ 接受电子对形成。
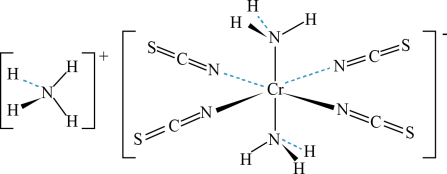
(2)雷氏盐(Reinecke’s salt)结构式如图所示。配离子中 的配体为
的配体为___________ (填化学式), 与配体间形成的共价键又称为
与配体间形成的共价键又称为___________ 。
(3) 中的Ni与CO中的C形成配位键。不考虑立体构型,
中的Ni与CO中的C形成配位键。不考虑立体构型, 结构中的配位键可用示意图表示为
结构中的配位键可用示意图表示为___________ 。
(4)钒能形成多种配合物,钒的两种配合物X、Y的化学式均为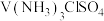 ,取X、Y溶液进行如下实验(已知配体难电离出来)。
,取X、Y溶液进行如下实验(已知配体难电离出来)。
则X中配离子的化学式为___________ ,Y中 的配体是
的配体是___________ 。
(1)向
 溶液中加入足量的氨水,先生成蓝色沉淀,后蓝色沉淀溶解可得到深蓝色
溶液中加入足量的氨水,先生成蓝色沉淀,后蓝色沉淀溶解可得到深蓝色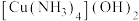 溶液。
溶液。①蓝色沉淀溶于氨水的离子方程式为
②
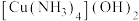 中所含配位键是通过配体分子中的
中所含配位键是通过配体分子中的(2)雷氏盐(Reinecke’s salt)结构式如图所示。配离子中
 的配体为
的配体为 与配体间形成的共价键又称为
与配体间形成的共价键又称为
(3)
 中的Ni与CO中的C形成配位键。不考虑立体构型,
中的Ni与CO中的C形成配位键。不考虑立体构型, 结构中的配位键可用示意图表示为
结构中的配位键可用示意图表示为(4)钒能形成多种配合物,钒的两种配合物X、Y的化学式均为
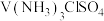 ,取X、Y溶液进行如下实验(已知配体难电离出来)。
,取X、Y溶液进行如下实验(已知配体难电离出来)。| 配合物 | X | X | Y | Y |
| 试剂 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
 的配体是
的配体是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】从金矿石提炼黄金往往采用氰化法提金。用稀的氰化钠溶液处理粉碎的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的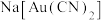 ,这与钢铁的电化学腐蚀相似,其反应方程式为
,这与钢铁的电化学腐蚀相似,其反应方程式为 ,最后再用Zn将
,最后再用Zn将 置换成金单质。
置换成金单质。
(1)下列关于氰化法说法不正确的是___________(复选)
(2)NaCN的电子式为___________ 。
(3)在空气中用氰化钠溶液提取金的正极反应式为 ,则负极反应式为
,则负极反应式为___________ 。
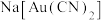 ,这与钢铁的电化学腐蚀相似,其反应方程式为
,这与钢铁的电化学腐蚀相似,其反应方程式为 ,最后再用Zn将
,最后再用Zn将 置换成金单质。
置换成金单质。(1)下列关于氰化法说法不正确的是___________(复选)
| A.Au是一种活泼金属 |
B.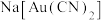 中存在离子键、配位键和非极性共价键 中存在离子键、配位键和非极性共价键 |
C.若无NaCN作用,Au难被 氧化 氧化 |
| D.氰化法的废液直接排放会带来环境污染问题 |
(3)在空气中用氰化钠溶液提取金的正极反应式为
 ,则负极反应式为
,则负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入乙醇,溶液中将析出深蓝色的晶体。
(1)写出该深蓝色晶体的化学式:________________________
(2)写出整个反应过程中的离子方程式:_________________ 、________________ 。
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:__________________ 。
(4)乙醇分子的极性_____ (大于、小于、等于)水分子的极性;乙醇能够和水互溶的原因是___________ 。
(1)写出该深蓝色晶体的化学式:
(2)写出整个反应过程中的离子方程式:
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:
(4)乙醇分子的极性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上可以用NaCl溶液制取重要的化工原料纯碱,此化工流程还需要一定量的CO2和NH3。
(1)NH3的分子构型是_______ ,用电子式表示NH3分子的形成过程_______ 。
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是_______ ,氮气分子的结构式是_______ 。
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是_______ ,它是_______ (填“极性”或“非极性”)分子。
(1)NH3的分子构型是
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硒是动物和人体所必需的微量元素之一,在周期表中信息如图所示。完成下列填空:

(1)Se元素在周期表中的位置为___ 。表中78.96的意义为__ 。Se原子最外层电子排布的轨道表示式为___ 。
(2)从原子结构角度解释硫的非金属性大于硒___ 。
(3)硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种___ (选填“极性、或非极性”)分子,其空间结构为___ 型。
(4)工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式___ 。理论上该反应每转移1mol电子,可得到SeO2的质量为___ g,得到SO2在标准状况下的体积为___ L。

(1)Se元素在周期表中的位置为
(2)从原子结构角度解释硫的非金属性大于硒
(3)硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种
(4)工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】工业制备纯碱的原理为:NaCl+CO2+NH3+H2O=NH4Cl+ NaHCO3↓。完成下列填空:
(1)上述反应体系中出现的几种短周期元素,非金属性最强的是_____ ,第二周期原子半径由大到小的是______ 。
(2)反应体系中出现的非金属元素可形成多种化合物 ,其中和铵根离子空间构型相同且属于有机物的电子式是______ ,该分子为_____ ( 选填“极性”、“非极性”)分子。
(3)写出上述元素中有三个未成对电子的原子核外电子排布式_____ ,下列关于该元素和氧元素之间非金属性大小判断依据正确的是____ (填编号)
a.最高价氧化物对应水化物的酸性 b.两元素形成化合物的化合价
c.气态氢化物的稳定性 d. 氢化物水溶液的酸碱性
(4)有人设想冰的晶胞也应该类似于金刚石,但实际较为复杂,可能是因为氢键较弱而导致“饱和性和方向性”很难被严格执行。例如:有文献报道氨晶体中每个氢原子都形成氢键,则每个NH3与周围______ 个NH3通过氢键相结合。
(5)化合物 FeF3熔点高于1000℃,而Fe(CO)5 的熔点却低于 0℃,FeF3熔点远高于Fe(CO)5的原因可能是_____________ 。
(1)上述反应体系中出现的几种短周期元素,非金属性最强的是
(2)反应体系中出现的非金属元素可形成多种化合物 ,其中和铵根离子空间构型相同且属于有机物的电子式是
(3)写出上述元素中有三个未成对电子的原子核外电子排布式
a.最高价氧化物对应水化物的酸性 b.两元素形成化合物的化合价
c.气态氢化物的稳定性 d. 氢化物水溶液的酸碱性
(4)有人设想冰的晶胞也应该类似于金刚石,但实际较为复杂,可能是因为氢键较弱而导致“饱和性和方向性”很难被严格执行。例如:有文献报道氨晶体中每个氢原子都形成氢键,则每个NH3与周围
(5)化合物 FeF3熔点高于1000℃,而Fe(CO)5 的熔点却低于 0℃,FeF3熔点远高于Fe(CO)5的原因可能是
您最近一年使用:0次



