名校
解题方法
1 . 《自然》杂志曾报道我国科学家通过测量 中
中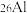 和
和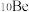 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)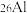 和
和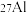 ___________。
___________。
(2)自然界一共存在三种硅的稳定同位素,分别是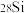 、
、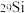 、
、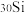 。
。
① 原子的结构示意图为
原子的结构示意图为___________ 。
②计算硅元素的近似相对原子质量的计算为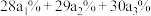 ,其中
,其中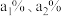 ……是指各同位素的
……是指各同位素的___________ 。
(3)向盐酸中逐滴滴加硅酸钠溶液,当 达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在
达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在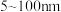 的
的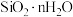 粒子。该分散系属于
粒子。该分散系属于___________ (选填“溶液”“浊液”“胶体”),简单的证明方法是___________ 。
 中
中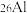 和
和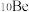 两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:(1)
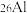 和
和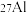 ___________。
___________。| A.是同种元素 | B.是同种核素 | C.具有相同中子数 | D.具有相同性质 |
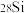 、
、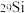 、
、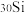 。
。①
 原子的结构示意图为
原子的结构示意图为②计算硅元素的近似相对原子质量的计算为
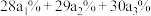 ,其中
,其中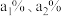 ……是指各同位素的
……是指各同位素的(3)向盐酸中逐滴滴加硅酸钠溶液,当
 达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在
达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在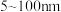 的
的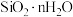 粒子。该分散系属于
粒子。该分散系属于
您最近一年使用:0次
名校
2 . 自然界中的铀和钴都有同位素。铀主要以三种同位素的形式存在,三种同位素的原子百分含量分别为 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式___________ 。(不必算出具体数值)。
 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式
您最近一年使用:0次
名校
解题方法
3 . 第ⅣA族元素R,在它的化合物R(OH)n中,其质量分数为0.778,在它的另一种化合物R(OH)m中,其质量分数为0.636.
(1)试求n和m的值:n=______ ,m=______ 。
(2)试求R的相对原子质量Ar=______ 。
(1)试求n和m的值:n=
(2)试求R的相对原子质量Ar=
您最近一年使用:0次
2024-01-12更新
|
68次组卷
|
2卷引用:海南省海口市长流中学2023-2024学年高一上学期第3次月考化学试题A卷
名校
4 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
名校
解题方法
5 . 读表,回答问题:
 和
和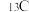 互为
互为______ 关系,请列出碳元素近似相对原子质量的计算表达式______ 。
| 核素 | 相对原子质量 | 丰度(原子分数) |
 | 12(整数,相对原子质量的基准) | 0.9893 |
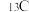 | 13.003354826 | 0.0107 |
 和
和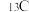 互为
互为
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
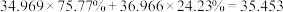
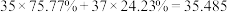
回答下列问题,写出指定数字的含义:
(1)35:__________ ,34.969:__________ 。
(2)75.77%__________ ,35.485__________ 。
| 核素符号 | 原子相对原子质量 | 丰度(%) |
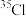 | 34.969 | 75.77% |
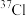 | 36.966 | 24.23% |
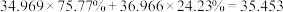
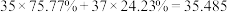
回答下列问题,写出指定数字的含义:
(1)35:
(2)75.77%
您最近一年使用:0次
名校
解题方法
7 . 原子是化学反应中不可再分的基本微粒,自古以来人们对于原子的研究从未停止过。了解了原子的结构,能够帮助人们更好地从微观角度认识物质并推断它们的性质。
(1)下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆孙的观点的是___________。
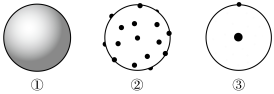
(2)一种元素有质量数分别为35,37的两种核素,该元素的近似相对原子质量为35.5,则两种核素的丰度之比为___________ 。
(3)下列微粒中,具有相同的电子层数与最外层电子数的是___________。
(1)下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆孙的观点的是___________。

| A.①②③ | B.③①② | C.③②① | D.②①③ |
(2)一种元素有质量数分别为35,37的两种核素,该元素的近似相对原子质量为35.5,则两种核素的丰度之比为
(3)下列微粒中,具有相同的电子层数与最外层电子数的是___________。
| A.He与Li | B. 与 与 | C. 与 与 | D. 与Ar 与Ar |
您最近一年使用:0次
名校
8 . 氯元素有两种核素 Cl、
Cl、 Cl。
Cl。
(1)关于 Cl原子说法正确的是
Cl原子说法正确的是_______ 。
(2) Cl、
Cl、 Cl具有
Cl具有_______ 。
(3) Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:_______ 决定元素种类,_______ 决定核素种类。
(4) Cl、
Cl、 Cl互为何种关系
Cl互为何种关系_______ ?
(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:_______ 、_______ 、_______ 。
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→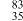 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是_______ 。
(7)已知:氯元素的近似相对原子质量为35.5。STP下,11.2LHCl气体中含H35Cl_______ mol。
 Cl、
Cl、 Cl。
Cl。(1)关于
 Cl原子说法正确的是
Cl原子说法正确的是| A.中子数等于质子数 | B.质子数等于电子数 |
| C.质子数等于质量数 | D.电子数等于中子数 |
 Cl、
Cl、 Cl具有
Cl具有| A.相同质量数 | B.不同质子数 | C.相同中子数 | D.相同电子数 |
 Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:(4)
 Cl、
Cl、 Cl互为何种关系
Cl互为何种关系(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO
 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→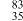 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是| A.该过程发生了化学变化 | B.Br元素的质量数为83 |
C. SeO SeO 中含有68个电子 中含有68个电子 | D. Se与 Se与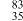 Br互为同位素 Br互为同位素 |
您最近一年使用:0次
名校
解题方法
9 . 观察下列表格,回答相关问题:
(1)其中属于离子化合物的物质有___________ 。
(2)试比较F-、Cl-、Br-的离子半径大小___________ (用元素符号表示);推测离子半径与离子晶体熔点的关系___________ ;猜想KCl的熔点___________ (高于/低于)NaCl的熔点。
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为___________ g(保留2位小数)。
| 物质 | NaF | NaCl | NaBr | KCl | AlCl3 | CH4 | CCl4 |
| 熔点/℃ | 995 | 801 | 755 | 190 | -182.5 | -23 |
(2)试比较F-、Cl-、Br-的离子半径大小
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为
您最近一年使用:0次
名校
解题方法
10 . 自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。
(1)Si原子的结构示意图为_______ 。
(2)28Si是硅的一种同位素,其原子核内质子数为________ ,Si原子的电子式为_______ ,Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素_______ 。
(1)Si原子的结构示意图为
(2)28Si是硅的一种同位素,其原子核内质子数为
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素
您最近一年使用:0次



