名校
1 . 根据2023年最新数据,中国钢铁产量占全球总产量的53.9%,铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为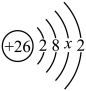 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是___________ ,铁原子核外 轨道上共填充了
轨道上共填充了___________ 个电子。
(2)铁原子中有___________ 种能量不同的电子,铁原子次外层的电子云有_种不同的伸展方向。
(3)自然界一共存在四种稳定的铁原子,分别是 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为___________ 。计算铁元素的近似相对质量的计算式为: ,其中
,其中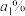 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的___________ 。
(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
(5) 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是___________ (用离子方程式表示)。
(6)向新配制的 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:
___ +___
+___ +____
+____ =____
=____ +____
+____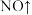 +____
+____
①配平上述反应__________ 。
②每生成0.5moI 气体,转移的电子数为
气体,转移的电子数为___________ 。
③要检验该反应后的溶液中是否还含有 ,实验方案是
,实验方案是___________ 。
(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式___________ 。
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:___________ 。
(1)铁的原子结构示意图为
 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是 轨道上共填充了
轨道上共填充了(2)铁原子中有
(3)自然界一共存在四种稳定的铁原子,分别是
 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为 ,其中
,其中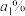 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
A. | B. | C. | D. |
(5)
 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是(6)向新配制的
 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:___
 +___
+___ +____
+____ =____
=____ +____
+____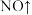 +____
+____
①配平上述反应
②每生成0.5moI
 气体,转移的电子数为
气体,转移的电子数为③要检验该反应后的溶液中是否还含有
 ,实验方案是
,实验方案是(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:
您最近一年使用:0次
名校
2 . Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______ (填序号,下同);
(2)互为同素异形体的是_____ ;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___ 种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____ ;
(2)用电子式表示二氧化碳分子的形成过程_________ ;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______ (填序号,下同);
(2)含有极性键的离子化合物是_________ ;
(3)氟化氢水溶液中存在的氢键有________ 种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____ 。
(1)互为同位素的是
(2)互为同素异形体的是
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式
(2)用电子式表示二氧化碳分子的形成过程
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是
(2)含有极性键的离子化合物是
(3)氟化氢水溶液中存在的氢键有
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为
您最近一年使用:0次
解题方法
3 . 现有下列粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、37Cl、14N、14C,请回答下列问题:
(1)它们分属_____ 种元素,属于氢元素的核素有_____ 种,属于铀元素的核素有_____ 种。互为同位素的原子分别为__________ 。
(2)质量数相等的粒子为_______ 、_______ 、_______ 。
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为__________ ;可得相对分子质量不同的水分子的种数为__________ 。
(1)它们分属
(2)质量数相等的粒子为
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为
您最近一年使用:0次



