1 . (1)写出表示含有8个质子,10个中子的原子的化学符号:______ ;
(2)最外层电子数为次外层电子数 的原子
的原子______ 或______ ;(填元素符号)
(3)根据下列微粒回答问题:
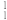 H、
H、 H、
H、 H、
H、 C、
C、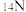 、
、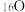 、
、 、
、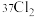
①以上8种微粒共有______ 种核素,共______ 种元素.
②互为同位素的是______ .
③质量数相等的是______ 和______ ,中子数相等的是______ 和______ .
(2)最外层电子数为次外层电子数
 的原子
的原子(3)根据下列微粒回答问题:
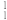 H、
H、 H、
H、 H、
H、 C、
C、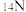 、
、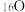 、
、 、
、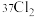
①以上8种微粒共有
②互为同位素的是
③质量数相等的是
您最近一年使用:0次
2 . (1)写出表示含有8个质子,10个中子的原子的化学符号:________ 。
(2)根据下列微粒回答问题: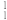 H、
H、 H、
H、 H、
H、 C、
C、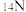 、
、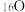 、
、 、
、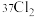 。
。
①以上8种微粒共有________ 种核素,共________ 种元素。
②互为同位素的是________ 。
③质量数相等的是________ 和________ ,中子数相等的是________ 和________ 。
(3)相同物质的量的 与
与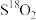 的质量之比为
的质量之比为________ ;中子数之比为________ ;电子数之比为________ 。
(4)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是______________ 。(铷的相对原子质量取85.5)
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为________ 。
(2)根据下列微粒回答问题:
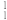 H、
H、 H、
H、 H、
H、 C、
C、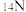 、
、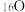 、
、 、
、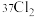 。
。①以上8种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的
 与
与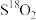 的质量之比为
的质量之比为(4)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为
您最近一年使用:0次
3 . 氯元素有两种天然同位素:3517Cl、3717Cl。
(1)在形成的Cl2分子中,会有__________ 种不同的分子,它们的相对分子质量分别是_______ 。
(2)从原子的结构看,原子的质量数均为整数,但氯元素的相对原子质量却是35.5,这是为什么?________________________________
(1)在形成的Cl2分子中,会有
(2)从原子的结构看,原子的质量数均为整数,但氯元素的相对原子质量却是35.5,这是为什么?
您最近一年使用:0次
4 . (1)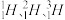 是三种不同的
是三种不同的_____ ,它们互为_____ ,它们都属于氢_____ (填元素,核素,同位素)
(2)α射线是由α粒子组成的,α粒子是一种没有核外电子的粒子,它带有两个 单位的正电荷,质量数等于 4,由此可推断α粒子有______ 个质子,_______ 个 中子。
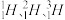 是三种不同的
是三种不同的(2)α射线是由α粒子组成的,α粒子是一种没有核外电子的粒子,它带有两个 单位的正电荷,质量数等于 4,由此可推断α粒子有
您最近一年使用:0次
2018高二·全国·专题练习
解题方法
5 . 现有下列粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、37Cl、14N、14C,请回答下列问题:
(1)它们分属_____ 种元素,属于氢元素的核素有_____ 种,属于铀元素的核素有_____ 种。互为同位素的原子分别为__________ 。
(2)质量数相等的粒子为_______ 、_______ 、_______ 。
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为__________ ;可得相对分子质量不同的水分子的种数为__________ 。
(1)它们分属
(2)质量数相等的粒子为
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为
您最近一年使用:0次
2016高一·全国·课时练习
6 . (1)H、D、T三种核素,它们之间的关系是______ ;在标准状况下,它们形成的单质的密度之比是___________ ;1 mol各单质中所含的质子数之比是_________ ;在标准状况下,1 L各种单质中所含电子数之比是____ 。
(2)核内中子数为N的R2+,质量数为A,则n g它的同价态氧化物中所含电子的物质的量为___________ 。
(3)含6.02×1023个中子的Li的质量是_________ ;4 g D2和20 g 18O2的单质化合时最多能生成______ g O。
(2)核内中子数为N的R2+,质量数为A,则n g它的同价态氧化物中所含电子的物质的量为
(3)含6.02×1023个中子的Li的质量是
您最近一年使用:0次



