1 . 某元素X构成的气态单质分子(双原子分子)有三种,其相对分子质量分别为70、72、74,标背状况下,V升该气体中此三种分子的物质的量之比为9∶6∶1.完成下列问题:
(1)X元素有_______ 种核素。
(2)各种核素的质量数分别为_______ 。
(3)X2的平均相对分子质量为_______ 。
(4)质量数较小的X原子的物质的量分数为_______ 。
(1)X元素有
(2)各种核素的质量数分别为
(3)X2的平均相对分子质量为
(4)质量数较小的X原子的物质的量分数为
您最近一年使用:0次
2 . 1993年8月,国际原子量委员会确认我国张青莲教授测定的锑(Sb)的相对原子质量为标准相对原子质量。选择下表提供的数据计算:
(1)锑元素的相对原子质量_________ (结果保留3位小数);
(2)121Sb的质量分数_______ %(结果保留2位小数)。
同位素 | 相对原子质量 | 质量数 | 丰度 |
121Sb | 120.904 | 121 | 57.36% |
123Sb | 122.904 | 123 | 42.64% |
(1)锑元素的相对原子质量
(2)121Sb的质量分数
您最近一年使用:0次
20-21高一上·浙江·期中
解题方法
3 . 氢元素有三种同位素H、D、T,氯元素有两种同位素35Cl、37Cl,氧原子有三种同位素16O、17O、18O。
(1)自然界中的水分子一共有___ 种;
(2)若用一种仪器分别测定10000个氯化氢的相对分子质量,所得数值最多有___ 种。
(1)自然界中的水分子一共有
(2)若用一种仪器分别测定10000个氯化氢的相对分子质量,所得数值最多有
您最近一年使用:0次
名校
解题方法
4 . 现有下列基本粒子:1H、2H、3H、1H+、234U、235U、238U、14N3-、40K、40Ca、Cl2、14N、14C,请回答下列问题:
(1)其中,含有__ 种元素,属于氢元素的核素有__ 种,属于铀元素的核素有__ 种,互为同位素的原子分别是__ ,__ 。
(2)质量数相等的粒子为__ ,__ ,__ (可不填满,也可补充)。
(3)氢元素的同位素1H、2H、3H与氧元素的同位素16O、17O、18O相互结合为水,可得水分子的种数为__ ,可得__ 种不同的相对分子质量。
(4)0.1mol14N3-中共含__ mol中子,含__ 个电子。
(1)其中,含有
(2)质量数相等的粒子为
(3)氢元素的同位素1H、2H、3H与氧元素的同位素16O、17O、18O相互结合为水,可得水分子的种数为
(4)0.1mol14N3-中共含
您最近一年使用:0次
5 . (1)写出表示含有8个质子,10个中子的原子的化学符号:______ ;
(2)最外层电子数为次外层电子数 的原子
的原子______ 或______ ;(填元素符号)
(3)根据下列微粒回答问题:
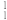 H、
H、 H、
H、 H、
H、 C、
C、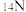 、
、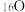 、
、 、
、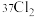
①以上8种微粒共有______ 种核素,共______ 种元素.
②互为同位素的是______ .
③质量数相等的是______ 和______ ,中子数相等的是______ 和______ .
(2)最外层电子数为次外层电子数
 的原子
的原子(3)根据下列微粒回答问题:
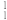 H、
H、 H、
H、 H、
H、 C、
C、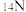 、
、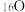 、
、 、
、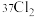
①以上8种微粒共有
②互为同位素的是
③质量数相等的是
您最近一年使用:0次
6 . (1)写出表示含有8个质子,10个中子的原子的化学符号:________ 。
(2)根据下列微粒回答问题: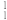 H、
H、 H、
H、 H、
H、 C、
C、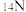 、
、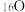 、
、 、
、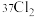 。
。
①以上8种微粒共有________ 种核素,共________ 种元素。
②互为同位素的是________ 。
③质量数相等的是________ 和________ ,中子数相等的是________ 和________ 。
(3)相同物质的量的 与
与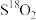 的质量之比为
的质量之比为________ ;中子数之比为________ ;电子数之比为________ 。
(4)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是______________ 。(铷的相对原子质量取85.5)
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为________ 。
(2)根据下列微粒回答问题:
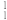 H、
H、 H、
H、 H、
H、 C、
C、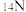 、
、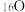 、
、 、
、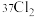 。
。①以上8种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的
 与
与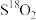 的质量之比为
的质量之比为(4)铷和另一种碱金属形成的合金7.8g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为
您最近一年使用:0次
7 . 某元素单质R质量为5.4g,跟足量的氯气反应可生成RCl3质量为26.7g,已知R原子中质子数比中子数少一个。
(1)求R的相对原子质量;___
(2)写出R的原子结构示意图和R离子的电子式。___ 、___
(1)求R的相对原子质量;
(2)写出R的原子结构示意图和R离子的电子式。
您最近一年使用:0次
8 . (将某文献资料上记载的原子量数据摘录如下):
试回答下列问题:
(1)24.23%是表示___ ;
(2)34.969是表示____ ;
(3)34.453是表示___ ;
(4)35是表示___ 。
| 35Cl | 34.969 | 75.77% | 35Cl | 35 | 75.77% |
| 37Cl | 36.966 | 24.23% | 37Cl | 37 | 24.23% |
| 平均 | 35.453 | 平均 | 35.485 | ||
(1)24.23%是表示
(2)34.969是表示
(3)34.453是表示
(4)35是表示
您最近一年使用:0次
名校
9 . 自然界中氢有_______ 种同位素,他们的中文名分别为________________ ,若用符号来表示,则分别为______________ ,自然界中氧也有三种同位素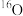 、
、 、
、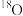 ,从水分子的原子组成来看,自然界中的水分子理论上有
,从水分子的原子组成来看,自然界中的水分子理论上有____________ 种,这些水分子的相对分子质量有__________ 种。
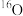 、
、 、
、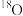 ,从水分子的原子组成来看,自然界中的水分子理论上有
,从水分子的原子组成来看,自然界中的水分子理论上有
您最近一年使用:0次
名校
10 . Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______ (填序号,下同);
(2)互为同素异形体的是_____ ;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___ 种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____ ;
(2)用电子式表示二氧化碳分子的形成过程_________ ;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______ (填序号,下同);
(2)含有极性键的离子化合物是_________ ;
(3)氟化氢水溶液中存在的氢键有________ 种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____ 。
(1)互为同位素的是
(2)互为同素异形体的是
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式
(2)用电子式表示二氧化碳分子的形成过程
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是
(2)含有极性键的离子化合物是
(3)氟化氢水溶液中存在的氢键有
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为
您最近一年使用:0次



