解题方法
1 . 已知一个12C原子的质量为1.993×10-23 g。填表:(保留三位小数)
| 35Cl | 37Cl | |
| 原子质量(×10-23 g) | 5.807 | 6.139 |
| 相对原子质量 | ① | ② |
| 原子百分率(丰度) | 74.82% | 25.18% |
| 元素的相对原子质量 | ③ | |
您最近一年使用:0次
名校
解题方法
2 . 已知一个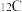 原子的质量为1.993×10-23g,填表:(保留三位小数)
原子的质量为1.993×10-23g,填表:(保留三位小数)
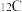 原子的质量为1.993×10-23g,填表:(保留三位小数)
原子的质量为1.993×10-23g,填表:(保留三位小数) |  | |
| 原子质量(×10-23g) | 5.807 | 6.139 |
| 相对原子质量 | ||
| 丰度(%) | 75 | 25 |
| 元素相对原子质量 |
您最近一年使用:0次
名校
3 . 已知硼有两种同位素原子10B和11B,若硼的相对原子质量为10.8,则10B的质量百分含量为____ 。
您最近一年使用:0次
2020-02-12更新
|
576次组卷
|
2卷引用:人教版 高中化学 必修2 第一章《物质结构元素周期律》单元检测题
真题
4 . 氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式___________ 。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为___________ L。
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量___________ 。
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比____________ 。②吸收后氨水的物质的量浓度_______________ (答案保留1位小数)。
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
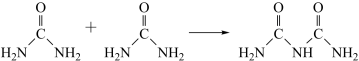 +NH3
+NH3
已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比__________ 。
根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。
由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,计算推进剂中联氨的质量
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。计算:①该混合气体中NO与NO2的体积比
(4)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
 +NH3
+NH3已知常压下120 mol CO(NH2)2在熔融状态发生缩合反应,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比
您最近一年使用:0次
2020-02-10更新
|
775次组卷
|
2卷引用:2020届人教版高中化学高三专题基础复习专题2《物质及其变化》测试卷
5 . (1)将Ag某金属R溶于盐酸,产生氢气体的体积时BL(标准状况),生成的氯化物化学式是RCl2,这种金属的相对原子质量是___ 。
(2)标准状况下,某气体的密度为1.977g/L,该物质摩尔质量为___ 。
(2)标准状况下,某气体的密度为1.977g/L,该物质摩尔质量为
您最近一年使用:0次
名校
6 . 某核素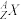 的氯化物XCl2 0.95g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的氯化物XCl2 0.95g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数为_________ 。
(2)若X的核内中子数为12,求47.5gXCl2中所含质子的物质的量是________ 。
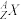 的氯化物XCl2 0.95g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的氯化物XCl2 0.95g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:(1)X的质量数为
(2)若X的核内中子数为12,求47.5gXCl2中所含质子的物质的量是
您最近一年使用:0次
2019-10-31更新
|
311次组卷
|
3卷引用:上海市复旦大学附中2015-2016学年高一上学期期中考试化学试题
名校
7 . 某物质H2RO3分子中共有x个电子,R原子的质量数为A,则R原子核内含有_______ 个质子,________ 个中子。
您最近一年使用:0次
2019-10-30更新
|
498次组卷
|
3卷引用:上海交通大学附属中学2017-2018学年高一化学原子结构练习2:原子结构和相对原子质量1
名校
8 . 某元素的原子为AZX,9.5g该元素的氯化物XCl2配成溶液后,需用200mL 1mol/L的AgNO3溶液才能把氯离子沉淀完全,已知,X元素核内质子数和中子数相等。
(1)据此请计算出A值______________ ,
(2)写出该元素符号并确定其在周期性表中的位置______________ 。
(1)据此请计算出A值
(2)写出该元素符号并确定其在周期性表中的位置
您最近一年使用:0次
9 . 某元素原子的氯化物化学式为MCl2,现将20.8 g该氯化物溶于水配成溶液后,需用200 mL 1 mol·L-1 AgNO3溶液才能把溶液中氯离子完全沉淀。已知该M原子中有81个中子,则:
(1)计算M的质量数并写出该核素的表示符号。______________
(2)指出M元素在周期表中的位置(周期、族)。_____________
(1)计算M的质量数并写出该核素的表示符号。
(2)指出M元素在周期表中的位置(周期、族)。
您最近一年使用:0次
9-10高一下·福建龙岩·期中
解题方法
10 . 某元素的同位素X,它的氯化物XCl 1.49g溶于水制成溶液后,加入1mol·L-1的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,试通过计算确定(写出计算过程):
(1)X元素在周期表中的位置________ ;
(2)把一小粒X的单质放入水中,有何现象_________ ? 写出反应的化学方程式____ 。
(1)X元素在周期表中的位置
(2)把一小粒X的单质放入水中,有何现象
您最近一年使用:0次



